
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察如图,然后回答问题: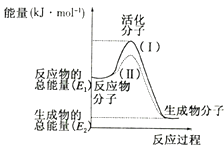
(1)图中所示反应是(填“吸热”或“放热”)反应,该反应的△H=(用含E1、E2的代数式表示).
(2)下列4个反应中符合示意图描述的反应的是 (填代号).
A.水蒸气与炭反应
B.用水稀释氢氧化钠溶液
C.铝粉与Fe2O3反应
D.灼热的碳与CO2反应
(3)已知热化学方程式:H2(g)+ ![]() O2 (g)=H2O(g)△H=﹣241.8kJ/mol.该反应的活化能为167.2kJ/mo1,则其逆反应的活化能为 .
O2 (g)=H2O(g)△H=﹣241.8kJ/mol.该反应的活化能为167.2kJ/mo1,则其逆反应的活化能为 .
(4)以甲烷为原料制取氢气是工业上常用的制氢方法.已知:
CH4 (g)+H2O(g)=CO(g)+3H2(g)△H=+206.2kJ/mol
CH4(g)+CO2(g)=2CO(g)+2H2 (g)△H=+247.4kJ/mol
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为 .
【答案】
(1)放热,(E2﹣E1 )KJ/mol
(2)C
(3)409.0KJ/mol
(4)CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=165.0kJ/mol
【解析】解:(1)依据图象分析反应物的能量大于生成物的能量,反应放热;在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才能发生化学反应,反应需要能量;反应的焓变=生成物的能量﹣反应物的能量;△H=(E2﹣E1 )KJ/mol;故答案为:放热;(E2﹣E1 )KJ/mol;(2)图示物质反应前后能量变化礼服业务能量高于生成物反应是放热反应,
A.水蒸气与炭反应需要高温进行,反应是吸热反应,故A不符合;
B.用水稀释氢氧化钠溶液过程中溶液温度变化不大,不是化学反应,故B不符合;
C.铝粉与Fe2O3反应,引发后反应继续进行为放热反应,故C符合;
D.灼热的碳与CO2反应属于吸热反应,故D不符合;
故答案为:C;(3)反应的活化能是使普通分子变成活化分子所需提供的最低限度的能量,依据图象能量关系可知,逆反应的活化能=正反应的活化能+反应的焓变;H2(g)+ ![]() O2(g)═H2O(g)△H=﹣241.8kJmol﹣1,该反应的活化能为167.2kJmol﹣1,则其逆反应的活化能=167.2KJ/mol+241.8KJ/mol=409.0KJ/mol;
O2(g)═H2O(g)△H=﹣241.8kJmol﹣1,该反应的活化能为167.2kJmol﹣1,则其逆反应的活化能=167.2KJ/mol+241.8KJ/mol=409.0KJ/mol;
故答案为:409.0KJ/mol;(4)①CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.2kmol﹣1②CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJmol﹣1
据盖斯定律,①×2﹣②得:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=165.0kmol﹣1,故答案为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0kmol﹣1.
(1)依据图象分析反应物的能量大于生成物的能量,反应放热;在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才能发生化学反应,反应需要能量;反应的焓变=生成物的能量﹣反应物的能量;(2)图示物质反应前后能量变化,反应物能量高于生成物能量,反应是放热反应,据此分析选项中的反应是放热反应的符合;(3)反应的活化能是使普通分子变成活化分子所需提供的最低限度的能量,依据图象能量关系可知,逆反应的活化能=正反应的活化能+反应的焓变;(4)从待求反应出发分析反应物、生成物在所给反应中的位置,通过相互加减可得,据盖斯定律,①×2﹣②得到.


科目:高中化学 来源: 题型:
【题目】如图为以惰性电极进行电解的装置: 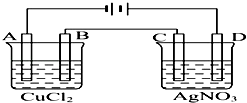
(1)写出A、B、C、D各电极上的电极反应式和总反应方程式: A: , B: , 总反应方程式:;
C: , D: , 总反应方程式: .
(2)在A、B、C、D各电极上析出生成物的物质的量之比为 .
(3)A极发生反应,B极发生反应.(填“氧化”或是“还原”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)是一种重要的清洁燃料气,其储运、燃烧安全性、理论燃烧温度等性能指标均优于液化石油气,也可用作燃烧电池的燃料,具有很好的好展前景.
(1)已知H2、CO和CH3OCH3的燃烧热(△H)分别为﹣285.5kJ/mol、﹣283kJ/mol和﹣1460.0kJ/mol,则工业上利用水煤气成分按1:1合成二甲醚的热化学方程式为
(2)工业上采用电浮远凝聚法处理污水时,保持污水的pH在5.0,通过电解生成Fe(OH)3胶体,吸附不溶性杂质,同时利用阴极产生的H2 , 将悬浮物带到水面,利于除去.实验室以二甲醚燃料电池模拟该方法设计的装置如图所示: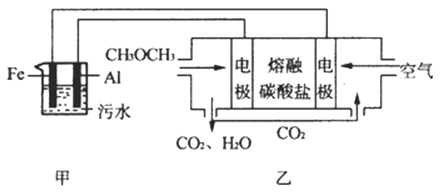
①乙装置以熔融碳酸盐为电解质,稀土金属材料为电极.写出该燃料电池的正极电极反应式 下列物质可用做电池熔融碳酸盐的是
A.MgCO3 B.Na2CO3 C.NaHCO3 D.(NH4)CO3
②写出甲装置中阳极产物离子生成Fe(OH)3沉淀的离子方程式:
③已知常温下Kap[Fe(OH)3]=4.0×10﹣38 , 电解一段时间后,甲装置中c(Fe3+)=
④已知:H2S的电离平衡常数:K1=9.1×10﹣8、K2=1.1×10﹣12;H2CO3的电离平衡常数:K1=4.31×10﹣7、K2=5.61×10﹣11 . 测得电极上转移电子为0.24mol时,将乙装置中生成的CO2通入200mL 0.2mol/L的Na2S溶液中,下列各项正确的是
A.发生反应的离子方程式为:CO2+S2﹣+H2O═CO32﹣+H2S
B.发生反应的离子方程式为:CO2+S2﹣+H2O═HCO3﹣+HS﹣
C.c(Na+)=2[c(H2S)+c(HS﹣)+c(S2﹣)]
D.c(Na+)+c(H+)=2c(CO32﹣)+2c(S2﹣)+c(OH﹣)
E.c(Na+)>c(HCO3﹣)>c(HS﹣)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25℃、101kPa下,1g C8H18(l)燃烧生成CO2和液态H2O时放出48.40kJ的热量,表示上述反应的热化学方程式正确的是( )
A.C8H18(l)+ ![]() O2(g)═8CO2(g)+9H2O(g)△H=﹣48.40 kJmol﹣1
O2(g)═8CO2(g)+9H2O(g)△H=﹣48.40 kJmol﹣1
B.C8H18(l)+ ![]() O2(g)═8CO2(g)+9H2O(l)△H=﹣5 517.6 kJmol﹣1
O2(g)═8CO2(g)+9H2O(l)△H=﹣5 517.6 kJmol﹣1
C.C8H18(l)+ ![]() O2(g)═8CO2(g)+9H2O(g)△H=+5 517.6 kJmol﹣1
O2(g)═8CO2(g)+9H2O(g)△H=+5 517.6 kJmol﹣1
D.2C8H18(l)+25O2(g)═16CO2(g)+18 H2O(l)△H=﹣5 517.6 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】储氢纳米碳管的研究成功体现了科技的进步,但用电孤法合成的碳纳米管常伴有大量的杂质-碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。反应化学方程式为:3C+2K2Cr2O7 +8H2SO4 = 3CO2↑+ 2K2SO4+2Cr2(SO4)3 +8 H2O
(1)上述反应中氧化剂是___________(填化学式), 被氧化的元素是_________(填元素符号)。
(2)H2SO4 在上述反应中表现出来的性质是____________(填选项编号)
A.氧化性 B.氧化性和酸性 C.还原性和酸性 D.酸性
(3)若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为______________L。
(4)请用双线桥法标出电子转移的方向和数目___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烯烃在酸性KMnO4溶液中双键断裂形式为: 
![]()
 现有二烯烃C10H18与酸性KMnO4溶液作用后可得到三种有机物:(CH3)2CO、CH3COOH、CH3CO(CH2)2﹣COOH,由此推断此二烯可能的结构简式为( )
现有二烯烃C10H18与酸性KMnO4溶液作用后可得到三种有机物:(CH3)2CO、CH3COOH、CH3CO(CH2)2﹣COOH,由此推断此二烯可能的结构简式为( )
A.(CH3)2C═C(CH3)CH2CH2CH═CH CH2CH3
B.(CH3)2C═CHCH2CH2C(CH3)═CHCH3
C.CH3CH═C(CH3)CH2CH2CH2C(CH3)═CH2
D.CH3CH═C(CH3)CH2CH2CH2CH═CHCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1mol H﹣O键形成时放出热量463kJ,则氢气中1mol H﹣H键断裂时吸收热量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组准备用环己醇制备环己烯,查得相关资料如下.反应原理:  反应物与产物的物理性质:
反应物与产物的物理性质:
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | ﹣103 | 83 | 难溶于水 |
(1)实验过程中可能发生的有机副反应的方程式为 .
(2)根据上述资料,装置(A,B,C)最适宜用来完成本次制备实验. 
(3)制备粗产品 将5mL加入试管A中,再加入10m , 摇匀后放入碎瓷片,缓慢加热至反应完全.
(4)粗产品提纯 ①环己烯粗产品中含有环己醇和少量酸性杂质等.粗产品需依次经过水洗、加碳酸钠溶液洗涤以及第二次水洗.在此过程中加入碳酸钠溶液的目的是;分液时,环己烯应从分液漏斗的(填“上”或“下”)口取出.
②向水洗后的环己烯中加入少量的无水氯化钙,再将混合物放入图D所示装置的(填仪器名称)中,进行蒸馏,收集产品时,温度计显示的温度应为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用标准的NaOH溶液滴定未知浓度的盐酸,选用酚酞作为指示剂,造成测定结果偏高的原因可能是( )
A.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
B.滴定终点读数时,俯视滴定管的刻度,其他操作正确
C.滴定到终点读数时,发现滴定管尖嘴内有气泡
D.配制标准溶液的NaOH中混有KOH杂质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com