
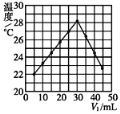
【题目】将V1 mL l.0mol/L盐酸和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V2+V2=50).下列叙述正确的是
A. 做该实验时环境温度为22℃
B. 该实验表明化学能可能转化为热能
C. NaOH溶液的浓度约为1.0 mol/L
D. 该实验表明有水生成的反应都是放热反应
【答案】B
【解析】
A.温度为22℃时加入盐酸10mL,则不是实验温度,故A错误;B.由图示可以看出该反应过程放出热量,表明化学能可能转化为热能,故B正确;C.恰好反应时参加反应的盐酸溶液的体积是30mL,由V1+V2=50mL可知,消耗的氢氧化钠溶液的体积为20mL,设恰好反应时氢氧化钠溶液中溶质的物质的量是n。根据HCl+NaOH=NaCl+H 2O可知,氢氧化钠的物质的量与盐酸的物质的量相等,n=1.0molL-1×0.03L=0.03mol,氢氧化钠的浓度c=![]() =1.5mol/L,故C错误;D.本实验只表示该反应放热,不表示其他有水生成的反应也是放热反应,如氯化铵和氢氧化钡晶体的反应为吸热反应,故D错误;故选B。
=1.5mol/L,故C错误;D.本实验只表示该反应放热,不表示其他有水生成的反应也是放热反应,如氯化铵和氢氧化钡晶体的反应为吸热反应,故D错误;故选B。


科目:高中化学 来源: 题型:
【题目】按要求完成下列问题。
(1)利用VSEPR推断分子或离子的空间构型:![]() ___________;SeO3__________。
___________;SeO3__________。
(2)与SeO3互为等电子体的一种离子为_____(填化学式)。SCN-电子式_______。
(3)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是__。

(4)硒、溴与砷同周期,三种元素的第一电离能从大到小顺序为__________(用元素符号比较)。
(5) 已知常温下Ni(CO)4是无色液体,其构型为正四面体。则配位原子是______,晶体类型为__________,推测其______(填“难”或“易”)溶于水。
(6)CO2晶胞中,与CO2紧邻的CO2有_______个。
(7)酸性比较:H2SeO3______H2SeO4 ,原因_________________________________。
(8)向CuSO4溶液中滴加氨水,溶液先出现沉淀后沉淀溶解,写出沉淀溶解的离子方程式_____________________________,[Cu(H2O)4]2+易转化为[Cu(NH3)4]2+原因__________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g)开始进行时,CO的浓度为4 mol·L-1,N2的浓度为0,2 min后测得N2的浓度为0.6 mol·L-1,则此段时间内,下列反应速率表示正确的是
N2(g)+4CO2(g)开始进行时,CO的浓度为4 mol·L-1,N2的浓度为0,2 min后测得N2的浓度为0.6 mol·L-1,则此段时间内,下列反应速率表示正确的是
A. v(CO)=1.2 mol·L-1·s-1 B. v(NO2)=0.3 mol·L-1·min-1
C. v(N2)=0.6 mol·L-1·min-1 D. v(CO2)=1.2 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Cl2制成漂粉精的主要目的是
A.使它转化为较稳定物质,便于保存和运输
B.增强漂白和消毒作用
C.使它转化为较易溶于水的物质
D.增加氯的质量分数,有利于漂白、消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烷燃料电池的工作原理示意图如下,下列说法中正确的是

A. a 为负极,电极反应式为 CH3CH3-14e-+18OH-===2CO32-+12H2O
B. 电子从 a 极经导线移向 b 极,再经溶液移向 a 极
C. 电池工作一段时间后电解质溶液的 pH 增大
D. 用该电池电解硫酸铜溶液(电解池的电极为惰性电极),消耗氧气的物质的量与析出铜的物质的量之比为 2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。
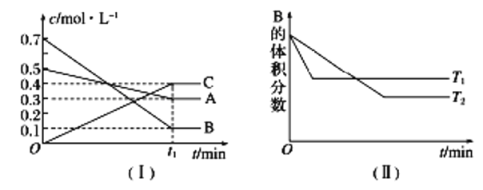
根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为________,正反应为_____(填“吸热”或“放热”)反应。
(2)t1 min后,改变下列某一条件,能使平衡向逆反应方向移动的有______(填字母序号)。
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年5月美国研究人员成功实现在常温常压下用氮气和水生产氨,原理如下图所示:
下列说法正确的是( )

A. 图中能量转化方式只有2种
B. H+向a极区移动
C. b极发生的电极反应为:N2+6H++6e-=2NH3
D. a极上每产生22.4LO2流过电极的电子数一定为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L固定体积的容器中混合,并在一定条件下发生如下反应∶2A(g)+B(g)![]() 2C(g)。若经2s后测得C的浓度为0.6 mol L-1,现有下列几种说法,其中正确的是
2C(g)。若经2s后测得C的浓度为0.6 mol L-1,现有下列几种说法,其中正确的是
A.用物质A表示的反应的平均速率为0.6 mol (L s)-1
B.2 s时物质B的浓度为1.4 mol L-1
C.2 s时物质A的转化率为70%
D.2 s时物质A的体积分数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“分子机器设计和合成”有着巨大的研究潜力。人类步入分子器件时代后,使得光控、温控和电控分子的能力更强,如图所示是蒽醌套索醚电控开关原理。

下列说法错误的是
A. 物质Ⅰ的分子式是C25H28O8
B. 1 mol物质Ⅰ可与8 mol H2发生加成反应
C. 反应[a]是氧化反应
D. 物质Ⅰ的所有原子不可能共平面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com