
”¾ĢāÄæ”æĪŖĮĖŹ¹Óīŗ½Ō±ŌŚ·É“¬ÖŠµĆµ½Ņ»øöĪČ¶ØµÄ”¢Į¼ŗƵÄÉś“ę»·¾³£¬Ņ»°ćŌŚ·É“¬ÄŚ°²×°Ź¢ÓŠNa2O2»ņK2O2æÅĮ£µÄ×°ÖĆ£¬ĖüµÄÓĆĶ¾ŹĒ²śÉśŃõĘų”£ĻĀĮŠ¹ŲÓŚNa2O2µÄŠšŹöÕżČ·µÄŹĒ
¢ŁNa2O2ÖŠŅõ”¢ŃōĄė×ÓµÄøöŹż±ČŹĒ1”Ć1
¢ŚNa2O2·Ö±šÓėĖ®¼°CO2·“Ó¦²śÉśµČĮæŃõĘųŹ±£¬ŠčĖ®ŗĶCO2µÄÖŹĮæĻąµČ
¢ŪNa2O2·Ö±šÓėĖ®¼°CO2·“Ó¦²śÉśµČĮæŃõĘųŹ±£¬×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĻąµČ
¢ÜNa2O2µÄĘÆ°×ŌĄķÓėSO2µÄĘÆ°×ŌĄķĻąĶ¬
¢ŻNa2O2ÓėSO2·“Ӧɜ³ÉNa2SO3ÓėO2
¢ŽNa2O2ÄÜÓėĖį·“Ӧɜ³ÉŃĪŗĶĖ®£¬ĖłŅŌNa2O2ŹĒ¼īŠŌŃõ»ÆĪļ
¢ßNa2O2ÓėĖ®·“Ó¦£¬Na2O2¼ČŹĒŃõ»Æ¼Į£¬ÓÖŹĒ»¹Ō¼Į
¢ąNa2O2Ķ¶Čėµ½×ĻÉ«ŹÆČļČÜŅŗÖŠ£¬ČÜŅŗĻȱ䥶£¬ŗóĶŹÉ«
A.¢Ł¢Ū¢Ž¢ąB.¢Ū¢ß¢ą
C.¢Ś¢Ż¢Ž¢ßD.¢Ł¢Ü¢ą
”¾“š°ø”æB
”¾½āĪö”æ
¢ŁNa2O2ÖŠÓŠ1øöO22-ŗĶ2øöNa+£¬Ņõ”¢ŃōĄė×ÓøöŹż±ČĪŖ1:2£¬¢Ł“ķĪó£»
¢Ś![]() £¬
£¬![]()
![]() £¬²śÉśµČĮæŃõĘų£¬ŠčŅŖ
£¬²śÉśµČĮæŃõĘų£¬ŠčŅŖ![]() ŗĶ
ŗĶ![]() µÄĪļÖŹµÄĮæĻąµČ£¬µ«ÓÉӌĦ¶ūÖŹĮæ²»µČ£¬¹ŹÖŹĮæ²»µČ£¬¢Ś“ķĪó£»
µÄĪļÖŹµÄĮæĻąµČ£¬µ«ÓÉӌĦ¶ūÖŹĮæ²»µČ£¬¹ŹÖŹĮæ²»µČ£¬¢Ś“ķĪó£»
¢ŪĆæ²śÉś![]() ×ŖŅʵē×ÓĪŖ
×ŖŅʵē×ÓĪŖ![]() £¬²śÉśŃõĘųµÄĮæĻąµČ£¬×ŖŅʵē×ÓĻąµČ£¬¢ŪÕżČ·£»
£¬²śÉśŃõĘųµÄĮæĻąµČ£¬×ŖŅʵē×ÓĻąµČ£¬¢ŪÕżČ·£»
¢ÜNa2O2ĘÆ°×ŹĒĄūÓĆĘäĒæŃõ»ÆŠŌ£¬¶ųSO2ĘÆ°×ŹĒÓÉÓŚ½įŗĻÓŠÉ«ĪļÖŹÉś³ÉĮĖ²»ĪČ¶ØµÄĪŽÉ«ĪļÖŹ£¬ŌĄķ²»ĻąĶ¬£¬¢Ü“ķĪó£»
¢ŻNa2O2¾ßÓŠĒæŃõ»ÆŠŌ£¬ÄÜŃõ»ÆSO2£¬![]() £¬¢Ż“ķĪó£»
£¬¢Ż“ķĪó£»
¢ŽNa2O2ÄÜÓėĖį·“Ӧɜ³ÉŃĪ”¢Ė®ŗĶŃõĘų£¬¹żŃõ»ÆÄĘŹōÓŚ¹żŃõ»ÆĪļ£¬¢Ž“ķĪó£»
¢ß![]() £¬Na2O2ÖŠŃõµÄ»ÆŗĻ¼Ū¼ČÉżøßÓÖ½µµĶ£¬Na2O2¼ČŹĒŃõ»Æ¼Į£¬ÓÖŹĒ»¹Ō¼Į£¬¢ßÕżČ·£»
£¬Na2O2ÖŠŃõµÄ»ÆŗĻ¼Ū¼ČÉżøßÓÖ½µµĶ£¬Na2O2¼ČŹĒŃõ»Æ¼Į£¬ÓÖŹĒ»¹Ō¼Į£¬¢ßÕżČ·£»
¢ą![]() £¬ČÜŅŗ³Ź¼īŠŌ£¬¹Ź±äĄ¶£¬µ«ÓÉÓŚNa2O2ĒæŃõ»ÆŠŌ£¬ÄÜĘÆ°×£¬¹ŹĶŹÉ«£¬¢ąÕżČ·£»
£¬ČÜŅŗ³Ź¼īŠŌ£¬¹Ź±äĄ¶£¬µ«ÓÉÓŚNa2O2ĒæŃõ»ÆŠŌ£¬ÄÜĘÆ°×£¬¹ŹĶŹÉ«£¬¢ąÕżČ·£»
×ŪÉĻ£¬ÕżČ·µÄĪŖ¢Ū¢ß¢ą”£
“š°øŃ”B”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©ŌŚ¢ŁCO2£¬¢ŚNaCl£¬¢ŪNa£¬¢ÜSi£¬¢ŻCS2£¬¢Ž½šøÕŹÆ£¬¢ß£ØNH4£©2SO4£¬¢ąŅŅ“¼ÖŠ£¬Óɼ«ŠŌ¼üŠĪ³ÉµÄ·Ē¼«ŠŌ·Ö×ÓÓŠ_______£ØĢīŠņŗÅ£¬ŅŌĻĀĶ¬£©£¬ŗ¬ÓŠ½šŹōĄė×ÓµÄĪļÖŹŹĒ__£¬·Ö×Ó¼äæÉŠĪ³ÉĒā¼üµÄĪļÖŹŹĒ________£¬ŹōÓŚĄė×Ó¾§ĢåµÄŹĒ__£¬ŹōÓŚŌ×Ó¾§ĢåµÄŹĒ__£¬¢Ł”«¢ŻĪåÖÖĪļÖŹµÄČŪµćÓÉøßµ½µĶµÄĖ³ŠņŹĒ__”£
£Ø2£©A£¬B£¬C£¬DĪŖĖÄÖÖ¾§Ģ壬ŠŌÖŹČēĻĀ£ŗ
A£®¹ĢĢ¬Ź±Äܵ¼µē£¬ÄÜČÜÓŚŃĪĖį
B£®ÄÜČÜÓŚCS2£¬²»ČÜÓŚĖ®
C£®¹ĢĢ¬Ź±²»µ¼µē£¬ŅŗĢ¬Ź±Äܵ¼µē£¬æÉČÜÓŚĖ®
D£®¹ĢĢ¬”¢ŅŗĢ¬Ź±¾ł²»µ¼µē£¬ČŪµćĪŖ3500 ”ę
ŹŌĶʶĻĖüĆĒµÄ¾§ĢåĄąŠĶ£ŗA£®__£»B£®__£»C£®__£»D£®__”£
£Ø3£©ĻĀĶ¼ÖŠA”«DŹĒ֊ѧ»Æѧ½ĢæĘŹéÉĻ³£¼ūµÄ¼øÖÖ¾§Ģå½į¹¹Ä£ŠĶ£¬ĒėĢīŠ“ĻąÓ¦ĪļÖŹµÄĆū³Ę£ŗA£®__£»B£®__£»C£®__D£®____”£
£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. 32 g S8£Ø·Ö×Ó½į¹¹£ŗ![]() £©ÖŠµÄ¹²¼Ū¼üŹżÄæĪŖNA
£©ÖŠµÄ¹²¼Ū¼üŹżÄæĪŖNA
B. 2 gÓÉH218OŗĶ2H2O×é³ÉµÄĪļÖŹÖŠŗ¬ÓŠµÄÖŹ×ÓŹżĪŖNA
C. 8 g CuOÓė×ćĮæH2³ä·Ö·“Ӧɜ³ÉCu£¬øĆ·“Ó¦×ŖŅʵĵē×ÓŹżĪŖ0.2NA
D. ±ź×¼×“æöĻĀ£¬11.2 L Cl2ČÜÓŚĖ®£¬ČÜŅŗÖŠCl£”¢ClO£ŗĶHClOµÄĪ¢Į£ŹżÖ®ŗĶĪŖNA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖĒæĖįÓėĒæ¼īŌŚĻ”ČÜŅŗĄļ·“Ó¦µÄÖŠŗĶČČæɱķŹ¾ĪŖ£ŗH£«(aq)£«OH£(aq)=H2O(l) ¦¤H£½£57.3kJ”¤mol-1¶ŌĻĀĮŠ·“Ó¦£ŗ
CH3COOH(aq)£«NaOH(aq)=CH3COONa(aq)£«H2O(l) ¦¤H£½£Q1kJ”¤mol-1
![]() H2SO4(ÅØ)£«NaOH(aq)=
H2SO4(ÅØ)£«NaOH(aq)=![]() Na2SO4(aq)£«H2O(l) ¦¤H£½£Q2kJ”¤mol-1
Na2SO4(aq)£«H2O(l) ¦¤H£½£Q2kJ”¤mol-1
HNO3(aq)£«NaOH(aq)=NaNO3(aq)£«H2O(l) ¦¤H£½£Q3kJ”¤mol-1
ÉĻŹö·“Ó¦¾łŌŚČÜŅŗÖŠ½ųŠŠ£¬ŌņĻĀĮŠQ1”¢Q2”¢Q3µÄ¹ŲĻµÕżČ·µÄŹĒ£Ø £©
A.Q2>Q3>Q1B.Q2>Q1>Q3C.Q1£½Q2£½Q3D.Q2£½Q3>Q1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)Ė®µÄµēĄėĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£¬ČōAµć±ķŹ¾25 ”ꏱĖ®µÄµēĄė“ļĘ½ŗāŹ±µÄĄė×ÓÅØ¶Č£¬Bµć±ķŹ¾100 ”ꏱĖ®µÄµēĄė“ļĘ½ŗāŹ±µÄĄė×ÓÅØ¶Č”£Ōņ100 ”ꏱ1 mol”¤L£1µÄNaOHČÜŅŗÖŠ£¬ÓÉĖ®µēĄė³öµÄc(H£«)________mol”¤L£1£¬Kw(25 ”ę)________Kw(100 ”ę)(Ģī”°>”±”¢”°<”±»ņ”°£½”±)”£25 ”ꏱ£¬ĻņĖ®µÄµēĄėĘ½ŗāĢåĻµÖŠ¼ÓČėÉŁĮæNH4Cl¹ĢĢ壬¶ŌĖ®µÄµēĄėĘ½ŗāµÄÓ°ĻģŹĒ________(Ģī”°“Ł½ų”±”¢”°ŅÖÖĘ”±»ņ”°²»Ó°Ļģ”±)”£
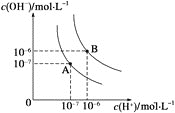
(2)µēĄėĘ½ŗā³£ŹżŹĒŗāĮæČõµē½āÖŹµēĄė³Ģ¶ČĒæČõµÄĮ攣ŅŃÖŖČē±ķŹż¾Ż”£
»ÆѧŹ½ | µēĄėĘ½ŗā³£Źż£Ø25”ę£© |
HCN | K=4.9”Į10-10 |
CH3COOH | K=1.8”Į10-5 |
H2CO3 | K1=4.3”Į10-7”¢K2=5.6”Į10-11 |
¢Ł25 ”ꏱ£¬ÓŠµČÅØ¶ČµÄNaCNČÜŅŗ”¢Na2CO3ČÜŅŗ”¢CH3COONaČÜŅŗ£¬ČżÖÖČÜŅŗµÄpHÓɓ󵽊”µÄĖ³ŠņĪŖ_____________________________”£
¢Ś25 ”ꏱ£¬µČÅØ¶ČµÄCH3COOHČÜŅŗŗĶNaOHČÜŅŗµČĢå»ż»ģŗĻ£¬ĖłµĆČÜŅŗĻŌ¼īŠŌ£¬Ōņc(Na£«)______c(CH3COO£)(Ģī”°>”±”¢”°<”±»ņ”°£½”±)”£
¢ŪĻņNaCNČÜŅŗÖŠĶØČėÉŁĮæCO2£¬Ėł·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒŹµŃéŹŅÖʱø“æ¾»ĀČĘųµÄŹµŃé×°ÖĆ£¬ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
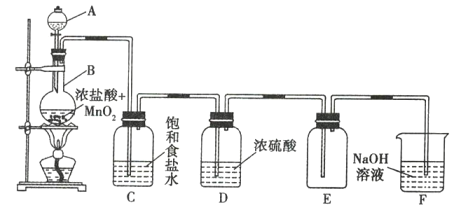
£Ø1£©Š“³öĻĀĮŠŅĒĘ÷µÄĆū³Ę£ŗA __________________ £¬B ________________ ”£
£Ø2£©Š“³öÖʱøĀČĘųµÄ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ __________________ ”£
£Ø3£©×°ÖĆCµÄ×÷ÓĆŹĒ __________________ £¬×°ÖĆDµÄ×÷ÓĆŹĒ __________________ ”£
£Ø4£©×°ÖĆFµÄ×÷ÓĆŹĒ __________________ £ØÓĆ»Æѧ·½³ĢŹ½±ķŹ¾£©”£
£Ø5£©ŹµŃé½įŹųŹ±£¬ŠčŅŖĻČ³·Č„BÓėCÖ®¼äµÄµ¼¹Ü£¬Č»ŗóŌŁ³·µō¾Ę¾«µĘ”£ČōĻČ³·µō¾Ę¾«µĘ£¬¶ų²»³·Č„BÓėCÖ®¼äµÄµ¼¹Ü£¬Ōņ»įµ¼ÖĀ __________________ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ”°“óĶ¬”±»ÆѧŠ”×éŌŚŹµŃéŹŅÖŠ¶Ō![]() ½ųŠŠĢ½¾æ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
½ųŠŠĢ½¾æ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)![]() ѧɜ¼×ÓĆĻĀĶ¼E×°ÖĆÖʱø
ѧɜ¼×ÓĆĻĀĶ¼E×°ÖĆÖʱø![]() ”£Ö÷·“Ó¦µÄ·¢Éś£¬±ķĆ÷ĮņĖį¾ßÓŠµÄŠŌÖŹÓŠ________
”£Ö÷·“Ó¦µÄ·¢Éś£¬±ķĆ÷ĮņĖį¾ßÓŠµÄŠŌÖŹÓŠ________

A.Ńõ»ÆŠŌ ![]() »¹ŌŠŌ
»¹ŌŠŌ ![]() ĖįŠŌ
ĖįŠŌ ![]() ¼īŠŌ
¼īŠŌ
![]() ѧɜŅŅŅŌ
ѧɜŅŅŅŌ![]() ·ŪĪ“ŗĶ
·ŪĪ“ŗĶ![]() ĪŖŌĮĻÖĘČ”
ĪŖŌĮĻÖĘČ”![]() £¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ£ŗ___
£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ£ŗ___
![]() ĻÖÓūŹÕ¼ÆŅ»ĘæøÉŌļµÄ
ĻÖÓūŹÕ¼ÆŅ»ĘæøÉŌļµÄ![]() £¬Ń”ÓĆĻĀĶ¼ÖŠµÄA”¢B”¢C”¢D×°ÖĆ£¬ĘäĮ¬½ÓĖ³Šņ
£¬Ń”ÓĆĻĀĶ¼ÖŠµÄA”¢B”¢C”¢D×°ÖĆ£¬ĘäĮ¬½ÓĖ³Šņ![]() °“ĘųĮ÷·½Ļņ£¬ÓĆŠ”Š“×ÖÄø±ķŹ¾£¬æÉÖŲø“Ń”ÓĆ
°“ĘųĮ÷·½Ļņ£¬ÓĆŠ”Š“×ÖÄø±ķŹ¾£¬æÉÖŲø“Ń”ÓĆ![]() ĪŖ£ŗ_________
ĪŖ£ŗ_________
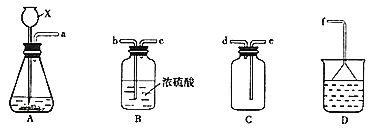
(2)ѧɜ±ūÓĆÅØ![]() ŗĶÕįĢĒ·“Ó¦£¬µĆµ½µÄĘųĢåÖŠŗ¬ÓŠ
ŗĶÕįĢĒ·“Ó¦£¬µĆµ½µÄĘųĢåÖŠŗ¬ÓŠ![]() ”¢
”¢![]() ”£ĻÖŃ”ŌńĻĀĶ¼ÖŠµÄ×°ÖĆ£¬ŃéÖ¤»ģŗĻĘųĢåÖŠ“ęŌŚ
”£ĻÖŃ”ŌńĻĀĶ¼ÖŠµÄ×°ÖĆ£¬ŃéÖ¤»ģŗĻĘųĢåÖŠ“ęŌŚ![]() ŗĶ
ŗĶ![]() ”£ĘäÖŠ£¬ÄÜÖ¤Ć÷“ęŌŚ
”£ĘäÖŠ£¬ÄÜÖ¤Ć÷“ęŌŚ![]() µÄĻÖĻóŹĒ_____”£
µÄĻÖĻóŹĒ_____”£
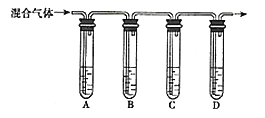
(3)ѧɜ¼×ŹµŃéÖŠ£¬“óŹŌ¹ÜÄŚ²śÉśĮĖ“óĮæŗŚÉ«¹ĢĢ唣²éŌÄ׏ĮĻÖŖ£ŗ
![]() ŗŚÉ«¹ĢĢåæÉÄÜŗ¬ÓŠCuO”¢CuS”¢
ŗŚÉ«¹ĢĢåæÉÄÜŗ¬ÓŠCuO”¢CuS”¢![]() ”£
ӣ
![]() ŗĶ
ŗĶ![]() ²»ČÜÓŚĻ”ŃĪĖį”¢Ļ”ĮņĖį£¬µ«¼ÓČČĻĀæÉČÜÓŚĻ”ĻõĖį”£
²»ČÜÓŚĻ”ŃĪĖį”¢Ļ”ĮņĖį£¬µ«¼ÓČČĻĀæÉČÜÓŚĻ”ĻõĖį”£
![]() Ļņŗ¬Ī¢Įæ
Ļņŗ¬Ī¢Įæ ![]() µÄČÜŅŗÖŠµĪ¼Ó
µÄČÜŅŗÖŠµĪ¼Ó![]() ČÜŅŗ£¬ÄܲśÉśŗģŗÖÉ«³Įµķ”£
ČÜŅŗ£¬ÄܲśÉśŗģŗÖÉ«³Įµķ”£
ĻÖȔɣĮæŗŚÉ«³Įµķ£¬¼ÓČėĻ”ĮņĖį£¬³ä·ÖÕńµ“ŅŌŗó£¬ŌŁµĪ¼Ó![]() ČÜŅŗ£¬Ī“¼ūŗģŗÖÉ«³Įµķ£¬ÓÉ“ĖĖłµĆ½įĀŪŹĒ_____________________”£ĮķȔɣĮæŗŚÉ«³Įµķ£¬¼ÓČė×ćĮæĻ”ĻõĖį²¢¼ÓČČ£¬·¢ĻÖŗŚÉ«¹ĢĢå×īÖÕĶźČ«Čܽā£¬ČÜŅŗ±äĪŖĄ¶É«£¬ÓŠĪŽÉ«ĘųÅŻÉś³É£¬¹ÜæŚ“¦³öĻÖŗģ×ŲÉ«”£ŹŌŠ“³öCuSČÜÓŚ×ćĮæĻ”ĻõĖįµÄĄė×Ó·½³ĢŹ½£ŗ__________ĪŖ²ā¶ØŗŚÉ«³ĮµķÖŠ
ČÜŅŗ£¬Ī“¼ūŗģŗÖÉ«³Įµķ£¬ÓÉ“ĖĖłµĆ½įĀŪŹĒ_____________________”£ĮķȔɣĮæŗŚÉ«³Įµķ£¬¼ÓČė×ćĮæĻ”ĻõĖį²¢¼ÓČČ£¬·¢ĻÖŗŚÉ«¹ĢĢå×īÖÕĶźČ«Čܽā£¬ČÜŅŗ±äĪŖĄ¶É«£¬ÓŠĪŽÉ«ĘųÅŻÉś³É£¬¹ÜæŚ“¦³öĻÖŗģ×ŲÉ«”£ŹŌŠ“³öCuSČÜÓŚ×ćĮæĻ”ĻõĖįµÄĄė×Ó·½³ĢŹ½£ŗ__________ĪŖ²ā¶ØŗŚÉ«³ĮµķÖŠ![]() µÄ°Ł·Öŗ¬Įæ£¬Č”
µÄ°Ł·Öŗ¬Įæ£¬Č”![]() ŗŚÉ«³Įµķ£¬ŌŚĖįŠŌČÜŅŗÖŠÓĆ
ŗŚÉ«³Įµķ£¬ŌŚĖįŠŌČÜŅŗÖŠÓĆ ![]() ČÜŅŗ“¦Ąķ£¬·¢Éś·“Ó¦ČēĻĀ£ŗ
ČÜŅŗ“¦Ąķ£¬·¢Éś·“Ó¦ČēĻĀ£ŗ![]()
![]() ,·“Ó¦ŗóÖó·ŠČÜŅŗ£¬øĻ¾”
,·“Ó¦ŗóÖó·ŠČÜŅŗ£¬øĻ¾”![]() £¬¹żĮæµÄøßĆĢĖį¼ŲČÜŅŗĒ”ŗĆÓė
£¬¹żĮæµÄøßĆĢĖį¼ŲČÜŅŗĒ”ŗĆÓė![]() ČÜŅŗĶźČ«·“Ó¦”£Ōņ»ģŗĻĪļÖŠ
ČÜŅŗĶźČ«·“Ó¦”£Ōņ»ģŗĻĪļÖŠ![]() µÄÖŹĮæ·ÖŹżĪŖ ___________
µÄÖŹĮæ·ÖŹżĪŖ ___________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĢõ¼žĻĀ£¬ŌŚŅ»øöĢå»żæɱäµÄĆܱÕČŻĘ÷ÖŠ³äČė2 molµÄĘųĢåAŗĶ1 molµÄĘųĢåB·¢Éś·“Ó¦£ŗ2A(g)£«B(g)![]() 3C(g)””¦¤H>0”£t1Ź±æĢ·“Ó¦“ļµ½Ę½ŗā£¬²¢²āµĆCŌŚČŻĘ÷ÖŠµÄĢå»ż·ÖŹżĪŖ¦Õ1”£t2Ź±æĢøıäijŅ»Ģõ¼ž(ĘäĖūĢõ¼ž²»±ä)£¬CŌŚČŻĘ÷ÖŠµÄĢå»ż·ÖŹżµÄ±ä»ÆČēĶ¼ĖłŹ¾£¬Ōņt2Ź±æĢøıäµÄĢõ¼žŹĒ(””””)
3C(g)””¦¤H>0”£t1Ź±æĢ·“Ó¦“ļµ½Ę½ŗā£¬²¢²āµĆCŌŚČŻĘ÷ÖŠµÄĢå»ż·ÖŹżĪŖ¦Õ1”£t2Ź±æĢøıäijŅ»Ģõ¼ž(ĘäĖūĢõ¼ž²»±ä)£¬CŌŚČŻĘ÷ÖŠµÄĢå»ż·ÖŹżµÄ±ä»ÆČēĶ¼ĖłŹ¾£¬Ōņt2Ź±æĢøıäµÄĢõ¼žŹĒ(””””)

A. ¼ÓČė1 molŗ¤Ęų
B. ¼ÓČė1 mol B
C. Ōö“óŃ¹Ēæ
D. ÉżøßĪĀ¶Č
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A.Ņ»¶ØĢõ¼žĻĀ£¬1molN2ŗĶ3molH2³ä·Ö·“Ó¦£¬Éś³ÉĪļÖŠµÄN-H¼üŹżÄæĪŖ6NA
B.ĶźČ«Č¼ÉÕ1.5molCH3CH2OHŗĶC2H4µÄ»ģŗĻĪļ£¬×ŖŅʵē×ÓŹżĪŖ18NA
C.100g 98%µÄÅØĮņĖįÖŠŗ¬ŃõŌ×ÓøöŹżĪŖ4NA
D.1L 0.1 mol/LµÄNa2SČÜŅŗÖŠS2£ŗĶHS£µÄ×ÜŹżĪŖ0.1NA
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com