
����Ŀ��A��B��C��D��E��X��Ϊ������Ԫ���γɵ����������ͼ��ʾת����ϵ������������ͷ�Ӧ������ȥ������ش��������⣺
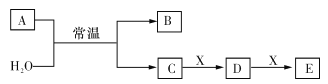
��1����A�Ƕ����ڷǽ���Ԫ��R�ĵ��ʣ�B����Ư�����ҹ����ֽ⣬CΪһԪǿ�ᡣ
��Ԫ��R��Ԫ�����ڱ��е�λ��Ϊ________________________����Ԫ��Q��Ԫ��R��������������ͬ��Q��ԭ�Ӱ뾶��С�������ߵļ��⻯��ķе���ߵ���_________������R������Q������ԭ����______________________________��
��д��ʵ�����Ʊ�����A�ķ�Ӧ�����ӷ���ʽ__________��
��X����Ϊ________������ĸ���ţ���
a��NaOH b��AlCl3 c��Na2CO3
��2����A�ǵ���ɫ���壬��д����CΪ�������Һ������ȼ�ϵ�صĸ����ĵ缫��Ӧ����ʽ____________________________________��
���𰸡� �������ڵ�VIIA�� Q HF���Ӽ������� MnO2+4H++2Cl-![]() Cl2��+Mn2++2H2O c H2-2e-+2OH-=2H2O
Cl2��+Mn2++2H2O c H2-2e-+2OH-=2H2O
����������1������������A�ǵ�����ˮ��Ӧ����C��CΪһԪǿ����B����Ư�����ҹ����ֽ⣬BΪ�����ᣬA����������Ϊ�������ڵ�VIIA�壻
Ԫ��Q��Ԫ��R��������������ͬ,��Q��ԭ�Ӱ뾶��С,����QΪ��Ԫ�أ�HF���Ӽ����������е�ߣ���Ϊ��Q�� HF���Ӽ���������
��ʵ�����Ʊ�����������������Ũ������ȷ�Ӧ�Ʊ���������ȷ�𰸣�MnO2+4H++2Cl-![]() Cl2��+Mn2++2H2O ��
Cl2��+Mn2++2H2O ��
��̼���������ᷴӦ����̼�����ƣ�̼�����������ᷴӦ�����Ȼ��ƣ�c ��ȷ�� ��ѡ c ��
��2��A�ǵ���ɫ����������ƣ���ˮ��Ӧ�����������ƺ�����������������������������Һ����ȼ�ϵ�أ�����������������������Ӧ�� H2-2e-+2OH-=2H2O����ΪH2-2e-+2OH-=2H2O��


 ��ѧ�̸̳����¿α�ϵ�д�
��ѧ�̸̳����¿α�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������β���ŷŵ�NOX��CO��Ⱦ������������β��ϵͳ�а�װ��ת����������Ч����NOX��CO���ŷš�
��֪����2CO(g)+O2(g)![]() 2CO2(g), ��H=-566.0kJ��mol-1
2CO2(g), ��H=-566.0kJ��mol-1
��N2(g)+O2(g)![]() 2NO(g)��H=+180.5 kJ��mol-1
2NO(g)��H=+180.5 kJ��mol-1
�ش��������⣺
��1��CO��ȼ����Ϊ___________����1molN2(g)��1molO2(g)�����л�ѧ������ʱ�ֱ���Ҫ����946kJ��498kJ����������1molNO(g)�����л�ѧ������ʱ�����յ�����Ϊ___________kJ��
��2��Ϊ��ģ�ⷴӦ2CO(g)+2NO(g)![]() 2CO2(g)+N2(g)�ڴ�ת�����ڵĹ������������һ���������÷�Ӧ�ں����ܱ������н��У��ô�������ò�ͬʱ��NO��CO��Ũ�������
2CO2(g)+N2(g)�ڴ�ת�����ڵĹ������������һ���������÷�Ӧ�ں����ܱ������н��У��ô�������ò�ͬʱ��NO��CO��Ũ�������
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/(10-4 kJ��mol-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
c(CO)/(10-3kJ��mol-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
��ǰ2s�ڵ�ƽ����Ӧ����v(N2)___________��
����˵��������Ӧ�ﵽƽ��״̬����___________��
A��2n(CO2)=n(N2) B����������ƽ����Է�����������
C�������ܶȲ��� D������������ѹǿ����
��3����ij���������з������з�Ӧ��2NO2(g)![]() 2NO(g)+O2(g)����һ������NO2��������ܱ������У������ƽ��ת�������¶ȱ仯��ͼ��ʾ��
2NO(g)+O2(g)����һ������NO2��������ܱ������У������ƽ��ת�������¶ȱ仯��ͼ��ʾ��

�÷�ӦΪ___________��Ӧ(��������������������)����֪ͼ��a���Ӧ�¶��£�NO2����ʼѹǿP0Ϊ120kPa��������¶��·�Ӧ��ƽ�ⳣ��Kp��ֵΪ___________��(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
��N2H4-O2ȼ�ϵ����һ�ָ�Ч����Ⱦ�����͵�أ���װ����ͼ��ʾ��
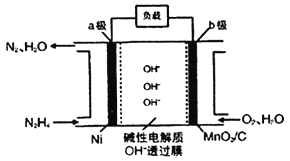
N2H4�ĵ���ʽΪ___________��a���ĵ缫��Ӧ����ʽΪ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ�������ֵ������˵����ȷ����
A. ��״����,2.24L���ȼ���������������ΪNA
B. 1molH2��1molI2(g)���ܱ������з�Ӧ�����ɵ�H-I����Ϊ2NA
C. �����£�0.1molFeͶ�뵽����Ũ�����з�Ӧ,ת�Ƶĵ�����Ϊ0.3NA
D. 8.8g������������ȩ(CH3CHO)�Ļ�����к��е�Cԭ����Ϊ0.4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���ijͬѧ���й����ʽ��еķ��ࣺ

(1)ÿ�������д������������ʷֱ���__________��__________��____________(�ѧʽ)��
(2)���������г����õ�����������������������ָ���ᡢ��������ᣬ��������ָ�ռ�ʹ��
�ٴ����ʵķ���Ƕȿ�����ǡ����һ��������__________________(�ѧʽ)��
��������������������֮����ɷ�Ӧ�����û�ѧ����ʽ��ʾ�������ռ�ʹ���ķ�Ӧ��______________________________��__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������κͽ��������ڹ�ũҵ�������й㷺��Ӧ�á�
(1)��֪��
��Ӧ��CaSO4(s)+CO(g)=CaO(s)+SO2(g)+CO2(g)��H1=+218.4 kJ��mol-1
��Ӧ��CaSO4(s)+4CO(g)=CaS(s)+4CO2(g) ��H2=-175.6kJ��mol-1
��Ӧ ��3CaSO4(s)+CaS(s)=4CaO(s)+4SO2(g) (B) ��H3
�١�H3=__________��
����ʹ��Ӧ�����ʼӿ�Ĵ�ʩ��____________________________________(д������)��
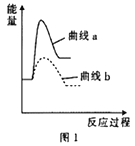
����֪ij�¶��·�Ӧ��ķ�Ӧ����С�ڷ�Ӧ��ķ�Ӧ����,��ͼ1������a��ʾ__________ (���Ӧ��Ӧ��)��
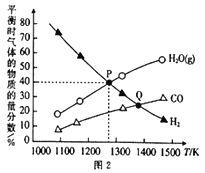
(2)��2L�ܱ������У�����0.1molMoS2(����)��0.2molNa2CO3��0.4molH2��������ӦMoS2(s)+2Na2CO3 (s)+4H2(g)![]() Mo(s)+2CO(g)+4H2O(g)+2Na2S(s),�ﵽƽ��ʱ������������ʵ����������¶ȱ仯���� ����ͼ2��ʾ��
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s),�ﵽƽ��ʱ������������ʵ����������¶ȱ仯���� ����ͼ2��ʾ��
�ٷ�Ӧ���ʣ�P��______ Q��(�<�� ��>����=��)�����ж�������_____________��
��������ѹ��P��__Q��(�<�� ��>����=��)�����ж�������_____________��
��P���Ӧ�¶��£�H2��ƽ��ת����Ϊ__________��ƽ�ⳣ��K=__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���G��һ�ֳ��õ�ֲ���ζ�ͣ���ҵ�Ͽɰ�����·�ߺϳɡ�
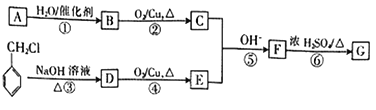
��֪��
���л���A�Ƿ����е�����˫����Ŀ֮��Ϊ4��1��ϩ����
��G�ķ���ʽΪC9H8O���ܷ���������Ӧ��
��CH3CHO+CH3CHO![]()
![]() ��
��
�ش��������⣺
(1)B������Ϊ__________��F�к��еĹ����ŵ�������__________��
(2)E�Ľṹ��ʽΪ__________��G�Ľṹ��ʽΪ________________��
(3)�ݵķ�Ӧ����Ϊ__________���ķ�Ӧ����Ϊ__________��
(4)���ɢ۵Ļ�ѧ����ʽΪ_____________________________��
(5)��Ӧ�١����з���ԭ�Ӿ�����(ԭ��������Ϊ100%)����__________ (�����)��
(6)ͬʱ��������������F��ͬ���칹����__________�֣����к˴Ź���������ʾ�������,�ҷ����֮��Ϊ3��3��2��2����__________ (��ṹ��ʽ)��
a�������Ϻ�������ȡ���� b�������к���-COO-�ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���ӦX2��g��+H2��g��![]() 2HX��g����ƽ�ⳣ��Ϊ100������1.0mol��HX��g��ͨ�����Ϊ1.0L���ܱ������У��ڸ��¶�ʱHX��g�������ֽ��ʽӽ��ڣ� ��
2HX��g����ƽ�ⳣ��Ϊ100������1.0mol��HX��g��ͨ�����Ϊ1.0L���ܱ������У��ڸ��¶�ʱHX��g�������ֽ��ʽӽ��ڣ� ��
A. 5% B. 17% C. 25% D. 33%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ������N��P��As���ַǽ���Ԫ�أ���ش�����������⡣
(1)��̬��ԭ�ӵļ۵����Ų�ʽΪ_________________��ͬ����Ԫ��ԭ�������京����ͬ��Ŀδ�ɶԵ��ӵ���___________________(��Ԫ�ط���)��
(2)�ۻ�(As4S4)�Ǻܶ�����Ϥ��һ�����ʣ�����ӽṹ��ͼ��ʾ������������ԭ���������ﵽ8���ӽṹ�������к��еĦҼ�����Ŀ��__________________�����ʾ��ԭ����______________����ԭ�ӵ��ӻ���ʽ��____________________��
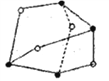
(3)����ķе�ϵͣ�������ĽǶ��ƶ�����ܵ�ԭ����_______________________��������Ŀռ乹����_____________________��
(4)����(P4)�����з��Ӷѻ���ʽ���ڷ����ܶѻ���ÿ��������Χ���ڵķ�����_________�����������徧�����ⳤΪypm������٤����������ֵ��NA��ʾ�����������ܶ�Ϊ____________g��cm-3��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com