
【题目】碳、氮广泛分布在自然界中,碳、氮的化合物性能优良,在工业生产和科技领域有重要用途。
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700oC的氮气流中反应制得:3SiO2(s) + 6C(s) + 2N2(g)![]() Si3N4(s) + 6CO(g) ΔH=-1591.2 kJ/mol则该反应每转移1mol e-,可放出的热量为________
Si3N4(s) + 6CO(g) ΔH=-1591.2 kJ/mol则该反应每转移1mol e-,可放出的热量为________
(2)高温时,用CO还原MgSO4可制备高纯MgO
①750℃时,测得气体中含等物质的量的SO2和SO3,此时反应的化学方程式是:____________
②由MgO制成的Mg可构成“镁—次氯酸盐”电池,其装置示意图如图,该电池的正极反应式为____________

(3)某研究小组将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g) + H2O(g)![]() CO2(g) + H2(g),得到如下数据:
CO2(g) + H2(g),得到如下数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
CO | H2O | CO | H2 | |||
1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
2 | 900 | 1 | 2 | 0.5 | 0.5 | — |
①实验Ⅰ中,前5min的反应速率v(CO2)=___________
②下列能判断实验Ⅱ已经达到平衡状态的是(填写选项序号)__________
a.容器内CO、H2O、CO2、H2的浓度不再变化
b.容器内压强不再变化
c.混合气体的密度保持不变
d.v正(CO)=v逆(CO2)
e.容器中气体的平均相对分子质量不随时间而变化
③若实验Ⅲ的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如下图所示,b点v正_______v逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是______________________

【答案】132.6kJ 2MgSO4 + CO ![]() 2MgO + SO2 + CO2 + SO3 ClO- + 2e- + H2O = Cl- + 2OH- 0.15 mol/(L·min) a d > 该反应达到平衡后,因反应为放热反应且反应容器为绝热容器,故容器内温度升高,反应逆向进行
2MgO + SO2 + CO2 + SO3 ClO- + 2e- + H2O = Cl- + 2OH- 0.15 mol/(L·min) a d > 该反应达到平衡后,因反应为放热反应且反应容器为绝热容器,故容器内温度升高,反应逆向进行
【解析】
根据题目信息写出生成物,根据质量守恒配平;由图可知镁-次氯酸盐”燃料电池中Mg与ClO-、H2O反应生成Cl-与Mg(OH)2;根据勒夏特列原理分析平衡的移动方向。
(1)根据方程式3SiO2(s)+6C(s)+2N2(g)Si3N4(s)+6CO(g)△H=-1591.2kJ/mol,由碳元素化合价变化情况可知每转移12mol电子,放出1591.2kJ热量,所以每转移1mole-,可放出的热量为132.6kJ,故答案为:132.6kJ;
(2)①用CO还原MgSO4可得到MgO、CO2、SO2和SO3,方程式为2MgSO4 + CO ![]() 2MgO + SO2 + CO2 + SO3,故答案为:2MgSO4 + CO
2MgO + SO2 + CO2 + SO3,故答案为:2MgSO4 + CO ![]() 2MgO + SO2 + CO2 + SO3;
2MgO + SO2 + CO2 + SO3;
②由图可知镁-次氯酸盐”燃料电池中Mg与ClO-、H2O反应生成Cl-与Mg(OH)2,该电池反应的总反应方程式为Mg+ClO-+H2O=Cl-+Mg(OH)2,正极电极反应是ClO-离子得到电子发生还原反应,电极反应为:ClO-+2e-+H2O=Cl-+2OH-,故答案为:ClO-+2e-+H2O=Cl-+2OH-;
(3) ① v(CO 2 ) = v(H 2 ) = 1.5mol÷2L÷ 5min=0.15mol · L -1 · min -1;
②a.容器内CO、H2O、CO2、H2的浓度不再变化,说明反应处于平衡状态,故a正确;
b.恒温、恒容条件下,气体的总物质的量始终不变,压强始终不变,故b错误;
c.恒容条件下,反应物和产物都是气体,密度始终不变,故c错误;
d.v正(CO)=υ逆(CO2),转化成CO2的正、逆反应速率相等,故d正确;
e.该反应气体的物质的量不变,气体的质量也不变,所以反应过程中气体的平均相对分子质量不变,故e错误,故选a、d。
③c点到达平衡,而b点未达到平衡,正反应速率减小,逆反应速率增大至相等,故b点v正>v逆;,因反应为放热反应且反应容器为绝热容器,故容器内温度升高,反应逆向进行使H2O(g)的转化率降低,故答案为:>;该反应达到平衡后,因反应为放热反应且反应容器为绝热容器,故容器内温度升高,反应逆向进行。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. ![]() 的一溴代物和
的一溴代物和![]() 的一溴代物都有4种(不考虑立体异构)
的一溴代物都有4种(不考虑立体异构)
B. CH3CH=CHCH3分子中的四个碳原子在同一直线上
C. 按系统命名法,化合物 的名称是2,3,4-三甲基-2-乙基戊烷
的名称是2,3,4-三甲基-2-乙基戊烷
D. ![]() 与
与![]() 都是α-氨基酸且互为同系物
都是α-氨基酸且互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X可用于合成Y.下列有关X、Y的说法正确的是( )
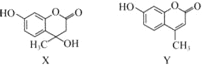
A. X分子中所有原子可能在同一平面上
B. X在一定条件下可以发生消去反应
C. Y与足量H2的加成产物中不含手性碳原子
D. X、Y与足量浓溴水反应的类型完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铅(PbO)是黄色固体。实验室用草酸在浓硫酸作用下分解制备CO,其原理为H2C2O4![]() CO↑+CO2↑+H2O。某学习小组设计实验探究CO还原氧化铅并检验氧化产物的装置如图所示(已知CO通入银氨溶液产生黑色银粒)。下列说法正确的是
CO↑+CO2↑+H2O。某学习小组设计实验探究CO还原氧化铅并检验氧化产物的装置如图所示(已知CO通入银氨溶液产生黑色银粒)。下列说法正确的是

A. 装置②③⑤⑥中的试剂依次为氢氧化钠溶液、碱石灰、银氨溶液、澄清石灰水
B. 实验时,先点燃①处酒精灯,等装置⑥中有明显现象且有连续气泡后再点燃④处酒精灯
C. 实验完毕时,先熄灭①处酒精灯,再熄灭④处酒精灯
D. 尾气处理装置可选用盛NaOH溶液的洗气瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行的反应:N2 + 3H22NH3,下列说法正确的是
A. 降低温度能加快逆反应速率
B. 保持体积不变充入N2,能加快反应速率
C. 达到平衡时,反应速率:v(正) =v(逆)=0
D. 达到平衡时,N2和H2的转化率可能达到100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1.5NA个H3PO4的摩尔质量为____,含氧原子的物质的量为____。
(2)a mol H2SO4中含有b个氧原子,则阿伏加德罗常数可以表示为_____。
(3)25.2g Na2RO3含Na+0.4mol,则Na2RO3的摩尔质量为___,R的相对原子质量为__。含R的质量为1.6g的Na2RO3,其物质的量为___。
(4)相同条件下,比较下列物质中氢原子数目多少(填“>”“<”或“=”):
①4.9g H2SO4____3.6g H2O ②1.6L CH4___2.4L H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒液流电池充电时间短,续航能力强,其充放电原理为VO2++V3++H2O![]() VO2++V2++2H+。以此电池为电源,用石墨电极电解Na2SO3溶液,可得到NaOH和H2SO4示意图如下。下列说法错误的是
VO2++V2++2H+。以此电池为电源,用石墨电极电解Na2SO3溶液,可得到NaOH和H2SO4示意图如下。下列说法错误的是

A. 全钒液流电池放电时,正极的电极反应式为VO2++2H++e-=VO2++H2O
B. 图中a电极为阴极,N物质是H2
C. 全钒液流电池充电时,V3+被氧化为VO2+
D. 电解时,b电极的反应式为SO32-+H2O-2e-=SO42-+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有BaCl2 和AlCl3的混合溶液aL,将它平均分成两份。一份滴加稀硫酸,使钡离子完全沉淀,另一份滴加AgNO3溶液,使氯离子完全沉淀。反应中消耗x mol H2SO4,y mol AgNO3溶液。据此得知原混合溶液中的铝离子浓度为( ) mol/L。
A. (y-2x)/a B. (y-x)/a C. 2(y-2x)/3a D. (y-2x)/3a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将2 mol SO2和1 mol O2置于容积为10 L的密闭容器中发生反应2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g) ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )

A. 由图甲推断,A点对应温度下该反应的平衡常数为800
B. 由图甲推断,B点O2的平衡浓度为0.15 mol·L-1
C. 达平衡后,若增大容器容积,则反应速率变化图像可以用图乙表示
D. 压强为0.50 MPa时,不同温度下SO2的转化率与温度的关系如图丙所示,则T2>T1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com