

| n |
| V |
| ||
| ||
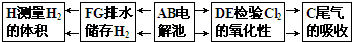 ����������˳���ǣ�H��F��G��A��B��D��E��C��
����������˳���ǣ�H��F��G��A��B��D��E��C��
| ||
| ||
| 1 |
| 5.0��10-3mol |
| 50��10-3L |
| 10-14 |
| 0.1 |


 ��ʱѵ���������������ϵ�д�
��ʱѵ���������������ϵ�д� �ƸԾ���Ȥζ����ϵ�д�
�ƸԾ���Ȥζ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ | B������ |
| C��С�� | D����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ʯ������Ca��OH��2�ĵ��룺Ca��OH��2��s��?Ca2++2OH- | ||||
| B����AgC1����Һ�еμ�Na2S��Һ������ɫ������2AgC1��s��+S2-=Ag2S��s��+2C1- | ||||
| C����NaHCO3��Һ�м��������ʯ��ˮ������ɫ������HCO3-+Ca2++OH-=CaCO3��+H2O | ||||
D��Fe��OH��3������Ʊ���FeCl3+3H2O
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ǿ�������Һ�ĵ�����һ�������������Һ�ĵ�����ǿ |
| B��������Һ�д������ֹ��ۻ�������� |
| C����FeCl3��Һ�������ɣ��ɵõ�FeCl3���� |
| D��0.10 mol/L Al2��SO4��3��Һ��Al3+��С��0.2NA ��NA���������ӵ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һc��A��B������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һc��A��B������缫�壬ͨ��������ֱ����Դ��������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | ��ѡ�� | ��ͬ����ѡ�� | ��ѡ���� |
| ��1�� | A��CO B��CO2 C��SO2 D��P2O5 | ||
| ��2�� | A��ʳ��ˮ B�����ǵĺ�ˮ C������Ʈ���Ŀ��� D��������̼���� |
||
| ��3�� | A��CaO B��SO2 C��Na2O D��CuO | ||
��4�� |
A��H2SO4B��H2CO3 C��NaH2PO4 D��HNO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 A��B��C���������������ص����ֳ��������ÿ����������Ԫ����������������֣����ǵ��ʣ�����֮������ͼ��ʾ��ת����ϵ��
A��B��C���������������ص����ֳ��������ÿ����������Ԫ����������������֣����ǵ��ʣ�����֮������ͼ��ʾ��ת����ϵ��| ��ȼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �ס������ص缫���϶���������̼���������о�Ϊ����NaCl��Һ����ش��������⣺
�ס������ص缫���϶���������̼���������о�Ϊ����NaCl��Һ����ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com