
 .
. .
. .
. 、
、 .
.
分析 C发生氧化反应生成兔耳草醛,根据兔耳草醛结构简式知,C结构简式为 ;根据题给信息知,枯茗醛和X发生加成反应生成A,A发生消去反应生成B,B发生加成反应生成C,从A到兔耳草醛其碳原子个数不变,则X为CH3CH2CHO,A为
;根据题给信息知,枯茗醛和X发生加成反应生成A,A发生消去反应生成B,B发生加成反应生成C,从A到兔耳草醛其碳原子个数不变,则X为CH3CH2CHO,A为 ,A→B发生醇的消去反应,生成B为
,A→B发生醇的消去反应,生成B为 ,B→C发生加成反应;
,B→C发生加成反应;
最新研究的兔耳草醛的合成路线中,苯与丙烯发生加成反应生成D,D为 ,D→兔耳草醛发生加成反应,以此解答该题.
,D→兔耳草醛发生加成反应,以此解答该题.
解答 解:(1)通过以上分析知,X结构简式为CH3CH2CHO,故答案为:CH3CH2CHO;
(2)由上述分析可知,B为 ,故答案为:
,故答案为: ;
;
(3)在Cu作催化剂、加热条件下,C发生氧化反应生成兔耳草醛,反应方程式为 ,
,
故答案为: ;
;
(4)通过以上分析知,D为 ,故答案为:
,故答案为: ;
;
(5)芳香族化合物Y与枯茗醛互为同分异构体,Y具有如下特征:
a.不能发生银镜反应,可发生消去反应,说明不含醛基但含有羟基;b.
核磁共振氢谱显示:Y消去反应产物的环上只存在一种化学环境的氢原子,说明Y发生消去反应产物的环上只有一种类型氢原子,Y可能的结构简式为 或
或 ,
,
故答案为: 、
、 .
.
点评 本题考查有机物推断,为高考高频点,根据反应条件、部分有机物结构简式结合题给信息进行推断即可,侧重考查学生分析推断及知识迁移能力,明确醛之间发生加成反应时断键和成键方式,难点是同分异构体种类判断,题目难度中等.


科目:高中化学 来源: 题型:解答题
 原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A 原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的 原子序数为29.
原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A 原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的 原子序数为29.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 | |
| B. | 已知时25℃时Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe(OH)3+3H+?Fe3++3H2O的平衡常数K=4.0×104 | |
| C. | 将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]大于Ksp(CaSO4) | |
| D. | 已知25℃时,Ksp[Mg(OH)2]=1.8×10-11,在MgCl2溶液中加入氨水调混合液的pH=11,产生沉淀,则此时溶液中的c (Mg2+)=1.8×10-5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
 实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数ω(Na2CO3),称取此混合物mg,溶于水中,配成溶液.
实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数ω(Na2CO3),称取此混合物mg,溶于水中,配成溶液.查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 .
. .
.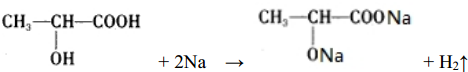 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Mg2+ | 8.1 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 以上R、R′、R″代表烃、烷基或芳基等)
以上R、R′、R″代表烃、烷基或芳基等)
 ,则与F具有相同官能团的同分异构体共5种(考虑顺反异构,不包含F).
,则与F具有相同官能团的同分异构体共5种(考虑顺反异构,不包含F). ,反应类型为消去反应.
,反应类型为消去反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A的单质的熔点最高 | B. | B元素的非金属性最强 | ||
| C. | C的简单离子半径最小 | D. | D的原子半径最大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com