
| A. | 用FeSO4除去酸性废水中的Cr2O72-:Cr2O72-+6 Fe2++14H+═2Cr3++6 Fe3++7H2O | |
| B. | NH4Al(SO4)2溶液中加入少量的氢氧化钠溶液:Al3++3OH-═Al(OH)3↓ | |
| C. | 用惰性电极电解MgCl2溶液2H2O+2Cl-$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 用CaSO4治理盐碱地:CaSO4(s)+Na2CO3(aq)?CaCO3(s)+Na2SO4(aq) |
分析 A.二价铁离子具有还原性,能够被Cr2O72-氧化;
B.氢氧化钠少量,先于铝离子反应;
C.反应生成氢氧化镁为沉淀,应保留化学式;
D.碳酸钙溶解度小于硫酸钙,依据沉淀转化规律解答.
解答 解:A.二价铁离子具有还原性,能够被Cr2O72-氧化,二者反应离子方程式:Cr2O72-+6 Fe2++14H+═2Cr3++6 Fe3++7H2O,故A正确;
B.NH4Al(SO4)2溶液中加入少量的氢氧化钠溶液,离子方程式:Al3++3OH-═Al(OH)3↓,故B正确;
C.用惰性电极电解MgCl2溶液,离子方程式:Mg2++2H2O+2Cl-$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+Mg(OH)2↓,故C错误;
D.碳酸钙溶解度小于硫酸钙,所以用CaSO4治理盐碱地,可以实现硫酸钙与碳酸钙的转化,离子方程式:CaSO4(s)+Na2CO3(aq)?CaCO3(s)+Na2SO4(aq),故D正确;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意沉淀转化规则,题目难度不大.


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | NaHCO3═Na++H++CO32- | B. | NaHSO4═Na++H++SO42- | ||
| C. | Fe(OH)3?Fe3++3OH- | D. | Ba(OH)2═Ba2++2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-b KJ/mol | |
| B. | C2H2(g)+$\frac{5}{2}$ O2(g)═2CO2(g)+H2O(l)△H=+2b KJ/mol | |
| C. | 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-4b KJ/mol | |
| D. | C2H2(g)+O2(g)═CO2(g)+H2O(l)△H=+b KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋中的醋酸和大理石发生了离子反应 | |
| B. | 醋中的醋酸使大理石氧化 | |
| C. | 醋中的醋酸使大理石还原 | |
| D. | 醋中的水使大理石溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L氢气中含有2NA个中子 | |
| B. | 0.1NA个氯化氢分子占有体积为2.24L | |
| C. | 2克金属钙变成钙离子时失去的电子数为0.1NA | |
| D. | 50mL0.1mol/L H2SO4溶液中含有H+数为0.005NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作和现象 | 结论 |
| A | 向氢氧化镁的饱和溶液中滴加FeCl3溶液,出现红褐色沉淀 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| B | 等浓度的Na2CO3和Na2SO3溶液的pH,前者>后者 | 非金属性S>C |
| C | 金属镁片和铝片用灵敏电流计相连,伸入烧碱溶液中,发现镁片上有气泡 | 金属性Mg<A1 |
| D | 冰醋酸中加入水,氢离子浓度先增大,后减小 | 醋酸的电离程度先增大后减小 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molFeSO4•7H2O的质量为278g/mol | |
| B. | FeSO4•7H2O的摩尔质量为278g | |
| C. | 配制100mL 0.1mol/L FeSO4溶液需要FeSO4•7H2O 2.78g | |
| D. | 配制100mL 0.1mol/L FeSO4溶液需要FeSO4•7H2O 1.52g |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2F2+2H2O═4HF+O2 | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | CaO+H2O═Ca(OH)2 | D. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
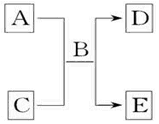 A、B、C、D和E均为中学化学常见的纯净物,其中B为自然界中含量最多的液体,它们之间有如图反应关系:
A、B、C、D和E均为中学化学常见的纯净物,其中B为自然界中含量最多的液体,它们之间有如图反应关系:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com