

分析 (1)氯气与水反应生成盐酸和次氯酸,结合溶液中物质的电离分析;氯水中的次氯酸不稳定易分解为盐酸和氧气;
(2)氯气有毒,直接排放能引起空气污染,可以和强碱反应,用碱液吸收;
(3)增大压强可以增大氯气的溶解度;一次加入太多的盐酸会使得产生的氯气的量多,出现很大的压强;
(4)根据大气压强原理来寻找排出液体的方法.
解答 解:(1)氯气与水反应生成盐酸和次氯酸,盐酸电离出氯离子和氢离子,次氯酸部分电离,水部分电离,所以氯水中含有七种粒子,其中的分子为Cl2、H2O、HClO;氯水中的次氯酸不稳定易分解为盐酸和氧气,2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,所以氯水久置会因为次氯酸分解而失效,
故答案为:Cl2、H2O、HClO;2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑;
(2)氯气有毒,多余的氯气不排放到空气中去,氯气可以和强碱氢氧化钠反应来吸收氯气,其反应的离子方程式为:Cl2+2OH-=ClO-+Cl-+H2O;
故答案为:NaOH溶液;Cl2+2OH-=ClO-+Cl-+H2O;
(3)图乙装置能在较短时间内得到饱和氯水,除了在摇动过程中增大了气体和水的接触面以外,另一个重要原因是氯气在瓶内产生较大的压强,增大了氯气的溶解度,分液漏斗中的盐酸应分数次加入试管内,若一次加入太多的盐酸,和高锰酸钾反应产生的氯气量太多,会导致瓶内压强过大会使瓶A的橡皮塞弹开,
故答案为:氯气在瓶内产生较大的压强,增大了氯气的溶解度;在瓶内产生过多的氯气,瓶内压强过大会使瓶A的橡皮塞弹开;
(4)配制氯水完成后,不必拆卸装置即可从瓶A中取用少量氯水,打开活塞2,关闭活塞1,用鼓气球向瓶A中鼓入空气,瓶内压强增大,会将液体从A瓶中排出,
故答案为:打开活塞2,关闭活塞1,用鼓气球向瓶A中鼓入空气.
点评 本题以氯及其化合物的性质考查氧化还原反应及物质的制备实验,把握习题中的信息及知识迁移应用为解答的关键,侧重学生综合应用能力及信息抽取和分析能力的考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Mg2+、H+、Cl-、OH- | B. | Na+、Ba2+、SO42-、NO3- | ||
| C. | Na+、H+、Cl-、CO32- | D. | K+、Cu2+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2molSO2(g)和1mol O2(g)所具有的键能总和大于2 molSO3(g)所具有的键能总和 | |
| B. | 将2molSO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出QKJ的热量 | |
| C. | 升高温度,平衡向逆反应移动,上述热化学方程式中的Q值减小 | |
| D. | 如将一定量SO2(g)和O2(g)于某密闭容器中充分反应后放热QKJ,则此过程中有2molSO2(g)被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分子中最多有12个碳原子处于同一平面上 | |
| B. | 分子中至少有9个碳原子处于同一平面上 | |
| C. | 该烃的一氯取代物最多有4种 | |
| D. | 该烃是苯的同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X>Y>Z>Q>W | |
| B. | 最高价氧化物对应的水化物的酸性:Z<Q | |
| C. | Q和W可形成原子个数比为1:1和1:2的化合物 | |
| D. | X、Y和W三种元素形成的化合物的水溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 为了分别研究SO2和Cl2的性质,设计了如图1所示的实验装置.
为了分别研究SO2和Cl2的性质,设计了如图1所示的实验装置.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ①盐泥a除泥沙外,还含有的物质是Mg(OH)2.
①盐泥a除泥沙外,还含有的物质是Mg(OH)2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
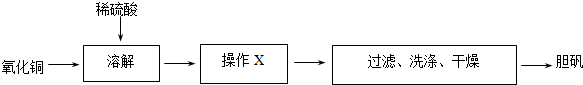
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
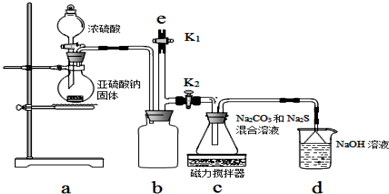
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com