
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,电离破坏化学键,而汽化只破坏分子间作用力,化学变化中一定有化学键的断裂和生成,以此来解答.
解答 解:①干冰汽化,只破坏分子间作用力;
②氯化氢气体溶于水,HCl发生电离,只破坏共价键;
③熔化NaCl固体,NaCl发生电离,只破坏离子键;
④NaOH固体溶于水,NaOH发生电离,只破坏离子键;
⑤H2O2分解发生化学变化生成氢气、氧气,共价键被破坏;
⑥Na2O2溶于水发生化学变化生成NaOH、氧气,破坏离子键和共价键;
⑦Na2O溶于水发生化学变化生成NaOH,离子键和共价键被破坏;
⑧氯化铵固体加热分解生成氨气、HCl,破坏离子键和共价键,
(1)仅离子键破坏的是③④,故答案为:③④;
(2)仅共价键破坏的②⑤,故答案为:②⑤;
(3)离子键和共价键同时破坏的是⑥⑦⑧,故答案为:⑥⑦⑧;
(4)未破坏化学键的是①,故答案为:①.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,注意电离、化学变化中化学键的变化,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H+十SO42-═BaSO4↓+H2O | |
| B. | 将稀硝酸滴加到氯化银固体上:AgCl+H+═Ag++HCl | |
| C. | 向碳酸氢铵溶液中加过量石灰水并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3•H2O | |
| D. | 用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
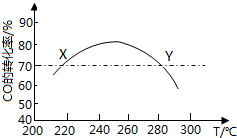 工业上,利用CO和H2合成二甲醚:3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)在合适的温度下,研究者进行了多次实验,每次实验保持原料气组成(3molCO、3molH2)、体积(10L)、反应时间等因素不变,实验结果如图所示.下列说法正确的是( )
工业上,利用CO和H2合成二甲醚:3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)在合适的温度下,研究者进行了多次实验,每次实验保持原料气组成(3molCO、3molH2)、体积(10L)、反应时间等因素不变,实验结果如图所示.下列说法正确的是( )| A. | X、Y两点对应的CO正反应速率相等 | |
| B. | 合成二甲醚的正反应△H>0 | |
| C. | 反应温度应控制在240℃~260℃之间 | |
| D. | 选择合适催化剂,可以提高CO转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
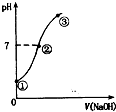 常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )
常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )| A. | ①点所示溶液中只存在HCl0的电离平衡 | |
| B. | ②到③的过程中水的电离程度一定减少 | |
| C. | ②点处表示氯气与氢氧化钠溶液恰好反应完全 | |
| D. | ②点所示溶液中:c( Na+)=c(HCl0)+2c(ClO -) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu和Cu2O的物质的量之比为2:1 | |
| B. | 产生的NO在标准状况下的体积为4.48L | |
| C. | 硝酸的物质的量浓度为2.6mol•L-1 | |
| D. | Cu和Cu2O与硝酸反应后剩余HNO3为0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
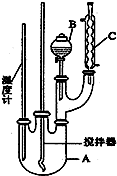
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH的电离程度变大 | B. | c(CH3COO-)增大 | ||
| C. | CH3COOH的Ka不变 | D. | 溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
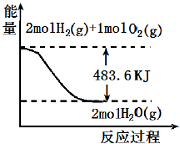
| A. | 表示 2molH2 (g)完全燃烧生成水蒸气吸收241.8 kJ热量 | |
| B. | 表示的热化学方程式为:H2(g)+$\frac{1}{2}$02(g)═H20(g)△H=-241.8 kJ/mol | |
| C. | 表示2mol H2(g)所具有的能量一定比2 mol气态水所具有的能量多483.6 kJ | |
| D. | H20(g)的能量低于H2(g)和O2(g)的能量之和 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com