
工业上用铝土矿(主要成分为Al2O3,含SiO2、Fe2O3等杂质)为原料冶炼铝的工艺流程如下,对下述流程中的判断正确的是:
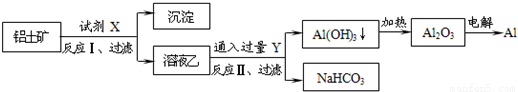
A.试剂X为稀硫酸,沉淀中含有硅的化合物
B.反应II中生成Al(OH)3的反应为:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-
C.结合质子(H+)的能力由弱到强的顺序是OH->CO32->AlO2-
D.Al2O3熔点很高,工业上还可采用电解熔融AlCl3冶炼Al
B
【解析】Al2O3、Fe2O3和硫酸反应,SiO2和硫酸不反应,要将氧化铝和其他两种分离出来,应该选择氢氧化钠,将氧化铝溶解为偏铝酸钠,则固体难溶物是氧化铁和二氧化硅,即试剂X为氢氧化钠,沉淀中含有二氧化硅和氧化铁,故A错误;
B、铝土矿(主要成分为Al2O3,含SiO2、Fe2O3等杂质)中加入过量的氢氧化钠以后会生成偏铝酸钠溶液,偏铝酸盐中通二氧化碳来获得氢氧化铝沉淀,即CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-,故B正确;
C、结合质子的能力就是指碱性,结合质子能力越强,相应的酸放出质子的能力就越弱,其对应的酸的酸性就越弱,显然酸性强弱HCO3->Al(OH)3>H2O,碱性:OH->AlO2->CO32-,所以结合质子能力:OH->AlO2->CO32-,故C错;
D、氯化铝是共价化合物,熔融时不存在铝离子,电解熔融的氯化铝不能获得金属铝,故D错误。


科目:高中化学 来源:2014高考名师推荐化学氧化还原概念(解析版) 题型:选择题
火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2→Cu2S+2FeS+SO2下列说法正确的是
A.SO2只是氧化产物
B.CuFeS2仅作还原剂,硫元素被氧化
C.每生成1 molCu2S,有4mol硫被氧化
D.每转移1.2 mol电子,有0.2 mol硫被氧化
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学有机推断(解析版) 题型:填空题
下列是利用烃C3H6合成有机高分子E和烃C6H14的流程图。请回答以下问题:
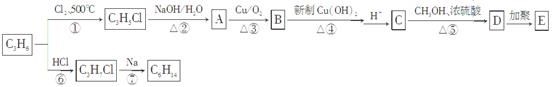 (1)①~⑥中属于取代反应的有 。
(1)①~⑥中属于取代反应的有 。
(2)C6H14的核磁共振氢谱只有两种峰,则C6H14的结构简式为 ;写出E的结构简式: 。
(3)写出B与新Cu(OH)2反应的化学方程式: 。
(4)D的同分异构体很多,符合下列条件的同分异构体有 种,其中氢原子核磁共振氢谱谱峰最少的结构简式为 。
①含碳碳双键 ②能水解 ③能发生银镜反应
(5)根据你所学知识和上图中相关信息,以乙醇为主要原料通过三步可能合成环己烷(无机试剂任选),写出第一步和第三步化学反应的化学方程式(有机物质写结构简式): 、 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学无机物性质及应用(非金属)(解析版) 题型:选择题
下列叙述错误的是
A.Al2(SO4)3可除去酸性废水中的悬浮颗粒
B.氯气与石灰乳反应能得到含氯漂白剂
C.燃煤时加入适量石灰石,可减少废气中SO2的排放
D.工业上硝酸可用于制化肥、农药、炸药和染料等
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学无机物性质及应用(金属)(解析版) 题型:选择题
下列方法不能用于鉴别Na2CO3和NaHCO3固体的是
A.分别加热两种固体,将放出的气体通入澄清石灰水
B.分别取两种固体溶于水,滴加Ba(OH)2溶液,观察是否生成沉淀
C.分别取两种固体各1 g,滴入几滴水振荡,用手触摸试管底部
D.分别取等质量的固体与足量稀盐酸充分反应,加热、蒸干、灼烧称重
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学探究组成、性质的实验方案的设计与评价(解析版) 题型:选择题
下列实验方案不能达到实验目的的是
| 实验目的 | 实验方案 |
A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液 |
B | 证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2 mL 1mol/L NaOH溶液中先加入3滴1 mol/L MgCl2溶液,再加入3滴1 mol/L FeCl3溶液 |
C | 检验蔗糖的水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,然后加入适量稀NaOH溶液,再向其中加入新制的银氨溶液,并水浴加热 |
D | 测定铝箔中氧化铝的含量 | 取a g铝箔与足量稀盐酸充分反应,逸出的气体通过碱石灰后,测其体积为b L(已转化为标准状况下) |
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学微粒的组成、结构及性质(解析版) 题型:填空题
下表为部分短周期元素化合价及相应原子半径的数据:
元素性质 | 元素编号 | |||||||
A | B | C | D | E | F | G | H | |
原子半径(nm) | 0.102 | 0.110 | 0.117 | 0.074 | 0.075 | 0.071 | 0.099 | 0.077 |
最高化合价 | +6 | +5 | +4 |
| +5 |
| +7 | +4 |
最低化合价 | -2 | -3 | -4 | -2 | -3 | -1 | -1 | -4 |
已知:
①A与D可形成化合物AD2、AD3;
②E与D可形成多种化合物,其中ED、ED2 是常见的化合物,C可用于制光电池。
(1)E在周期表中位置是 ;
(2)C和H的气态氢化物的稳定性强弱关系为 (用分子式表示);
(3)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是 。
(4)工业上可用纯碱溶液处理ED和ED2,该反应如下:
ED+ED2+Na2CO3=2 +CO2
横线上某盐的化学式应为 。
(5)在一密闭容器中发生反应2AD2+D2 2AD3 ΔH=-47 kJ/mol,在上述平衡体系中加入18D2,当平衡发生移动后,AD2中18D的百分含量 (填“增加”“减少”或“不变”)其原因为 。
2AD3 ΔH=-47 kJ/mol,在上述平衡体系中加入18D2,当平衡发生移动后,AD2中18D的百分含量 (填“增加”“减少”或“不变”)其原因为 。
(6)请设计一个实验方案,使铜和稀的H2AD4溶液反应,得到蓝色溶液和氢气。绘出该实验方案装置图。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学弱电解电离(解析版) 题型:选择题
25 ℃时,a mol·L一元酸HA与b mol·L-1NaOH等体积混合后,pH为7,则下列关系一定正确的是
A.a=b B.a>b
C.c(A-)=c(Na+) D.c(A-)<c(Na+)
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学实验药品保存、基本操作、检验(解析版) 题型:选择题
下列关于仪器使用的说法正确的是
A.滴定管装滴定液时不应先用滴定液润洗
B.锥形瓶用作反应容器时一定不能加热
C.蒸馏时温度计水银球可以高于蒸馏瓶支管口
D.振荡分液漏斗时应关闭其玻璃塞和活塞
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com