
某温度时,把1 mol N2O4气体通入体积为10 L的真空密闭容器中,立即出现红棕
色,反应进行4 s时,NO2的浓度为0.04 mol·L-1,再经过一定时间后,反应达到平衡,这时
容器内的压强为开始时的1.8倍。则下列说法正确的是( )
A.前4 s以N2O4的浓度变化表示的平均反应速率为0.01 mol·L-1·s-1
B.4 s时容器内的压强为开始时的1.2倍
C.平衡时容器内含0.4 mol N2O4
D.平衡时容器内含0.8 mol NO2
答案 B
解析 N2O4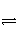
 2NO2
2NO2
n起始/mol 1 0
n变化/mol 0.2 0.04×10
n4 s/mol 0.8 0.4
前4 s N2O4的浓度变化为0.2 mol/10 L=0.02 mol·L-1;
因此前4 s N2O4的平均反应速率为0.005 mol·L-1·s-1,A不正确。4 s时气体的总的物质的量为0.8 mol+0.4 mol=1.2 mol。根据压强比等于物质的量比可得B正确。设达到平衡时,N2O4的物质的量变化了x。
N2O4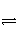
 2NO2
2NO2
n起始/mol 1 0
n变化/mol x 2x
n平衡/mol 1-x 2x
根据已知条件1 mol-x+2x=1 mol+x=1.8 mol,解得x=0.8 mol。平衡时N2O4的物质的量为1 mol-x=1 mol-0.8 mol=0.2 mol,NO2的物质的量为2x=2×0.8 mol=1.6 mol,故C、D不正确。


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是( )
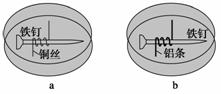
A.a中铁钉附近呈现红色 B.b中铁钉上发生还原反应
C.a中铜丝上发生氧化反应 D.b中铝条附近有气泡产生
查看答案和解析>>
科目:高中化学 来源: 题型:
取6根铁钉、6支洁净试管及其他材料,按下图所示准备。
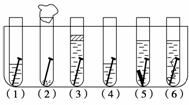
试管(1)放入一根铁钉,再注入蒸馏水,使铁钉和空气及水接触;
试管(2)的底部放入硅胶(一种干燥剂),再放入铁钉,用棉花团堵住试管口,使铁钉和干燥空气接触;
试管(3)先放入一根铁钉,趁热倒入煮沸的蒸馏水(赶出原先溶解在蒸馏水中的空气)浸没铁钉,再加上一层植物油,使铁钉不能跟空气接触;
试管(4)中放入铁钉并注入食盐水,使铁钉和空气及食盐水接触;
试管(5)放入相连的铁钉和锌片,注入自来水,浸没铁钉和锌片;
试管(6)放入相连的铁钉和铜丝,注入自来水,浸没铁钉和铜丝。
把6支试管放在试管架上,几天后观察铁钉被腐蚀的情况,其中____________试管内的铁钉未被腐蚀。从铁钉被腐蚀的情况可知引起和促进铁钉被腐蚀的条件是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有甲、乙、丙三支试管,分别加入下列物质后,观察这三支试管的颜色,其中颜色最浅的是( )
甲:10 mL 0.01 mol·L-1的FeCl3溶液和10 mL 0.01 mol·L-1的KSCN溶液
乙:5 mL水、10 mL 0.01 mol·L-1的FeCl3溶液5 mL 0.01 mol·L-1的KSCN溶液
丙:10 mL 0.1 mol·L-1的FeCl3,溶液和10 mL 0.1 mol·L-1的KSCN溶液
A.甲试管 B.乙试管 C.丙试管 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
N2的结构可以表示为 ,CO的结构可以表示为
,CO的结构可以表示为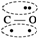 ,其中椭圆框表示π键,下列说法不正确的是( )
,其中椭圆框表示π键,下列说法不正确的是( )
A.N2分子与CO分子中都含有叁键
B.N2分子与CO分子中的π键并不完全相同
C.N2分子与CO分子中的价电子总数相等
D.N2分子与CO分子的化学性质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
密闭容器中发生可逆反应: X2(g)+Y2(g)  2Z(g)。已知起始时X2、Y2、Z各物质的浓度分别为0.1mol·L-1、0.3mol·L-1、0.2mol·L-1,反应在一定条件下达平衡时,各物质的浓度可能是()
2Z(g)。已知起始时X2、Y2、Z各物质的浓度分别为0.1mol·L-1、0.3mol·L-1、0.2mol·L-1,反应在一定条件下达平衡时,各物质的浓度可能是()
A. c(Z)=0.3mol·L-1
B. c(Y2)=0.35mol·L-1
C. c(Y2)=0.2mol·L-1
D. c(Z)=0.4mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上制备BaCl2的工艺流程图如下:
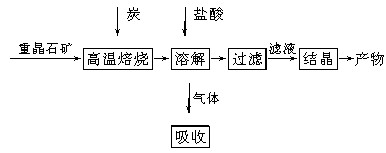
某研究小组在实验室用重晶石(主要成分为BaSO4)对工业过程进行模拟实验。查表得:
BaSO4(s)+4C(s)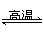
 4CO(g)+BaS(s)
4CO(g)+BaS(s)
ΔH1=571.2 kJ·mol-1 ①
BaSO4(s)+2C(s)
 2CO2(g)+BaS(s)
2CO2(g)+BaS(s)
ΔH2=226.2 kJ·mol-1 ②
(1)气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为________________________________________________________________________
________________________________________________________________________。
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,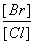 =__________________。
=__________________。
[Ksp(AgBr)=5.4×10-13 mol2·L-2,Ksp(AgCl)=2.0×10-10 mol2·L-2]
(3)反应:C(s)+CO2(g)
 2CO(g)的ΔH=________kJ·mol-1。
2CO(g)的ΔH=________kJ·mol-1。
(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是
________________________________________________________________________,
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com