
【题目】有下列几组物质,请将序号填入下列空格内:
A、CH2=CH﹣COOH和油酸( C17H33COOH)
B、12C60和石墨
C.![]() 和
和
D.35Cl和37Cl
E.乙醇和乙二醇
(1)互为同位素的是_____。
(2)互为同系物的是_____。
(3)互为同素异形体的是:_____。
(4)互为同分异构体的是_____。
(5)既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是_____
(6)写出乙醇的催化氧化方程式:_____。
【答案】D A B C E 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
【解析】
根据 “四同”的概念分析解答;根据乙醇的化学性质分析解答。
A.CH2=CH-COOH和油酸(C17H33COOH)结构相似、分子组成相差15个“CH2”原子团,故互为同系物;
B.12C60和石墨都是由碳元素组成的不同单质,故互为同素异形体;
C.![]() 和
和![]() 分子式相同,但结构不同,故互为同分异构体;
分子式相同,但结构不同,故互为同分异构体;
D.35Cl和37Cl质子数相同,中子数不同,故互为同位素;
E.乙醇和乙二醇都属于醇类。
(1)互为同位素的是35Cl和37Cl,故答案为:D;
(2)互为同系物的是CH2=CH-COOH和油酸(C17H33COOH),故答案为:A;
(3)互为同素异形体的是12C60和石墨,故答案为:B;
(4)互为同分异构体的是![]() 和
和![]() ,故答案为:C;
,故答案为:C;
(5)既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是乙醇和乙二醇,故答案为:E;
(6)乙醇在铜或银的催化下被氧气氧化生成乙醛和水,反应方程式为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。


 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)制备铝的某种化合物的工艺流程如下,下列有关说法不正确的是( )
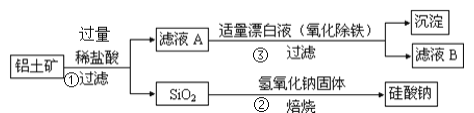
A.向滤液A中加入KSCN溶液,溶液一定会变红
B.![]() 的离子反应方程式为
的离子反应方程式为![]()
C.![]() 漂白液的目的是氧化除铁,该过程中涉及的氧化还原反应为
漂白液的目的是氧化除铁,该过程中涉及的氧化还原反应为![]()
D.![]() 中漂白液要适量,若过量则可能产生有毒的气体氯气
中漂白液要适量,若过量则可能产生有毒的气体氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(室温下与水缓慢反应)是一种新型无机材料,广泛应用于集成电路生产领域。化学研究小组同学按下列流程制取氮化铝并测定所得产物中AlN的质量分数。
己知:AlN+NaOH+3H2O=Na[Al(OH)4]+NH3↑。
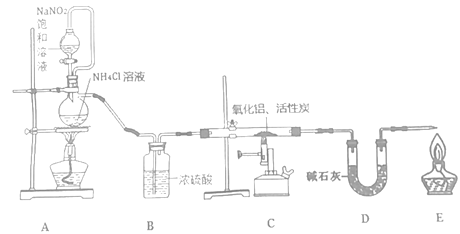
回答下列问题:
(1)检查装置气密性,加入药品,开始实验。最先点燃___(“A”、“C”或“E”)处的酒精灯或酒精喷灯。
(2)装置A中发生反应的离子方程式为___,装置C中主要反应的化学方程式为___,制得的AlN中可能含有氧化铝、活性炭外还可能含有___。
(3)实验中发现氮气的产生速率过快,严重影响尾气的处理。实验中应采取的措施是___(写出一种措施即可)。
(4)称取5.0g装置C中所得产物,加入NaOH溶液,测得生成氨气的体积为1.68 L(标准状况),则所得产物中AlN的质量分数为___。
(5)也可用铝粉与氮气在1000℃时反应制取AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,共主要原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室在 500℃时,隔绝空气加热硫酸亚铁铵[(NH4)2Fe(SO4)2]至分解完全并确定分解产物成分的装置如图所示 (已知分解的固体产物可能有 FeO、Fe2O3 和 Fe3O4,气体产物可能有 NH3、N2、H2O、SO3 和 SO2)。下列说法正 确的是( )
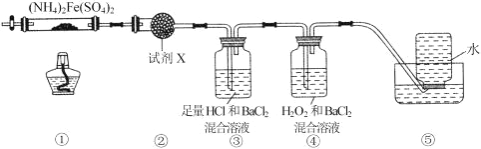
A. 取①中固体残留物与稀硫酸反应并滴加 KSCN,溶液变红,则残留物一定为 Fe2O3
B. 装置②用于检验分解产物中是否有水蒸气生成,试剂 X 最好选用碱石灰
C. 装置③用于检验分解产物中是否有 SO3 气体生成并除去 SO3 和 NH3
D. 装置④用于检验分解产物中是否有 SO2 气体生成,装置⑤用于收集生成的 NH3 和 N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A常用作有机合成的中间体,其质谱图表明其相对分子质量为84。已知16.8 g A完全燃烧生成44.0 g CO2和14.4 g H2O。请回答下列问题:
(1)A的分子式是____________。
(2)若红外光谱分析表明A分子中含有羟基和位于分子一端的C≡C键,且核磁共振氢谱上有三个峰,峰面积之比为6∶1∶1,则A的结构简式是_______。
(3)有机物B是A的同分异构体,1 mol B可与1 mol Br2加成。该有机物中所有碳原子在同一个平面上,没有顺反异构现象。写出B与新制氢氧化铜反应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取浓度相同的NaOH和HCl溶液,以3∶2体积比相混合,所得溶液的pH等于12,则原溶液的浓度为
A.0.01mol·L-1B.0.017mol·L-1
C.0.05mol·L-1D.0.50mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求书写下列化学方程式:
(1)丙烯的加聚________________________________________;
(2)1,3﹣丁二烯与等物质的量的单质溴在60℃时发生1,4﹣加成_________________________;
(3)1,2﹣二溴乙烷与氢氧化钠水溶液共热________________;
(4)乙醛的还原______________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一密闭容器中,反应mA(g)+nB(g) ![]() pC(g)达到平衡时,测得c(A)为0.5 mol·L-1;在温度不变的条件下,将容器体积扩大一倍,当达到平衡时,测得c(A)为0.3 mol·L-1。则下列判断正确的是
pC(g)达到平衡时,测得c(A)为0.5 mol·L-1;在温度不变的条件下,将容器体积扩大一倍,当达到平衡时,测得c(A)为0.3 mol·L-1。则下列判断正确的是
A. 化学计量数:m+n>p B. 平衡向正反应方向移动了
C. 物质B的转化率增大了 D. 物质C的质量分数增加了
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2 mol 某烃 A在氧气中完全燃烧后,生成 CO2 和 H2O 各 1.2 mol。试回答:
(1)烃 A 的分子式为_____。
(2)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A 的键线式为_____。
(3)若烃A能使溴水褪色,在催化剂作用下,与H2 加成,其加成产物经测定分子中含有4个甲基,烃A可能有的结构简式为 _______。(任写一种即可)
(4)比烃 A 少一个碳原子且能使溴水褪色的 A 的同系物有____种同分异构体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com