
【题目】某烧碱样品因部分变质含Na2CO3。某化学课外小组的同学用滴定法测定该烧碱样品中NaOH的质量分数。
(资料)常用的酸碱指示剂及其变色范围如下:
酚酞:pH<8.2 无色 8.2<pH<10浅红色 pH>10 红色
甲基橙:pH<3.1红色 3.1<pH<4.4橙色 pH>4.4 黄色
(实验步骤)
I. 迅速地称取烧碱样品0.50g,溶解后配制成100 mL溶液,备用。
Ⅱ.将0.1000mol/L HCl标准溶液装入酸式滴定管,调零,记录起始读数V0;用碱式滴定管取20.00 mL样品溶液于锥形瓶中,滴加2滴酚酞;以HCl标准溶液滴定至第一终点(此时溶质为NaCl和NaHCO3),记录酸式滴定管的读数V1;然后再向锥形瓶内滴加2滴甲基橙,继续用HCl标准溶液滴定至第二终点,记录酸式滴定管的读数V2。重复上述操作两次,记录数据如下:
实验序号 | 1 | 2 | 3 |
V0/ mL | 0.00 | 0.00 | 0.00 |
V1/ mL | 21.72 | 21.68 | 21.70 |
V2/ mL | 23.72 | 23.68 | 23.70 |
(1)步骤I中所需的玻璃仪器有烧杯、玻璃棒、胶头滴管和________。
(2)下列有关步骤I中样品溶液的说法正确的是________(填字母序号)。
a. 样品溶液中水的电离程度比相同pH的NaOH溶液中的小
b. c(OH-)>c(CO32-)>c(HCO3-)
c. c(H+)+ c(Na+)=c(CO32-)+c(HCO3-)+ c(OH-)
d. 向该溶液中滴加盐酸至第一终点时,n(Cl-)+n(CO32-)+n( HCO3-)+n(H2CO3)=n(Na+)
(3)酸式滴定管用蒸馏水洗净后、装入标准溶液前,应进行的操作是_______。
(4)滴定至第一终点的过程中,发生反应的离子方程式为_____。
(5)判断滴定至第二终点的现象是溶液由___色变为橙色。
(6)样品中NaOH的质量分数w(NaOH)= _____%。(计算结果保留小数点后1位)
(7)下列操作会导致测得的NaOH质量分数偏高的是____(填字母序号)。
a. 达到第一终点前,锥形瓶中有气泡产生
b. 记录酸式滴定管读数V1时,俯视标准液液面
c. 第一终点后继续滴定时,锥形瓶中有少许液体溅出
【答案】100 mL容量瓶 bd 用HCl标准溶液润洗酸式滴定管 H+ + OH-=H2O H+ + CO32-=HCO3- 黄 78.8 ac
【解析】
(1)根据配制溶液的体积分析;
(2)根据影响水电离的因素、电荷守恒、物料守恒分析;
(3)滴定管先水洗再润洗;
(4)滴定至第一终点的过程中,盐酸与氢氧化钠、碳酸钠依次发生反应;
(5)根据甲基橙的变色范围判断滴定至第二终点的现象;
(6)根据表格数据,碳酸氢钠生成二氧化碳消耗盐酸的体积为23.70-21.70=2mL,氢氧化钠消耗盐酸的体积是21.70-(23.70-21.70)=19.70 mL;
(7)达到第一终点消耗的盐酸多,则氢氧化钠的质量分数越大。
(1)步骤I是准确配制100mL溶液,所需的玻璃仪器有烧杯、玻璃棒、胶头滴管和100mL容量瓶;
(2)a. 样品溶液中的氢氧根离子主要由氢氧化钠电离和碳酸钠水解共同提供,NaOH溶液中的氢氧根离子主要由氢氧化钠电离,所以氢氧化钠溶液中氢氧化钠的浓度大于样品溶液中氢氧化钠的浓度,样品溶液中水的电离程度比相同pH的NaOH溶液中的大,故a错误;
b. 根据表格数据,碳酸氢钠生成二氧化碳消耗盐酸的体积为23.70-21.70=2mL,氢氧化钠消耗盐酸的体积是21.70-(23.70-21.70)=19.70 mL,氢氧化钠的物质的量大于碳酸钠,所以c(OH-)>c(CO32-)>c(HCO3-),故b正确;
c. 根据电荷守恒,c(H+)+ c(Na+)=2c(CO32-)+c(HCO3-)+ c(OH-),故c错误;
d. 向该溶液中滴加盐酸至第一终点时,溶质为NaCl和NaHCO3,根据物料守恒,n(Cl-)+n(CO32-)+n( HCO3-)+n(H2CO3)=n(Na+),故d正确。
(3)滴定管先水洗再润洗,酸式滴定管用蒸馏水洗净后、装入标准溶液前,应进行的操作是用HCl标准溶液润洗酸式滴定管;
(4)滴定至第一终点的过程中,盐酸与氢氧化钠、碳酸钠依次发生反应,反应离子方程式是H+ + OH-=H2O 、 H+ + CO32-=HCO3-;
(5)根据甲基橙的变色范围,滴定至第二终点的现象是溶液由黄色变为橙色;
(6)根据表格数据,碳酸氢钠生成二氧化碳消耗盐酸的体积为23.70-21.70=2mL,氢氧化钠消耗盐酸的体积是21.70-(23.70-21.70)=19.70 mL;所以氢氧化钠的物质的量是0.1 mol/L×0.0197L=0.00197mol,氢氧化钠的质量是0.00197mol×40g/mol=0.0788g,样品中NaOH的质量分数w(NaOH)= 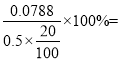 78.8%。
78.8%。
(7)a. 达到第一终点前,锥形瓶中有气泡产生,达到第一终点消耗的盐酸多,测得的NaOH质量分数偏高,故选a;
b. 记录酸式滴定管读数V1时,俯视标准液液面,达到第一终点消耗的盐酸少,测得的NaOH质量分数偏低,故不选b;
c. 第一终点后继续滴定时,锥形瓶中有少许液体溅出,第二次滴定消耗的盐酸少,达到第一终点消耗的盐酸多,测得的NaOH质量分数偏高,故选c;


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在某容积一定的密闭容器中,有下列的可逆反应:A(g)+B(g)![]() xC(g)(正反应放热)有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)
xC(g)(正反应放热)有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)
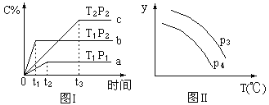
A. P3>P4,y轴表示B的转化率 B. P3<P4,y轴表示B的体积分数
C. P3<P4,y轴表示混合气体的密度 D. P3>P4,y轴表示混合气体的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为2CH3OH +3O2![]() 2CO2+ 4H2O。下列说法不正确的是
2CO2+ 4H2O。下列说法不正确的是

A.左电极为电池的负极,a处通入的物质是甲醇
B.正极反应式为:O2+ 2H2O + 4e-= 4OH-
C.负极反应式为:CH3OH + H2O-6e- = CO2+ 6H+
D.该电池提供1mole-,消耗氧气0.25mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2 mol X和2 mol Y充入2 L密闭容器中发生如下反应:X(g)+3Y(g) ![]() 2Z(g)+a Q(g)
2Z(g)+a Q(g)
达到平衡时生成0.8 mol Z,测得Q的浓度为0.4 mol/L,下列叙述错误的是
A.a的值为2 B.平衡时X的浓度为0.2 mol/L
C.平衡时Y的转化率为60% D.平衡时Z的体积百分含量为20%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中成药连花清瘟胶囊在对抗 H1N1病毒中发挥重大作用,其有效成分绿原酸的结构简式如图,下列有关说法错误的是

A. 绿原酸属于芳香族化合物
B. 分子中至少有 7 个碳原子共面
C. 1mol 绿原酸最多可消耗 5mol NaOH
D. 与绿原酸苯环上取代基种类及个数均相同的有机物有5 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散。下列判断正确的是( )
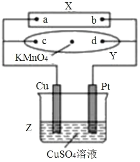
A.滤纸上c点附近会变红色
B.Cu电极质量减小,Pt电极质量增大
C.Z中溶液的pH先减小,后增大
D.溶液中的SO42-向Cu电极定向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白桦脂酸对白血病等恶性肿瘤细胞有抑制作用,其结构简式如图所示,在白桦脂酸中加入合适的试剂检验其官能团(必要时可加热),下列试剂、现象、结论都正确的一项是
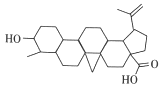
选项 | 试剂 | 现象 | 结论 |
A | 氯化铁溶液 | 溶液变色 | 含有羟基 |
B | 银氨溶液 | 有银镜产生 | 含有醛基 |
C | 碳酸氢钠溶液 | 有气泡产生 | 含有羧基 |
D | 酸性KMnO4溶液 | 溶液褪色 | 含有碳碳双键 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)文明中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的价电子排布式为_________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中SO42-的立体构型是_____。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为______ ,提供空轨道的中心微粒是_____。
③氨的沸点_____(“高于”或“低于”)膦(PH3),原因是______;氨是_____分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______。
(3)单质铜及镍都是由______键形成的晶体:元素铜与镍的第二电离能分别为:ICu=1958kJ/mol,INi=1753kJ/mol,ICu>INi的原因是______。
(4)某镍白铜合金的立方晶胞结构如图所示。
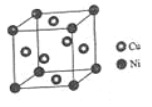
①晶胞中镍原子与铜原子的数量比为_____。
②若合金的密度为dg/cm3,晶胞参数a=________nm
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com