
| A. | 正极反应式为Mg-2e-═Mg2+ | |
| B. | 正极反应式为Ag+e-═Ag | |
| C. | 电池放电时Cl-由负极向正极迁移 | |
| D. | 负极会发生副反应Mg+2H2O═Mg(OH)2+H2↑ |
分析 Mg-AgCl电池中,活泼金属Mg是还原剂、AgCl是氧化剂,金属Mg作负极,正极反应为:2AgCl+2e-═2C1-+2Ag,负极反应式为:Mg-2e-=Mg2+,据此分析.
解答 解:A.活泼金属镁作负极,失电子发生氧化反应,反应式为:Mg-2e-=Mg2+,故A错误;
B.AgCl是难溶物,其电极反应式为:2AgCl+2e-═2C1-+2Ag,故B错误;
C.原电池放电时,阴离子向负极移动,则Cl-在正极产生由正极向负极迁移,故C错误;
D.镁是活泼金属与水反应,即Mg+2H2O=Mg(OH)2+H2↑,故D正确;
故选:D.
点评 本题考查原电池工作原理,注意常见物质的性质,如镁的还原性以及银离子的氧化性是解题的关键,题目难度中等.


科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
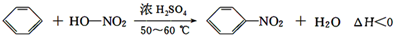
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
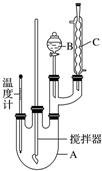
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间生成n mol A2同时生成n mol AB | |
| B. | 容器内总压不随时间变化 | |
| C. | 单位时间生成2n mol AB同时生成n mol B2 | |
| D. | 混合气体的平均相对分子质量不随时间变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
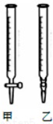 某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:| 滴定次数 | 盐酸体积mL | NaOH溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 21.30 |
| 2 | 20.00 | 0.00 | 16.30 |
| 3 | 20.00 | 0.00 | 16.32 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、I-、CO32-、ClO- | B. | Ba2+、Na+、SCN-、Cl- | ||
| C. | Fe2+、H+、K+、NO3- | D. | Cu2+、Mg2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
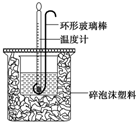 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃[来源:Z,xx,k.Com] | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.3 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 20.5 | 20.6 | 24.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/L 的Na2CO3溶液中,含有的Na+离子数为2 NA | |
| B. | 0.5 mol H2SO4含有的原子数目为3.5NA | |
| C. | 32 g O2所含的分子数目为NA | |
| D. | 27g金属铝变成铝离子时失去的电子数为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com