
| A. | 氨气可用于制造氮肥 | B. | 氯气可用于消毒和制造漂白粉 | ||
| C. | 蔗糖可以食用 | D. | 用工业酒精勾兑的白酒可以饮用 |
分析 A.氨气和酸反应生成铵盐;
B.氯气和水反应生成的HClO具有强氧化性,次氯酸能杀菌消毒,氯气和氢氧化钙反应制取漂白粉;
C.蔗糖具有甜味,可以食用;
D.工业酒精含有甲醇,甲醇有毒.
解答 解:A.氨气属于碱性气体,能和酸反应生成铵盐而制造氮肥,故A正确;
B.氯气和水反应生成的HClO具有强氧化性,次氯酸能杀菌消毒,氯气和氢氧化钙反应制取漂白粉,漂白粉的主要成分是氯化钙和次氯酸钙,故B正确;
C.蔗糖具有甜味,可以食用,故C正确;
D.工业酒精含有甲醇,甲醇有毒,用工业酒精勾兑的白酒不能饮用,容易造成甲醇中毒,故D错误;
故选;D.
点评 本题考查了生活中常见的化学知识,涉及氨气、氯气的用途,食品的安全,题目难度不大,熟悉相关物质的性质是解题关键.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:解答题
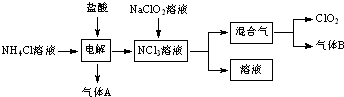
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,16 g O2和32g O3的混合物中,含有O原子数目为3NA | |
| B. | 标准状况下,1 mol Na2O和1 mol Na2O2的混合物中,含有离子总数为7NA | |
| C. | 1 mol NaBH4中离子键的数目为2NA | |
| D. | 在K35ClO3+6H37Cl═KCl+3Cl2↑+3H2O中,若生成71 g Cl2,转移的电子数目为$\frac{5}{3}$NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
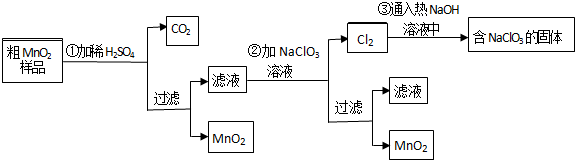
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
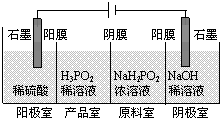 次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极质量不变 | B. | 电流通过导线由铜片流向银片 | ||
| C. | 烧杯中Ag+浓度逐渐减小 | D. | 电池工作时,铜片失电子,被还原 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com