
分析 (1)X若为氢时,其最外层电子数为1;X若为硫,原子序数比X大的Y、Z、W不可能都是短周期元素;
(2)氧化镁溶于酸,氧化铝溶于强酸、强碱,四种元素可能有1种是铝元素;
(3)白色沉淀应为碱,短周期元素中只有Mg(OH)2符合;
(4)滤液中加入过量的盐酸溶液,得到的应是难溶于水的弱酸,可为H2SiO3或H4SiO4;
X、Y、Z、W四种元素中的3种为Mg、Al、Si,只有X为碳时才符合X与W同主族且X原子序数最小的条件.
解答 解:(1)X若为氢时,其最外层电子数为1,不合理;X若为硫,原子序数比X大的Y、Z、W不可能都是短周期元素,不合理,X为碳或氧时合理,故答案为:AD;
(2)氧化镁溶于酸,氧化铝溶于强酸、强碱,四种元素可能有1种是铝元素,故答案为:可能;
(3)对所有短周期元素进行试探,唯有镁元素符合性质,可知白色沉淀物的化学式为Mg(OH)2,故答案为:Mg(OH)2;
(4)唯有硅元素在变化中最终得到白色沉淀H2SiO3(或H4SiO4),生成该白色沉淀的离子方程式为SiO32-+2H+=H2SiO3↓(或SiO32-+2H++H2O=H4SiO4↓),
X、Y、Z、W四种元素中的3种为Mg、Al、Si,只有X为碳时才符合X与W同主族且X原子序数最小的条件,X与浓H2SO4反应的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:SiO32-+2H+=H2SiO3↓;碳;C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
点评 本题考查无机物的推断,题目难度中等,注意根据元素对应原子结构特点以及单质、化合物的相关性质进行推断,学习中要注重相关知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 9种 | B. | 10种 | C. | 12种 | D. | 15种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5L | B. | 5.5L | C. | 6L | D. | 6.5L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | T 1时,v正>v逆 | |
| B. | 正反应的△H<0 | |
| C. | a、b两点的反应速率 v( a)=v( b) | |
| D. | T<T 1时,ω增大的原因是平衡向正方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
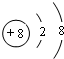 .
. 和XY2
和XY2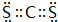 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 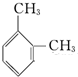 | B. | 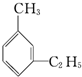 | C. | 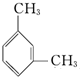 | D. | 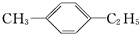 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
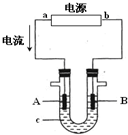 电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH2-NO2和H2N-CH2-COOH互为同分异构体 | |
| B. | O2和O3互为同素异形体 | |
| C. | H、D、T互为同位素 | |
| D. | 干冰和冰为同一种物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com