
如图是三种稀酸对FeCr合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的是( )

A.稀硝酸对FeCr合金的腐蚀性比稀硫酸和稀盐酸的弱
B.稀硝酸和铁反应的化学方程式是Fe+6HNO3(稀)===Fe(NO3)3+3NO2↑+3H2O
C.Cr含量大于13%时,因为三种酸中盐酸的氢离子浓度最大,所以对FeCr合金的腐蚀性最强
D.随着Cr含量增加,稀硝酸对FeCr合金的腐蚀性减弱
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)烧瓶、锥形瓶、量筒加热时均需要垫石棉网( )
(2)加热试管时先均匀加热,后局部加热( )
(3)用10 mL的量筒准确量取8.80 mL的稀硫酸( )
(4)坩埚加热时直接放在铁圈或三脚架上加热( )
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列仪器或装置,请回答下列问题:
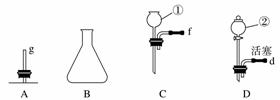
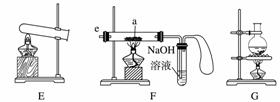
(1)仪器①的名称是__________________,②的名称是________________________。
(2)用上图仪器组装成气体发生装置:用KClO3和MnO2制O2应选的装置是________(填字母,下同);用废H2O2与MnO2制O2,并控制产生O2的速率,应选的装置是________。
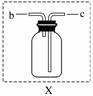
(3)若用装置X进行“排空气法”收集制取的O2,氧气应从__________(填“b”或“c”,下同)端导入。若瓶中装满水,用排水法收集氧气,氧气应从__________端导入。
(4)若用F装置进行CO还原Fe2O3的实验,实验室制取CO的方法一般采取甲酸脱水法(HCOOH CO↑+H2O),用纯净的CO完成该实验。
CO↑+H2O),用纯净的CO完成该实验。
①除F、X外还需要的装置有________,X中应加入的试剂是________,X与其他导管连接的顺序是______________________(填导管口的序号);
②实验时,a处的可能的现象为___________________________________________;
F装置中气球的作用是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:
H2O NH3 NH3、NH4HCO3 滤液
↓ ↓ ↓ ↑
水氯镁石→ →
→ →
→ →
→ →
→ →碱式碳酸镁
→碱式碳酸镁
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为________。
(3)高温煅烧碱式碳酸镁得到MgO。取碱式碳酸镁4.66 g,高温煅烧至恒重,得到固体2.00 g和标准状况下CO2 0.896 L,通过计算确定碱式碳酸镁的化学式。
(4)若热水解不完全,所得碱式碳酸镁中将混有MgCO3,则产品中镁的质量分数________(填“升高”、“降低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应广泛应用于金属的冶炼。下列说法不正确的是( )
A.冶炼铁的主要原料有铁矿石、焦炭、空气、石灰石等,其中石灰石的作用是除去铁矿石中的脉石(二氧化硅)
B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应
C.工业上Mg可由电解熔融的MgO制取,Na也可由电解熔融的NaCl制取
D.铝热法还原铁的反应中,放出的热量能使铁熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
铜器久置,表面会生成一层绿色固体,为了解铜在空气中的腐蚀情况,某化学兴趣小组收集家中铜器表面的绿色固体进行探究。查阅相关资料后,猜想该绿色物质可能是铜的碳酸盐。
该小组同学利用下图装置进行实验(部分夹持仪器略)。
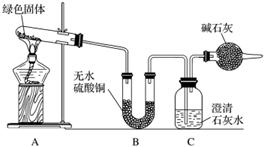
①对试管内的绿色固体进行加热,至完全分解,观察到A装置中绿色固体逐渐变成黑色,B装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊。
②取少量加热后生成的黑色固体于试管中,加入稀硫酸,观察到黑色固体逐渐溶解,溶液变成蓝色。
③取少量上述蓝色溶液于试管中,浸入一根洁净的铁丝。观察到铁丝表面有红色物质析出。
请回答下列问题:
(1)绿色固体中含有的元素是_______________________________________________。
(2)加热后试管中剩余的黑色物质是___________________________________________。
(3)假设该绿色物质是一种纯净物,则其化学式可能是________________________,加热分解的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(4)上述实验步骤③中的反应的离子方程式为_______________________________
________________________________________________________________________。
(5)实验装置最后的干燥管的作用是__________________________________。
(6)如果将B、C两装置对调,能否达到实验目的______(填“能”或“不能”),为什么?________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下,将3.36 L CO2气体通入200 mL 1.00 mol·L-1 NaOH溶液中,充分反应后溶液中c(CO )与c(HCO
)与c(HCO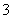 )的比值为(不考虑CO
)的比值为(不考虑CO 、HCO
、HCO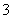 的水解)( )
的水解)( )
A.1∶1 B.1∶2
C.2∶1 D.1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
将足量CO2气体通入水玻璃(Na2SiO3溶液)中,然后加热蒸干,再在高温下充分灼烧,最后得到的固体物质是( )
A.Na2SiO3 B.Na2CO3、Na2SiO3
C.Na2CO3、SiO2 D.SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是某研究性学习小组设计制取氯气并以氯气为反应物进行特定反应的装置。
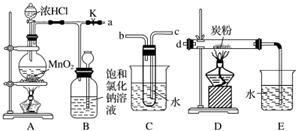
(1)要将C装置接入B和D之间,正确的接法是a→____→________→d。
(2)实验开始先点燃A处的酒精灯,打开活塞K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为___________________________________________________。
为了使C装置发挥更好的作用,可向烧杯中加入浓硫酸,加入浓硫酸的作用是________________________________________________________________________
________________________________________________________________________。
(3)D处反应完毕后,关闭弹簧夹K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是_________________________________________________________,
B的作用是______________________________________________________。
(4)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由并在方框中画出改进后的装置图。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com