
 H2(g) + CO(g), ΔH =" +131.3" kJ·mol-1,ΔS =" +133.7" J·mol-1·K-1
H2(g) + CO(g), ΔH =" +131.3" kJ·mol-1,ΔS =" +133.7" J·mol-1·K-1 2NH3(g)的K=0.5,
2NH3(g)的K=0.5, N2 (g)+ 3H2(g)的K= (填数值)。
N2 (g)+ 3H2(g)的K= (填数值)。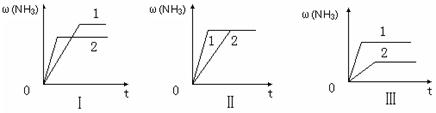
| A.图Ⅰ可能是不同压强对反应的影响,且P2>P1 |
| B.图Ⅱ可能是不同压强对反应的影响,且P1>P2 |
| C.图Ⅲ可能是不同温度对反应的影响,且T1>T2 |
| D.图Ⅱ可能是同温同压下,催化剂性能,1>2 |


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源:不详 题型:计算题
 xB(气)+C(气)并达到平衡,A在平衡混合气中的体积百分含量为58.6%,混合气的总质量为46g,密度为0.72g·L-1。求:
xB(气)+C(气)并达到平衡,A在平衡混合气中的体积百分含量为58.6%,混合气的总质量为46g,密度为0.72g·L-1。求:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g)+H2O(g);△H=-49.0kJ/mol测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g);△H=-49.0kJ/mol测得CO2和CH3OH(g)的浓度随时间变化如图所示。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO(g)+H2O(g),
CO(g)+H2O(g),| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
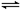 2SO3(g) △H=-196.6 kJ·mol-1
2SO3(g) △H=-196.6 kJ·mol-1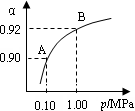
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
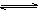 C(g)+3D(g),现分别从两条途径建立平衡:I.A、B的起始浓度均为2 mol·L-1 Ⅱ.C、D的起始浓度分别为2 mol·L-1和6 mol·L-1.下列说法正确的是( )
C(g)+3D(g),现分别从两条途径建立平衡:I.A、B的起始浓度均为2 mol·L-1 Ⅱ.C、D的起始浓度分别为2 mol·L-1和6 mol·L-1.下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向SO2水溶液中加盐酸有利于SO32-离子浓度的减少 |
| B.加入催化剂有利于氨的氧化反应 |
| C.室温下比高温更有利于合成氨中氨的生成 |
| D.用排饱和食盐水来除Cl2中HCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g)(正反应为放热反应),为了使平衡向生成氨的方向移动,可采用的方法是
2NH3(g)(正反应为放热反应),为了使平衡向生成氨的方向移动,可采用的方法是| A.增大压强 | B.减小压强 | C.升高温度 | D.使用催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com