
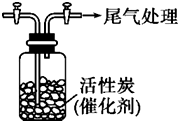
 ijѧϰС������SO2���л�ԭ�ԣ��Ʋ�SO2�ܱ�Cl2��������SO2Cl2���������ϣ�SO2Cl2�ڳ�����Ϊ��ɫҺ�壬����ˮ�⣬����ʪ���������������
ijѧϰС������SO2���л�ԭ�ԣ��Ʋ�SO2�ܱ�Cl2��������SO2Cl2���������ϣ�SO2Cl2�ڳ�����Ϊ��ɫҺ�壬����ˮ�⣬����ʪ������������������� I�������ڻ������У�Ԫ�ػ��ϼ۵Ĵ�����Ϊ����н��
�������̺�Ũ���ᷴӦ�����������Ȼ��̺�ˮ��
�������ڱ��͵��Ȼ��������ܣ��Ȼ������������У�Ũ���������ˮ�ԣ����Ը���������
������1����SO2Cl2��H2O��Ӧ����������Ȼ��⣻
���������������ӷ�Ӧ���ɲ���Һ������Ȼ���������ע��Ӧ�ȼ������ᱵ��Һ�����ų���������ӵĸ��ţ�
��2��SO2��Cl2����SO2Cl2�ķ�ӦΪ���淴Ӧ��SO2Cl2�ֽ�õ��������Ͷ���������ˮ��Һ�з���������ԭ��Ӧ����������Ȼ��⣬�������Ȼ�����Ӧ�������ᱵ������
��� �⣺I��SO2Cl2�У���Ϊ-2�ۣ���Ϊ-1�ۣ�����Ԫ�صĻ��ϼ�Ϊx�������ڻ������У�Ԫ�ػ��ϼ۵Ĵ�����Ϊ���֪��X+��-2����2+��-1����2=0����ã�X=+6��������Ԫ�ػ��ϼ�Ϊ+6�ۣ�
�ʴ�Ϊ��+6�ۣ�
II���������̺�Ũ���ᷴӦ���̴�+4�۽�Ϊ+2�ۣ��ȴ�-1����Ϊ0�ۣ���Ӧ�ķ���ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
�ʴ�Ϊ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
���Ȼ����ӷ�����ȡ�������к����Ȼ����ˮ�������Ȼ��⼫������ˮ�������ڱ��͵��Ȼ�����Һ�����ܣ����Խ��Ƶõ�����ͨ�������Ȼ�����Һ����ȥ�Ȼ������壬Ҫ�ռ����������Ӧ��ȥ�����е�ˮ������ѡ��Ũ������Ը���������
�ʴ�Ϊ�������Ȼ�����Һ��Ũ���
������1����SO2Cl2�ڳ�����Ϊ��ɫҺ�壬����ˮ�⣬����ʪ�������������Ϊ�Ȼ������Һ������SO2Cl2��ˮ��Ӧ����Ԫ�صĻ��ϼ۲��䣬������������ᣬ��Ӧ�ķ���ʽΪ��SO2Cl2+2H2O=H2SO4+2HCl��
�ʴ�Ϊ��SO2Cl2+2H2O=H2SO4+2HCl��
��Ҫ������Һ�е�������Ӧ�ų���������ӵĸ��ţ����ԣ�ȡ��������Һ���Թ��У��������Ba��NO3��2��Һ�����ˣ�����Һ�еμ�HNO3�ữ���ټ���AgNO3��Һ����������ɫ��������˵����Һ����Cl-��
�ʴ�Ϊ��ȡ��������Һ���Թ��У��������Ba��NO3��2��Һ�����ˣ�����Һ�еμ�HNO3�ữ���ټ���AgNO3��Һ����������ɫ��������˵����Һ����Cl-��
��2����SO2��Cl2����SO2Cl2�ķ�ӦΪ���淴Ӧ��SO2Cl2�ֽ�õ��������Ͷ���������ˮ��Һ�з���������ԭ��Ӧ��SO2+Cl2+2H2O�T2HCl+H2SO4������������Ȼ��⣬�������Ȼ�����Ӧ�������ᱵ������
�ʴ�Ϊ��BaSO4��
��SO2��Cl2�������Ϸ�Ӧ��SO2+Cl2?SO2 Cl2�����ڰ�ɫ������BaSO4�����Է�Ӧ��Ļ�������б�Ȼ����SO2��Cl2�������壬���SO2��Cl2����SO2Cl2�ķ�ӦΪ���淴Ӧ��
�ʴ�Ϊ��SO2+Cl2?SO2Cl2�����ڰ�ɫ������BaSO4�����Է�Ӧ��Ļ�������б�Ȼ����SO2��Cl2�������壮���SO2��Cl2����SO2Cl2�ķ�ӦΪ���淴Ӧ��
���� ��������SO2���л�ԭ�Խ��з�Ӧ�����ʵ��̽������ȷ������������ʡ�SO2Cl2��Ϣ�Ĵ����ǽ���ؼ���ע�����Ӽ���ķ�����������ѧ���ۺ�Ӧ��֪ʶ����������Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ�鷽�� | ʵ��Ŀ�Ļ���� |
| A | ȡһ��Сľ�������뱥��������Һ�У������ʪ������ȡ�������ɺ����ھƾ������洦��ľ��δȼ�� | ֤�������ƿ���ľ�ķ���� |
| B | ��ȡ��δ֪Ũ������������Һ����ƿ�м���2mL��̪��Ȼ�������ȷ�ζ������һ��������룬��Һ�ɺ�ɫ��Ϊ��ɫ�Ұ���Ӳ��ָ� | ȷ�ж���֪Ũ�ȵ�����ζ�δ֪Ũ�ȵ�����������Һ�ĵζ����յ� |
| C | ��װ��ʯ��ʯ�ļ������շ������м���Ũ���ᣬ��������������ͨ���������̼��������Һ����ͨ�뱽������Һ�У���������Һ�������� | ���ԣ����̼����� |
| D | ��ʢ�б��ӵ�Ũ��Һ���Թ�����μ���ϡ��ˮ���ߵα��� | ���ӵĶ��Լ��� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ֽ��ˮͨ����ѹˮ��ѹ�����»��ܶ��У��ɼ�����Ⱦ | |
| B�� | ú��������Һ�������ú�������ʡ�������Ⱦ | |
| C�� | �ȼҵ�еġ��ָ����Na2CO3 | |
| D�� | ú�ĸ���ʯ�͵ķ���Ϊ�����仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���ʳ��ˮ���ռ� | B�� | �ϳɰ��еĴ��ϳ� | ||
| C�� | ���������еĴ����� | D�� | ����еİ���ˮ̼�ữ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2C2O4��Һ�У�2c��Na+��=c��C2O42-��+c��HC2O4-��+c��H2C2O4�� | |
| B�� | 0.1 mol•L-1�Ĵ�������Һ20 mL��0.1 mol•L-1����10 mL��Ϻ���Һ�����ԣ�����c��CH3COO-����c��Cl-����c��H+����c��CH3COOH�� | |
| C�� | ����������ʵ���Ũ�ȵ�NaCl��NaClO��Һ��������Һ�������������ǰ�ߴ� | |
| D�� | 0.1mol?L-1��NaHA��Һ����pH=4��c��HA-����c��H+����c��H2A����c��A2-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=1��NaHSO4��Һ��c��Na+��+c��H+��=c��SO42-��+c��OH-�� | |
| B�� | ��10mL pH=l2��NaOH��Һ�еμӵ����pH=2��CH3COOH��c��CH3COO-����c��Na+����c��OH-����C��H+�� | |
| C�� | 0.10 mol•L-1 NaHCO3��Һ��ˮϡ�ͺ�n ��H+����n ��OH-���ij˻���� | |
| D�� | 0.1mol/LNH4Cl��0.1mol/L��ˮ����������Һ�Լ��ԣ�c��NH3•H2O����c��NH4+����c��Cl-����c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
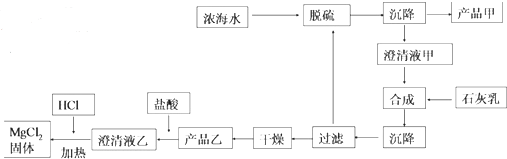
| ���� | Na+ | Mg2+ | Cl- | SO${\;}_{4}^{2-}$ |
| Ũ��/��g•L-1�� | 63.7 | 28.8 | 144.6 | 46.4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com