
| A. | 光导纤维是以二氧化硅为主要原料制成的 | |
| B. | 在西部和沿海地区兴建风力发电站,解决能源短缺问题 | |
| C. | 糖类、油脂、蛋白质都属于天然有机高分子化合物 | |
| D. | 铁质器具表面刷漆或将其置于干燥处保存,均能有效减缓铁的锈蚀 |
分析 A.二氧化硅具有良好的光学特性;
B.风力发电,可解决火力发电的资源问题;
C.油脂相对分子质量小于10000;
D.金属腐蚀的条件:潮湿的环境、氧气存在;
解答 解:A.二氧化硅具有良好的光学特性,是制造光导纤维主要原料,故A正确;
B.风力发电是一种清洁能源,建风力发电站,解决能源短缺问题,故B正确;
C.油脂相对分子质量小于10000,不是高分子化合物,故C错误;
D.铁质器具表面刷漆可以隔绝氧气,将其置于干燥处保存,与水不接触,铁不易生成锈,故D正确;
故选:C.
点评 本题为综合题,考查了物质的性质与用途、新能源的开发与利用、高分子化合物判断、金属的腐蚀与防护,熟悉相关知识是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA | |
| B. | 5.6g铁粉与足量水蒸气反应生成的H2分子数目为0.1NA | |
| C. | 向0.1mol/L的FeBr2溶液中通入适量Cl2,当c (Br-)=0.1mol/L时,消耗Cl2的分子数为0.1NA | |
| D. | 在反应Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2中,每生成1molCu,转移电子的数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打溶液电离:NaHCO3═Na++H++CO32- | |
| B. | 明矾净水原理:Al3++3H2O?Al(OH)3↓+3H+ | |
| C. | 稀醋酸呈酸性:CH3COOH+H2O?CH3COO-+H3O+ | |
| D. | 重晶石的电离:BaSO4?Ba2++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2(SO4)3和小苏打反应,可用于泡沫灭火器灭火 | |
| B. | 次氯酸盐具有氧化性,可用于漂白织物 | |
| C. | 铁比铜金属性强,可用Fe腐蚀Cu刻制印刷电路板 | |
| D. | HF与SiO2反应氢氟酸,可用于在玻璃器皿上刻蚀标记 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3溶液滴入沸水中制备Fe(OH)3胶体:$Fe_{\;}^{3+}$+$3OH_{\;}^-$═Fe(OH)3(胶体) | |
| B. | Cu溶于稀硝酸:Cu+2$H_{\;}^+$+$NO_3^-$═$Cu_{\;}^{2+}$+NO2↑+H2O | |
| C. | 向苯酚钠溶液中通入少量的CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| D. | 氯气溶于水:Cl2+H2O═2H++$Cl_{\;}^-$+$ClO_{\;}^-$ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
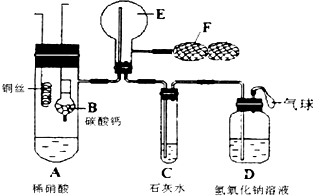 为了证明铜和稀硝酸反应产生一氧化氮气体,某学校学生实验小组设计了一个实验,其装置如图所示(加热装置与固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是可控制气体流向,用于鼓入空气的双连打气球.
为了证明铜和稀硝酸反应产生一氧化氮气体,某学校学生实验小组设计了一个实验,其装置如图所示(加热装置与固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是可控制气体流向,用于鼓入空气的双连打气球.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com