
分析 一般来说,活泼金属与非金属形成离子键,非金属性之间形成共价键,含离子键的一定为离子化合物,以此来解答.
解答 解:①Ne不含化学键;
②HCl只含H-Cl共价键,为共价化合物;
③P4只含P-P共价键,为单质;
④Na2O2含离子键和共价键,为离子化合物;
⑤Na2S只含离子键,为离子化合物;
⑥NaOH含离子键和共价键,为离子化合物;
⑦H2O2含共价键,为共价化合物;
⑧NH4Cl含离子键和共价键,为离子化合物;
⑨AlCl3含共价键,为共价化合物;
⑩MgCl2中只含离子键,为离子化合物;
(1)只存在共价键的是①②⑦⑨,故答案为:①②⑦⑨;
(2)只存在离子键的是⑤⑩,故答案为:⑤⑩;
(3)属于离子化合物的是④⑤⑥⑧⑩,故答案为:④⑤⑥⑧⑩;
(4)属于共价化合物的是②⑦⑨,故答案为:②⑦⑨.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④⑤⑥ | C. | ①③⑥ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
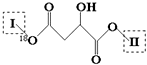 (其中I、II为未知部分的结构):为推测X的分子结构,现进行如图所示的转化.
(其中I、II为未知部分的结构):为推测X的分子结构,现进行如图所示的转化.
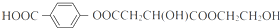 .
. .
.
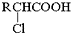 ;RCH2Br$→_{②H_{2}O/H+}^{①NaCN}$RCH2COOH
;RCH2Br$→_{②H_{2}O/H+}^{①NaCN}$RCH2COOH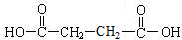 .
.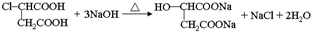 .
.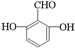 、
、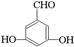 、
、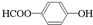 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
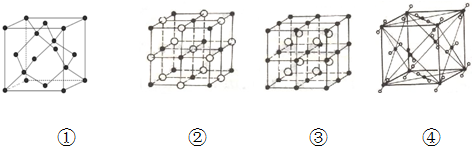
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO3+H2O═H2SO4 | B. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | AgNO3+HCl═AgCl↓+HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
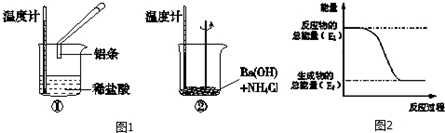
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
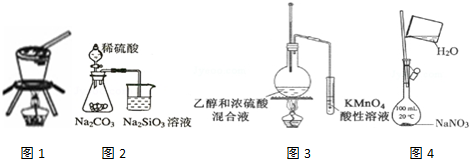
| A. | 用图1装置从饱和食盐水中提取NaCl晶体 | |
| B. | 用图2装置证明非金属性强弱 S>C>Si | |
| C. | 用图3装置验证乙烯的生成 | |
| D. | 用图4装置配制一定物质的量浓度的NaNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
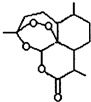 合理使用药物是保证身心健康、提高生活质量的有效手段.药物化学已经成为化学的一个重要领域.
合理使用药物是保证身心健康、提高生活质量的有效手段.药物化学已经成为化学的一个重要领域.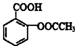 是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为
是常用的解热镇痛药,可以由水杨酸与乙酸酐反应制取,反应原理为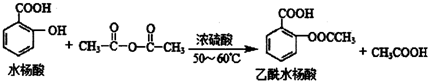
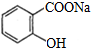 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com