
| A、HCO3-水解的离子方程式:HCO3-+H2O═CO32-+H3O+ | ||
| B、漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3- | ||
| C、过量的SO2通入NaOH溶液中:SO2-+2OH-=SO32-+H2O | ||
D、新制氢氧化铜和乙醛反应:CH3CHO+2Cu(OH)2+OH-
|
| △ |


科目:高中化学 来源: 题型:
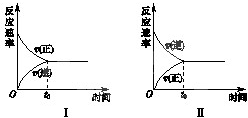 t℃时,在两个相同的密闭刚性容器(恒容)中分别进行SO2和SO3相互转化的实验,反应的化学方程式为2SO2(g)+O2(g)?2SO3(g),实验Ⅰ和实验Ⅱ的情况分别如图Ⅰ和图Ⅱ所示:
t℃时,在两个相同的密闭刚性容器(恒容)中分别进行SO2和SO3相互转化的实验,反应的化学方程式为2SO2(g)+O2(g)?2SO3(g),实验Ⅰ和实验Ⅱ的情况分别如图Ⅰ和图Ⅱ所示:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Cu2+、NO3-、Cl- |
| B、Na+、Zn2+、OH-、Br- |
| C、K+、SO42-、Cl-、Mg2+ |
| D、Ba2+、Na+、OH-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2+、Na+、Cl-、SO42- |
| B、K+、Na+、Cl-、Cu2+ |
| C、K+、Na+、NO3-、CO32- |
| D、Na+、Ba2+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHB溶液不一定呈酸性,Na2B溶液不一定呈碱性 |
| B、在Na2B溶液中一定有:c(Na+)=2c(B2-)+c(HB-)+c(H2B) |
| C、NaHB水溶液中一定有:c(Na+)+c(H+)=c(HB-)+c(OH-)+2c(B2-) |
| D、在Na2B溶液中一定有:2c(OH-)=c(H+)+c(HB-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两种物质的阴离子半径都比阳离子半径小 |
| B、与水反应时,水都做氧化剂 |
| C、与盐酸反应都只生成一种盐 |
| D、溶于水,所得溶液都能使无色酚酞变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:
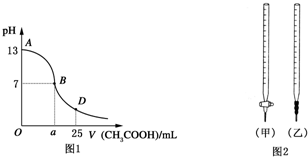 Ⅰ.如图1为向25mL 0.1mol?L-1NaOH溶液中逐滴滴加0.2mol?L-1CH3COOH溶液过程中溶液pH的变化曲线.请回答:
Ⅰ.如图1为向25mL 0.1mol?L-1NaOH溶液中逐滴滴加0.2mol?L-1CH3COOH溶液过程中溶液pH的变化曲线.请回答:| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 酚酞 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 石蕊 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
查看答案和解析>>
科目:高中化学 来源: 题型:
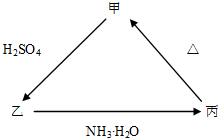 甲、乙、丙三种物质之间有如下图所示的转化关系,其中甲物质为氧化物:
甲、乙、丙三种物质之间有如下图所示的转化关系,其中甲物质为氧化物:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com