
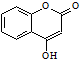
 ŹĒŅ»ÖÖŅ½Ņ©ÖŠ¼äĢ壮³£ÓĆĄ“Öʱøæ¹ÄżŃŖŅ©£¬æÉĶعżĻĀĮŠĀ·ĻßŗĻ³É£ŗ
ŹĒŅ»ÖÖŅ½Ņ©ÖŠ¼äĢ壮³£ÓĆĄ“Öʱøæ¹ÄżŃŖŅ©£¬æÉĶعżĻĀĮŠĀ·ĻßŗĻ³É£ŗ

 ŗĶŅŅ“¼ĪŖŌĮĻ£¬Öʱø
ŗĶŅŅ“¼ĪŖŌĮĻ£¬Öʱø  µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£©£®ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼Ź¾ĄżČēĻĀ£ŗCH2=CH2$\stackrel{HBr}{”ś}$ CH3CH2Br$”ś_{”÷}^{NaOH}$CH3CH2OH£®
µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪÓĆ£©£®ŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼Ź¾ĄżČēĻĀ£ŗCH2=CH2$\stackrel{HBr}{”ś}$ CH3CH2Br$”ś_{”÷}^{NaOH}$CH3CH2OH£® ·ÖĪö AÓėŅų°±ČÜŅŗ·“Ó¦ÓŠŅų¾µÉś³É£¬ŌņAÖŠ“ęŌŚČ©»ł£¬ÓÉĮ÷³ĢæÉÖŖ£¬AÓėŃõĘų·“Ó¦æÉŅŌÉś³ÉŅŅĖį£¬ŌņAĪŖCH3CHO£¬ÓÉBŗĶCµÄ½į¹¹¼ņŹ½æÉŅŌ擳ö£¬ŅŅĖį·Ö×ÓÖŠµÄōĒ»ł±»ĀČŌ×ÓČ”“ś£¬·¢ÉśĮĖČ”“ś·“Ó¦£¬DÓė¼×“¼ŌŚÅØĮņĖįĢõ¼žĻĀ·¢Éśõ„»Æ·“Ӧɜ³ÉE£¬EµÄ½į¹¹ĪŖ £¬ÓÉFµÄ½į¹¹¼ņŹ½æÉÖŖ£¬CŗĶE ŌŚ“߻ƼĮĢõ¼žĻĀĶŃČ„Ņ»øöHCl·Ö×ӵƵ½F£¬FÖŠ“ęŌŚõ„»ł£¬ŌŚ¼īŅŗÖŠæÉŅŌ·¢ÉśĖ®½ā·“Ó¦£¬ŅŌ
£¬ÓÉFµÄ½į¹¹¼ņŹ½æÉÖŖ£¬CŗĶE ŌŚ“߻ƼĮĢõ¼žĻĀĶŃČ„Ņ»øöHCl·Ö×ӵƵ½F£¬FÖŠ“ęŌŚõ„»ł£¬ŌŚ¼īŅŗÖŠæÉŅŌ·¢ÉśĖ®½ā·“Ó¦£¬ŅŌ ŗĶŅŅ“¼ĪŖŌĮĻ£¬Öʱø
ŗĶŅŅ“¼ĪŖŌĮĻ£¬Öʱø  £¬æÉŅŌ½«
£¬æÉŅŌ½« ŌŚ¼īŠŌĢõ¼žĻĀĖ®½āµĆ±½¼×“¼£¬ŌŁŃõ»ÆµĆ±½¼×Ėį£¬ŌŁÓėŅŅ“¼·¢Éśõ„»Æ·“Ó¦µĆ²śĘ·£¬¾Ż“Ė“šĢā£®
ŌŚ¼īŠŌĢõ¼žĻĀĖ®½āµĆ±½¼×“¼£¬ŌŁŃõ»ÆµĆ±½¼×Ėį£¬ŌŁÓėŅŅ“¼·¢Éśõ„»Æ·“Ó¦µĆ²śĘ·£¬¾Ż“Ė“šĢā£®
½ā“š ½ā£ŗAÓėŅų°±ČÜŅŗ·“Ó¦ÓŠŅų¾µÉś³É£¬ŌņAÖŠ“ęŌŚČ©»ł£¬ÓÉĮ÷³ĢæÉÖŖ£¬AÓėŃõĘų·“Ó¦æÉŅŌÉś³ÉŅŅĖį£¬ŌņAĪŖCH3CHO£¬ÓÉBŗĶCµÄ½į¹¹¼ņŹ½æÉŅŌ擳ö£¬ŅŅĖį·Ö×ÓÖŠµÄōĒ»ł±»ĀČŌ×ÓČ”“ś£¬·¢ÉśĮĖČ”“ś·“Ó¦£¬DÓė¼×“¼ŌŚÅØĮņĖįĢõ¼žĻĀ·¢Éśõ„»Æ·“Ӧɜ³ÉE£¬EµÄ½į¹¹ĪŖ £¬
£¬
¢ŁÓÉŅŌÉĻ·ÖĪöæÉÖŖAĪŖCH3CHO£¬¹Ź“š°øĪŖ£ŗCH3CHO£»
¢ŚÓÉBŗĶCµÄ½į¹¹¼ņŹ½æÉŅŌ擳ö£¬ŅŅĖį·Ö×ÓÖŠµÄōĒ»ł±»ĀČŌ×ÓČ”“ś£¬·¢ÉśĮĖČ”“ś·“Ó¦£¬¹Ź“š°øĪŖ£ŗČ”“ś·“Ó¦£»
¢ŪŌŚÅØĮņĖį×÷“߻ƼĮ”¢¼ÓČČĢõ¼žĻĀ£¬ĮŚōĒ»ł±½¼×ĖįŗĶ¼×“¼·¢Éśõ„»Æ·“Ӧɜ³ÉĮŚōĒ»ł±½¼×Ėį¼×õ„ŗĶĖ®£¬Ęä·“Ó¦·½³ĢŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
¢ÜFÖŠ“ęŌŚõ„»ł£¬ŌŚ¼īŅŗÖŠæÉŅŌ·¢ÉśĖ®½ā·“Ó¦£¬·½³ĢŹ½ĪŖ£ŗ £¬ĖłŅŌ1molF×ī¶ąĻūŗÄ3molNaOH£¬
£¬ĖłŅŌ1molF×ī¶ąĻūŗÄ3molNaOH£¬
¹Ź“š°øĪŖ£ŗ3£»
¢Żøł¾ŻGµÄ½į¹¹¼ņŹ½£ŗa£®GÖŠÓŠĢ¼Ģ¼Ė«¼ü£¬ÄÜÓėäåĖ®·¢Éś¼Ó³É·“Ó¦£¬¹ŹaÕżČ·£»b£®GÖŠÓŠōĒ»ł£¬ÄÜÓė½šŹōÄĘ·“Ó¦£¬¹ŹbÕżČ·£»c.1mol G×ī¶ąÄÜŗĶ4molĒāĘų·“Ó¦£¬¹Źc“ķĪó£»d£®GµÄ·Ö×ÓŹ½ŹĒC9H6O3£¬¹ŹdÕżČ·£¬¹ŹŃ”c£»
ŅŌ ŗĶŅŅ“¼ĪŖŌĮĻ£¬Öʱø
ŗĶŅŅ“¼ĪŖŌĮĻ£¬Öʱø  £¬æÉŅŌ½«
£¬æÉŅŌ½« ŌŚ¼īŠŌĢõ¼žĻĀĖ®½āµĆ±½¼×“¼£¬ŌŁŃõ»ÆµĆ±½¼×Ėį£¬ŌŁÓėŅŅ“¼·¢Éśõ„»Æ·“Ó¦µĆ²śĘ·£¬ŗĻ³ÉµÄĀ·ĻßĮ÷³ĢĶ¼ĪŖ
ŌŚ¼īŠŌĢõ¼žĻĀĖ®½āµĆ±½¼×“¼£¬ŌŁŃõ»ÆµĆ±½¼×Ėį£¬ŌŁÓėŅŅ“¼·¢Éśõ„»Æ·“Ó¦µĆ²śĘ·£¬ŗĻ³ÉµÄĀ·ĻßĮ÷³ĢĶ¼ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗc£» £»
£»
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄĶʶĻÓėŗĻ³É£¬ĪŖøßæ¼³£¼ūĢāŠĶ£¬×ŪŗĻæ¼²éѧɜ·ÖĪöĪŹĢāµÄÄÜĮ¦ŗĶ»ÆѧÖŖŹ¶µÄ×ŪŗĻŌĖÓĆÄÜĮ¦£¬ĢāÄæÄѶČÖŠµČ£¬“šĢā×¢Ņā×¢Ņā׊ĻøÉóĢā£¬°ŃĪÕĢāøųŠÅĻ¢£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ņŗ¾§Ģ¬½éÓŚ¾§ĢåדĢ¬ŗĶŅŗĢ¬Ö®¼ä£¬Ņŗ¾§¾ßÓŠŅ»¶Ø³Ģ¶ČµÄ¾§ĢåµÄÓŠŠņŠŌŗĶŅŗĢåµÄĮ÷¶ÆŠŌ | |
| B£® | ³£Ń¹ĻĀ£¬0”ꏱ±łµÄĆܶȱČĖ®µÄĆܶȊ”£¬Ė®ŌŚ4”ꏱĆܶČ×ī“ó£¬ÕāŠ©¶¼Óė·Ö×Ó¼äµÄĒā¼üÓŠ¹Ų | |
| C£® | ŹÆÓĶĮŃ½ā”¢ĆŗµÄøÉĮó”¢ÓńĆ×ÖĘ“¼”¢µ°°×ÖŹµÄ±äŠŌŗĶÄÉĆ×ŅųĮ£×ӵľŪ¼Æ¶¼ŹĒ»Æѧ±ä»Æ | |
| D£® | Č¼ĮĻµÄĶŃĮņĶѵŖ”¢SO2µÄ»ŲŹÕĄūÓĆŗĶNOxµÄ“ß»Æ×Ŗ»Æ¶¼ŹĒ¼õÉŁĖįÓź²śÉśµÄ“ėŹ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £®
£®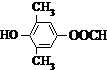 »ņ
»ņ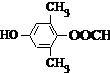 £®
£®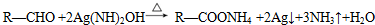 £®
£®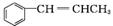 ĪŖŌĮĻÖʱø
ĪŖŌĮĻÖʱø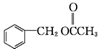 µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼ČēĻĀ£¬ŹŌŌŚ·½æņÄŚ²¹³äÓŠ»śĪļµÄ½į¹¹¼ņŹ½£ŗ
µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼ČēĻĀ£¬ŹŌŌŚ·½æņÄŚ²¹³äÓŠ»śĪļµÄ½į¹¹¼ņŹ½£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

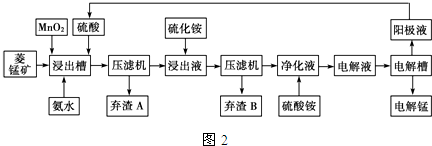
| ĪļÖŹ | Fe£ØOH£©2 | Ni£ØOH£©2 | Co£ØOH£©2 | Mn£ØOH£©2 | Fe£ØOH£©3 |
| æŖŹ¼³ĮµķpH | 7.5 | 7.7 | 7.6 | 8.3 | 2.7 |
| ĶźČ«³ĮµķpH | 9.7 | 8.4 | 8.2 | 9.8 | 3.8 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®| µēøŗŠŌ | ČŪ·Šµć | ĪČ¶ØŠŌ | ĖįŠŌ |
| O£¾N | NH3£¾PH3 | Fe2+£¼ Fe3+ | H3PO4£¼HNO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HClO2”śClO2+Cl2+H2O£ØĪ“ÅäĘ½£©£¬1 mol HClO2·Ö½āŹ±×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ1 mol | |
| B£® | ±ź×¼×“æöĻĀ£¬14 g CO”¢C2H4»ģŗĻĘųĢåÓė11.2 L N2Ėłŗ¬ÓŠµÄ·Ö×ÓŹż¶¼ŹĒ0.5NA | |
| C£® | Óė½šŹōCu³£ĪĀĻĀ·“Ó¦·Å³öĘųĢåµÄČÜŅŗæÉŅŌ“ęŌŚµÄĄė×ÓÓŠ£ŗFe2+”¢Al3+”¢SO42-”¢K+ | |
| D£® | ŌŚČ¼ĆŗŹ±¼ÓČėŹŹĮæŹÆ»ŅŹÆ£¬æɼõÉŁSO2µÄÅÅ·Å£¬ĘäÖŠ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ2CaCO3+O2+2SO2$\frac{\underline{\;øßĪĀ\;}}{\;}$2CaSO3+2CO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶žŃõ»ÆĮņĶØČėĀČ»ÆĢśČÜŅŗ£ŗSO2+2Fe3++2H2O=SO42-+2Fe2++4H+ | |
| B£® | ĮņĖįĒāļ§ČÜŅŗÖŠµĪ¼ÓÉŁĮæNaOHČÜŅŗ£ŗH++NH4++2OH-=NH3•H2O+H2O | |
| C£® | ¼īŠŌĢõ¼žĻĀĀĮ·Ū»¹ŌNaNO2£ŗNO2-+2Al+3OH-+H2O=2AlO2-+NH3•H2O | |
| D£® | ŌŚĒæ¼īČÜŅŗÖŠ“ĪĀČĖįÄĘÓėFe£ØOH£©3·“Ӧɜ³ÉNa2FeO4£ŗ3ClO-+Fe£ØOH£©3=FeO42-+3Cl-+H2O+4H+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
 ¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢Z”¢WŌŚÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČēĶ¼£¬WŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒĘä×īÄŚ²ćµē×ÓŹżµÄ3±¶£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢Z”¢WŌŚÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČēĶ¼£¬WŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒĘä×īÄŚ²ćµē×ÓŹżµÄ3±¶£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©| A£® | Ō×Ó°ė¾¶£ŗY£¾Z£¾X | |
| B£® | ŗ¬YŌŖĖŲµÄŃĪČÜŅŗÓŠµÄĻŌĖįŠŌ£¬ÓŠµÄĻŌ¼īŠŌ | |
| C£® | ×ī¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ£ŗZ£¾W | |
| D£® | XÓėRµÄŗĖµēŗÉŹżĻą²ī24 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com