
”¾ĢāÄæ”æŅŃÖŖ·“Ó¦mX(g)+nY(g)![]() qZ(g)µÄ”÷H<0£¬m+n>q£¬ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ·“Ó¦“ļµ½Ę½ŗāŹ±£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
qZ(g)µÄ”÷H<0£¬m+n>q£¬ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ·“Ó¦“ļµ½Ę½ŗāŹ±£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. ĶØČėĻ”ÓŠĘųĢåŹ¹Ń¹ĒæŌö“ó£¬Ę½ŗā½«ÕżĻņŅʶÆ
B. Ōö¼ÓXµÄĪļÖŹµÄĮ棬YµÄ×Ŗ»ÆĀŹ½µµĶ
C. ½µµĶĪĀ¶Č£¬»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ±äŠ”
D. XµÄÕż·“Ó¦ĖŁĀŹŹĒYµÄÄę·“Ó¦ĖŁĀŹµÄm/n±¶
”¾“š°ø”æD
”¾½āĪö”æŹŌĢā·ÖĪö£ŗA£®ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠĶØČėĻ”ÓŠĘųĢå×ÜŃ¹Ōö“󣬷ÖŃ¹²»±ä£¬Ę½ŗā²»¶Æ£¬¹ŹA“ķĪó£»B£®Ōö¼ÓXµÄĮæ»įĢįøßYµÄ×Ŗ»ÆĀŹ£¬YµÄ×Ŗ»ÆĀŹŌö“󣬱¾Éķ×Ŗ»ÆĀŹ¼õŠ”£¬¹ŹB“ķĪó£»C£®·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬½µĪĀĘ½ŗāÕżĻņ½ųŠŠ£¬·“Ó¦Ē°ŗóĘųĢåĢå»ż¼õŠ”£¬¹ż³ĢÖŠĘųĢåÖŹĮæ²»±ä£¬»ģŗĻĘųĢåµÄĻą¶Ō·Ö×ÓÖŹĮæŌö“󣬹ŹC“ķĪó£»D£®ĖŁĀŹÖ®±ČµČÓŚ»Æѧ·½³ĢŹ½µÄĻµŹżÖ®±Č£¬v(X)Õż£ŗv(Y)Õż=m£ŗn£¬Ę½ŗāŹ±£¬XµÄÕż·“Ó¦ĖŁĀŹŹĒYµÄÄę·“Ó¦ĖŁĀŹµÄ![]() ±¶£¬¹ŹDÕżČ·£»¹ŹŃ”D”£
±¶£¬¹ŹDÕżČ·£»¹ŹŃ”D”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ50 mLĖįŹ½µĪ¶Ø¹ÜÖŠŹ¢ÓŠŃĪĖį£¬ŅŗĆęĒ”ŗĆŌŚa mLæĢ¶Č“¦£¬°Ń¹ÜÄŚŅŗĢåČ«²æ·ÅČėĮæĶ²ÄŚ£¬ĖłµĆŅŗĢåµÄĢå»żŅ»¶Ø (””””)
A. µČÓŚa mL B. µČÓŚ(50-a)mL C. “óÓŚ(50-a)mL D. “óÓŚa mL
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ50mlÅØH2SO4ČÜŅŗ£Ø×ćĮ棩֊¼ÓČė3.2gCu£¬ŌŚ¼ÓČČĢõ¼žĻĀ³ä·Ö·“Ó¦£ŗ
£Ø1£©·“Ó¦ĻūŗĵÄH2SO4µÄĪļÖŹµÄĮæŹĒ_____________Éś³ÉSO2µÄĢå»żĪŖ£Ø±ź×¼×“æöĻĀ£©____________mL£®
£Ø2£©ČōĢāøÉÖŠÅØĮņĖįµÄĪļÖŹµÄĮæÅضČĪŖamol/L£¬Ķ¶Čė×ćĮæµÄĶʬ¼ÓČČ£¬³ä·Ö·“Ó¦ŗ󣬱»»¹ŌµÄĮņĖįµÄĪļÖŹµÄĮæn£ØH2SO4£©____0.025amol£ØĢī”°µČÓŚ”±”¢”°“óÓŚ”±»ņ”°Š”ÓŚ”±£©£®
£Ø3£©½«ĢāøÉÖŠ·“Ó¦ŗóµÄČÜŅŗĻ”ŹĶµ½500mL£¬Č”³ö50mL£¬²¢ĻņČ”³öŅŗÖŠ¼ÓČė×ćĮæµÄBaCl2ČÜŅŗ£¬µĆµ½³Įµķ19.81g£¬ŌņŌÅØĮņĖįµÄĪļÖŹµÄĮæÅضČĪŖ_____________£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
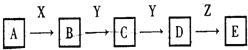
”¾ĢāÄæ”æĻĀĮŠ¹ŲĻµĶ¼ÖŠ£¬AŹĒŅ»ÖÖÕżŃĪ£¬DµÄĻą¶Ō·Ö×ÓÖŹĮæ±ČCµÄĻą¶Ō·Ö×ÓÖŹĮæ“ó16£¬EŹĒĖį£®µ±XĪŽĀŪŹĒĒæĖį»¹ŹĒĒæ¼īŹ±£¬¶¼ÓŠČēĻĀ×Ŗ»Æ¹ŲĻµ£ŗµ±XŹĒĒæĖįŹ±£¬A”¢B”¢C”¢D”¢E¾łŗ¬ÓŠĶ¬Ņ»ŌŖĖŲ£ŗµ±XŹĒĒæ¼īŹ±£¬A”¢B”¢C”¢D”¢E¾łŗ¬ÓŠĮķŅ»ÖÖŌŖĖŲ£®»Ų“šĻĀĮŠĪŹĢā£ŗ
Ēė»Ų“š£ŗ
(1)AŹĒ________£¬YŹĒ________£¬ZŹĒ________”£
(2)µ±XŹĒĒæĖįŹ±£¬EŹĒ________£¬Š“³öBÉś³ÉCµÄ»Æѧ·½³ĢŹ½£ŗ__________________________________________________________”£
(3)µ±XŹĒĒæ¼īŹ±£¬EŹĒ________£¬Š“³öBÉś³ÉCµÄ»Æѧ·½³ĢŹ½£ŗ _________________________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©ĻĀĮŠĪļÖŹÖŠ£¬ŹōÓŚĒæµē½āÖŹµÄŹĒ£ØĢīŠņŗÅ£¬ĻĀĶ¬£©__________£¬ŹōÓŚČõµē½āÖŹµÄŹĒ________£¬ŹōÓŚ·Ēµē½āÖŹ_____________£»
¢Ł°±Ęų ¢Ś°±Ė® ¢ŪŃĪĖį ¢Ü“×Ėį ¢ŻĮņĖį±µ ¢ŽĀČ»ÆŅų ¢ßĀČ»ÆÄĘ ¢ą¶žŃõ»ÆĢ¼ ¢į“×Ėįļ§ ¢āĒāĘų
£Ø2£©ĻõĖįĒ¦µÄĻ”ČÜŅŗÖŠ£¬µĪČė¼øµĪĻ”Na2SO4Éś³É°×É«PbSO4³Įµķ£¬ŌŁµĪČėŹżµĪ±„ŗĶ“×ĖįÄĘČÜŅŗ£¬Ī¢ČČ£¬²¢²»¶Ļ½Į¶Æ£¬³ĮµķĀżĀżČܽā£»ĒėŠ“³ö³ĮµķČܽā¹ż³ĢµÄĄė×Ó·½³ĢŹ½_____________£»
£Ø3£©ŅŃÖŖ25”ꏱ£¬H2C2O4µÄµēĄėĘ½ŗā³£ŹżĪŖK1=5.0”Į10-2£¬K2=5.4”Į10-5£»H3PO4µÄµēĄėĘ½ŗā³£ŹżĪŖ K1=7.52”Į10-3 ,K2=6.23”Į10-8, K3=2.2”Į10-13”£ĒėŠ“³öÉŁĮæH3PO4Óė¹żĮæNa2C2O4·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ__________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
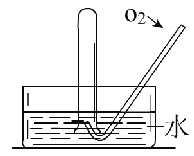
”¾ĢāÄæ”æČēĶ¼ĖłŹ¾£¬½«Ņ»Ęæ³äĀśNO2ĘųĢåµÄŹŌ¹Üµ¹æŪŌŚĖ®²ŪÖŠ£¬ĘųĢåŃÕÉ«ÓÉ____Öš½„±äĪŖ____É«£¬ŹŌ¹ÜÄŚµÄŅŗĆę»įÖš½„_____________£»µ±·“Ó¦Ķ£Ö¹ŗóĻņŹŌ¹ÜÖŠ»ŗĀżĶØČėŃõĘų£¬ĘųĢåŃÕÉ«ÓÖÓÉ______É«Öš½„±äĪŖ______É«£¬Ö®ŗóÓÖ±äĪŖ______É«£¬ŹŌ¹ÜÄŚµÄŅŗĆę»į____________”£ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾ŹŌ¹ÜÖŠ·¢ÉśµÄ»Æѧ·“Ó¦_____________£¬____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠŠšŹöÖŠŅ»¶ØÕżČ·µÄŹĒ
A. Ņ»¶ØĢõ¼žĻĀijĆܱÕČŻĘ÷Ź¢2 mol N2Óė3 mol H2·“Ӧɜ³ÉµÄNH3·Ö×ÓŹżĪŖ2NA
B. 25 ”ꏱ£¬Ksp(BaSO4)£½1”Į10£10£¬ŌņBaSO4±„ŗĶČÜŅŗÖŠBa2£«ŹżÄæĪŖ1”Į10£5NA
C. Ņ»¶ØĢõ¼žĻĀ4.6g NaĶźČ«ÓėO2·“Ӧɜ³É7.2 g²śĪļ£¬Ź§Č„µÄµē×ÓŹżĪŖ0.2NA
D. 1 L 0.1mol”¤L£1µÄNaHCO3ČÜŅŗÖŠHCO![]() ŗĶCO
ŗĶCO![]() µÄĄė×ÓŹżÖ®ŗĶĪŖ0.1NA
µÄĄė×ÓŹżÖ®ŗĶĪŖ0.1NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚČŻ»żĪŖ1 LµÄĆܱÕČŻĘ÷ÖŠ£¬¼ÓČė1.0 mol AŗĶ2.2 mol B½ųŠŠČēĻĀ·“Ó¦£ŗA(g) £« 2B(g) ![]() C(g) £« D(g)£¬ŌŚ800”ꏱ£¬DµÄĪļÖŹµÄĮæn(D)ŗĶŹ±¼ätµÄ¹ŲĻµČēĶ¼”£
C(g) £« D(g)£¬ŌŚ800”ꏱ£¬DµÄĪļÖŹµÄĮæn(D)ŗĶŹ±¼ätµÄ¹ŲĻµČēĶ¼”£
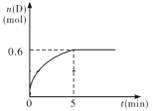
£Ø1£©800”ꏱ£¬0”«5 minÄŚ£¬ŅŌB±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ____________”£
£Ø2£©ĄūÓĆĶ¼ÖŠŹż¾Ż¼ĘĖćŌŚ800 ”ꏱµÄĘ½ŗā³£ŹżµÄŹżÖµĪŖ___________”£
£Ø3£©Čō700”ę£¬·“Ó¦“ļĘ½ŗāŹ±£¬AµÄÅضČĪŖ0.55mol/L£¬ŌņøĆ·“Ó¦ĪŖ_________·“Ó¦(Ģī”°ĪüČČ”±»ņ”°·ÅČČ”±)”£
£Ø4£©800 ”ꏱ£¬Ä³Ź±æĢ²āµĆĢåĻµÖŠĪļÖŹµÄĮæÅضČČēĻĀ£ŗc(A)£½0.06 mol”¤L£1£¬c(B)£½0.50 mol”¤L£1£¬c(C)£½0.20 mol”¤L£1£¬c(D)£½0.018 mol”¤L£1£¬Ōņ“ĖŹ±øĆ·“Ó¦______________(Ģī”°ĻņÕż·½Ļņ½ųŠŠ”±”¢”°ĻņÄę·½Ļņ½ųŠŠ”±»ņ”°“¦ÓŚĘ½ŗāדĢ¬”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©½«µČĢå»żµČĪļÖŹµÄĮæÅØ¶ČµÄ“×ĖįŗĶĒāŃõ»ÆÄĘČÜŅŗ»ģŗĻŗó£¬ČÜŅŗ³Ź £ØĢī”°ĖįŠŌ”±”¢”°ÖŠŠŌ”±»ņ”°¼īŠŌ”±£¬ĻĀĶ¬£©£¬ČÜŅŗÖŠc(Na+) c(CH3COO--)£ØĢī”°£¾”±”¢”°£½”±»ņ”°£¼”±£¬ĻĀĶ¬£©”£
£Ø2£©ĪļÖŹµÄĮæÅضČĻąĶ¬µÄ“×ĖįŗĶĒāŃõ»ÆÄĘČÜŅŗ»ģŗĻŗó£¬ČÜŅŗÖŠc(Na+) = c(CH3COO--)£¬Ōņ»ģŗĻŗóČÜŅŗ³Ź £¬“×ĖįĢå»ż ĒāŃõ»ÆÄĘČÜŅŗĢå»ż”£
£Ø3£©³£ĪĀĻĀ£¬pH£½3µÄ“×ĖįŗĶpH£½11µÄĒāŃõ»ÆÄĘČÜŅŗµČĢå»ż»ģŗĻŗóČÜŅŗ³Ź £¬ČÜŅŗÖŠc(Na+) c(CH3COO--)”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com