
下列实验能达到目的的是
A.用浓FeCl3溶液和NaOH溶液混合制备Fe(OH)3胶体
B.将混有少量HCl的CO2通入饱和NaHCO3溶液中除去HCl
C.用湿润的pH试纸测定等浓度的Na2CO3和Na2SO3 溶液的pH大小
D.用AgNO3溶液鉴别Na2SO4溶液与NaCl溶液
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源:2015届陕西省宝鸡市岐山县高三上学期期中考试化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写不正确的是
A.Cl2与NaOH溶液反应:Cl2+2OH-===Cl-+ClO-+H2O
B.澄清石灰水与少量苏打溶液混合:Ca2+ + OH-+ HCO3-=== CaCO3↓ + H2O
C.碳酸钙溶于盐酸:CaCO3 + 2H+ === Ca2+ + CO2↑ + H2O
D.氯化亚铁溶液中通入氯气:2Fe2+ + Cl2 === 2Fe3+ + 2Cl-
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高二上学期期中考试化学试卷(解析版) 题型:选择题
在等物质的量浓度的两种弱酸的钠盐(NaR、NaR′)溶液中分别通入适量的CO2,发生如下反应:NaR+CO2+H2O=HR+NaHCO3,2NaR′+CO2+H2O=2HR′+ Na2CO3。现有物质的量浓度相同的四种溶液:①HR②HR′③NaR④NaR′,由水电离出c(OH-)大小顺序是
A.①>②>③>④ B.②>①>④>③
C.③>④>①>② D.④>③>②>①
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高一上学期期中考试化学试卷(解析版) 题型:填空题
(12分)(1)30%的H2SO4和50%的H2SO4等质量混合后,所得溶液的质量分数________(填“大于”、“小于”或“等于”)40%,如果等体积混合,混合后溶液的质量分数________(填“大于”、“小于”或“等于”)40%。
(2)已知98%的浓H2SO4的物质的量浓度为18.4 mol·L-1,试判断49%的H2SO4的物质的量浓度________(填“大于”、“小于”或“等于”)9.2 mol·L-1。
(3)在一定温度和压强下,1体积X2(g)和3体积Y2(g)化合生成2体积Z(g),则Z气体的化学式是________ 。
(4)在标准状况下,CO和CO2的混合气体质量为36 g,体积为22.4 L,则CO所占的体积是__________ L,质量是________ g。
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高一上学期期中考试化学试卷(解析版) 题型:选择题
医学上对血液中毒最常用的净化手段是血液透析。透析时,病人的血液通过浸在透析液中的透析膜进行循环和透析。血液中的蛋白质和血细胞不能透过透析膜,血液内的毒性物质则可以透过,由此可以判断
A.蛋白质、血细胞不溶于水,毒性物质可溶于水
B.蛋白质以分子形式存在,毒性物质以离子形式存在
C.蛋白质、血细胞的粒子直径大于毒性物质的粒子直径
D.蛋白质、血细胞不能透过滤纸,毒性物质能透过滤纸
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高三上学期10月月考试卷(解析版) 题型:选择题
XSO4溶液与NaOH溶液反应,可生成X3(OH)4SO4沉淀和Na2SO4溶液,现有V1mL0.1mol/L XSO4溶液和V2mL 0.2mol/L NaOH溶液(V1+V2=50),为了使沉淀的质量达到最大值,V1和V2的取值应为 ( )
A.V1=30,V2=20 B.V1=20,V2=30 C.V1=10,V2=40 D.V1=15,V2=35
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省大连市高三10月月考理综化学试卷(解析版) 题型:实验题
甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。
操作 | 现象 |
通入氯气至过量
| I.A中溶液变红 II.稍后,溶液由红色变为黄色 |
(1)B中反应的离子方程式是 。
(2)A中溶液变红的原因是 。
(3)为了探究现象II的原因,甲同学进行如下实验。
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在 。
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象II的原因是SCN—与Cl2发生了反应。
(4)甲同学猜想SCN—可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN—的电子式为 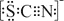 。
。
①甲同学认为SCN—中碳元素没有被氧化,理由是 。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN—中被氧化的元素是 。
③通过实验证明了SCN- 中氮元素转化为NO3-,他的实验方案是 。
④若SCN—与Cl2反应生成1 mol CO2,则转移电子的物质的量是 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com