
【题目】分子式为C4H10O且不能被催化氧化为醛的有机物有( )
A. 3种B. 4种C. 5种D. 6种
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。回答下列问题:
(1)联氨分子的电子式为 ,其中氮的化合价为 。
(2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为 。
(3)①2O2(g)+N2(g)==N2O4(l) △H1
②N2(g)+2H2(g)==N2H4(l) △H2
③O2(g)+2H2(g)==2H2O(g) △H3
④2N2H4(l)+N2O4(l)==3N2(g)+4H2O(g) △H4=-1048.9kJ-mol-1
上述反应热效应之间的关系式为△H4= ,联氨和N2O4可作为火箭推进剂的主要原因为 。
(4)联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步电离反应的平衡常数值为 (已知:N2H4+H+![]() N2H5+的K=8.7xl07; Kw=1.0xl0-14)。联氨与硫酸形成的酸式盐的化学式为 。
N2H5+的K=8.7xl07; Kw=1.0xl0-14)。联氨与硫酸形成的酸式盐的化学式为 。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是 。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2 kg;与使用Na2S03处理水中溶解的O2相比,联氨的优点是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是
A. 标准状况下,2.24LCCl4含有的共价键数为0.42NA
B. 氢原子数为0.4NA的甲醇分子中含有的键数为0.4NA
C. 1![]() Fe溶于过量硝酸,电子转移数为2NA
Fe溶于过量硝酸,电子转移数为2NA
D. 14![]() 乙烯和丙烯混合气体中的氢原子数为2NA
乙烯和丙烯混合气体中的氢原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见化合物DA2和DA3;工业上电解熔融C2A3制取单质C;B、E除最外层均只有2个电子外,其余各层全充满。回答下列问题:
(1)B、C中第一电离能较大的是______________(填元素符号),基态D原子价电子的轨道表达式为______________。
(2)DA2分子的VSEPR模型是______________。H2A比H2D熔沸点高得多的原因是______________。

(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6 在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。
①C2Cl6属于______________晶体(填晶体类型),其中C原子的杂化轨道类型为______________杂化。
②[C(OH)4]-中存在的化学键有______________。
(4)工业上制备B的单质是电解熔融B的氯化物,而不是电解BA,原因是__________。

(5)B、C的氟化物晶格能分别是2957kJ·mol-1、5492kJ·mol-1,二者相差很大的原因是______________。
(6)D与E所形成化合物晶体的晶胞如右图所示。
①在该晶胞中,E的配位数为____________。
②原子坐标参数可表示晶胞内部各原子的相对位置。右图晶胞中,原子坐标参数a为(0,0,0);b为(![]() ,0,
,0,![]() );c为(
);c为(![]() ,
,![]() ,0)。则d原子(面心上)的坐标参数为______________。
,0)。则d原子(面心上)的坐标参数为______________。
③已知该晶胞的密度为ρg/cm3,则其中两个D原子之间的距离为______________pm(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)水溶液中的离子平衡是中学化学的重要知识。
①25℃时,Na2CO3溶液呈碱性,原因是___________水解引起的(填“Na+”或“CO32-”);升高温度可以__________(填“促进”或“抑制”)Na2CO3的水解;
②常温下,pH=2的盐酸,该溶液中c( HCl )= _________________ mol/L;
(2)12g碳与适量水蒸气反应生成CO和H2,需吸收131.3kJ热量,此反应的热化学方程式为_____________________(填字母代号)。
A.C + H2O == CO + H2 ΔH= +131.3 kJ·mol-1
B. C(s)+ H2O(g) == CO(g) + H2(g) ΔH= +10.94 kJ·mol-1
C. C(s)+ H2O(g) == CO(g) + H2(g) ΔH= +131.3 kJ·mol-1
体积为1 L的容恒密闭容器中,充入1.00 mol CO2和3.00 mol H2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.00 kJ·mol-1
CH3OH(g)+H2O(g) ΔH=-49.00 kJ·mol-1
测得CO2和CH3OH(g)的浓度随时间变化如下图所示。
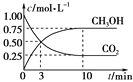
①从反应开始到平衡,二氧化碳的平均反应速率v(CO2)=______mol·(L·min)-1;
②该反应的平衡常数的表达式K= ___________________________;
③能说明该反应达到化学平衡状态的是__________(填字母代号);
A.c(CO2) = c(H2O) B.单位时间内消耗3mol H2,同时生成1mol CH3OH
C.容器内气体的压强不再变化
④下列措施中能使n(CH3OH)/n(CO2)增大的是________。
A.升高温度 B.将H2O(g)从体系中分离 C.再充入1.00 mol CO2
(4)下图是实验室电解精炼铜装置,
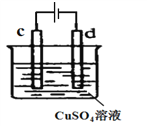
①d的电极材料为________________(填“粗铜”或“精铜”);
②c的电极反应方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pKa=lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。常温下,用0.1mol·L1NaOH溶液滴定20mL0.1mol·L1 H2SO3溶液的滴定曲线如下图所示(曲线上的数字为pH)。下列说法不正确的是( )

A. a点所得溶液中:2c(H2SO3)+c(SO32-)=0.1mol·L1
B. b点所得溶液中:c(H2SO3)+c(H+)=c(SO32-)+c(OH-)
C. c点所得溶液中:c(Na+)>3c(HSO3-)
D. d点所得溶液中:c(Na+)>c(SO32-)> c(HSO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2017·贵州省遵义市第四中学高一上学期期中考试)由NO和CO组成的混合气体与同温同压下空气的密度相等(空气的平均相对分子质量为29),下列关系正确的是
A.混合气体中,CO与NO质量比15∶14
B.混合气体中,CO与NO分子个数比1∶2
C.混合气体中,CO占有的体积大于NO占有的体积
D.混合气体中,CO与NO密度比14∶15
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硝酸银与氯化钾反应生成硝酸钾和不溶于水的氯化银,化学方程式为AgNO3+KCl=AgCl↓+KNO3。将含有少量氯化钾的硝酸钾固体提纯,某学生如图所示的实验操作。回答下列问题:

(1)将样品置于烧杯中,加入适量的水溶解,同时用玻璃棒搅拌,搅拌的作用是___________。
(2)向溶液中加入适量的________溶液,使氯化钾转化为沉淀。
(3)将混合液进行过滤,过滤装置和操作如图所示,指出图中的两处错误:①__________________;②______________________。
(4)为了从液体中得到硝酸钾晶体,可选用的两种结晶方法是:① __________________________ ;②______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com