
25℃ 时,水的离子积为Kw ,该温度下将 a mol ·L-盐酸 与b mol·L-1氨水等体积混合,若恰好完全反应,下列结论中不正确的是
A.混合液中:c(H+ ) ≤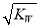
B.混合液中:c(NH3·H2O)+c(NH4+)=0.5a mol·L-1
C.a = b
D.混合液中:c(H+)+c(NH4+)= c(OH-)+c(Cl-)
科目:高中化学 来源:2015届青海省西宁市高三上学期第一次月考理综化学试卷(解析版) 题型:实验题
(15分)为了探究H2O2、H2SO3和Br2氧化性的相对强弱,设计如下实验(夹持仪器已略去)。请回答下列问题:

(1)仪器A的名称_________,其作用是___________。
(2)用仪器B滴加液体并不需要打开玻璃塞c,原因是____________________________。
(3)实验记录如下(请补全空白):
步骤 | 实验操作 | 实验现象 | 实验结论 |
Ⅰ | 打开活塞a,逐滴加入H2SO3溶液至过量 | ________________ | __________________________ |
Ⅱ | 向步骤Ⅰ所得溶液中逐滴加入H2O2溶液 | 刚开始溶液颜色无明显变化,继续滴加,溶液变为橙黄色 | __________________________ |
(4)步骤Ⅱ中,开始时颜色无明显变化的原因是(写出一条)_______________________,
步骤Ⅰ中反应的离子方程式_________________________________________________,
步骤Ⅱ中主要反应的离子方程式_____________________________________________。
查看答案和解析>>
科目:高中化学 来源:2015届陕西省高二下学期期末考试化学试卷(解析版) 题型:选择题
室温下,向20.00 mL 1.000 mol·L-1氨水中滴入1.000 mol·L-1盐酸,溶液pH和温度随加入盐酸体积变化曲线如图所示。下列有关说法错误的是

A.a、d两点的溶液,水的离子积Kw(a)>Kw(d)
B.将此氨水稀释,溶液的导电能力减弱
C.c点时消耗盐酸体积V(HCl)<20 mL
D.室温下,a点的氨水电离常数为 mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015届重庆市高三上期第一次月考理综化学试卷(解析版) 题型:选择题
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是
A.若M(甲)<M(乙),则气体的压强:甲>乙
B.若M(甲)>M(乙),则气体的摩尔体积:甲<乙
C.若M(甲)>M(乙),则气体体积:甲<乙
D.若M(甲)<M(乙),则分子数:甲<乙
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高二上学期期中考试化学试卷(解析版) 题型:填空题
以下是25 ℃时几种难溶电解质的溶解度:
难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些杂质离子。例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=a,过滤结晶即可。
请回答下列问题:
(1)上述三种除杂方案都能够达到很好的效果,Fe3+、Fe2+都被转化为 (填化学式)而除去。
(2)①中加入的试剂应该选择 为宜,其原因是 。
(3)②中除去Fe3+所发生的总反应的离子方程式为 。
(4)已知Fe(OH)3的Ksp=1×10-35mol4/L4 ;化学上通常认为残留在溶液中离子浓度小于1×10-5mol/L时,沉淀完全。方案③中a最小值为 .
(5)下列与方案③相关的叙述中,正确的是 (填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH=a可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=a的溶液中
E.在pH>a的溶液中Fe3+一定不能大量存在
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列物质中,不能和氯气发生取代反应的是
A.C8H18 B.C2H5Cl C.CH2Cl2 D.CCl4
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.物质的量浓度和体积都相同的盐酸和醋酸溶液,在与足量锌反应时,起始时二者产生H2速率基本相等
B.100 mL 1 mol·L-1的盐酸和50 mL 2 mol·L-1的盐酸,分别与足量的锌反应时,两者放出H2速率和质量均相等
C.100 mL pH=3的H2SO4和HCl溶液,与足量锌反应后,放出H2的质量相等
D.100 mL pH=3的盐酸与醋酸溶液,与足量锌反应后,所得H2的质量相等
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高一上学期期中考试化学试卷(解析版) 题型:选择题
某无色透明的溶液中,下列各组离子能大量共存的是
A.H+、Cl-、Ba2+、CO32- B.Ag+、I-、K+、NO3-
C.K+、OH-、Cl-、Na+ D.Fe3+、Cl-、NO3-、Na+
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省分校高三上学期期初考试化学试卷(解析版) 题型:填空题
(8分)在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
(1)某厂废水中含KCN,其浓度为650mg / L。现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2 → KOCN+2KCl+H2O 被氧化的元素是 。
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平虾类方程式,并标出电子转移数目:
KOSN+ KOH+ Cl2→ CO2+ N2+ KCl+ H2O
(3)若处理尚书废水20L,使KCN完成转化为无毒物质,至少需要液氯 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com