
分析 A、B、C、D为常见气态单质.
①A和B可以在放电条件下发生化合反应,其产物还可以与B化合生成红棕色气体,该红棕色气体为NO2,则A为氮气,B为氧气;
②C分别与N2、O2反应生成的两种化合物分子中都含有10个电子,则形成的化合物分别为NH3、H2O,所以C为H2;
③H2和D反应生成的化合物J易溶于水,在其溶液中滴加AgNO3溶液,生成白色沉淀,该化合物为HCl,则D为Cl2;然后根据各物质的性质分析.
解答 解:A、B、C、D为常见气态单质,①A和B可以在放电条件下发生化合反应,其产物还可以与B化合生成红棕色气体,该红棕色气体为NO2,则A为氮气,B为氧气;②C分别与N2、O2反应生成的两种化合物分子中都含有10个电子,则形成的化合物分别为NH3、H2O,所以C为H2;③H2和D反应生成的化合物J易溶于水,在其溶液中滴加AgNO3溶液,生成白色沉淀,该化合物为HCl,则D为Cl2,
(1)C和D反应生成的化合物为HCl,氯化氢分子中含有18个电子,1 molHCl分子中含有18mol电子,所含的电子数为18NNA,
故答案为:18;
(2)②中化合物为NH3、H2O,非金属性越强,对应氢化物稳定性越强,由于非金属性:N<O,则稳定性:H2O>NH3,
故答案为:H2O;NH3;
(3)D为氯气,B、C形成的化合物为H2O,氯气与水反应生成氯化氢和次氯酸,该反应的化学方程式为:Cl2+H2O=HCl+HClO,
故答案为:Cl2+H2O=HCl+HClO.
点评 本题考查无机推断,题目难度中等,涉及阿伏伽德罗常数的计算、元素周期律的应用及化学方程式书写等等再说,熟练掌握常见物质组成、性质为解答关键,试题培养了学生的分析、理解能力.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:解答题
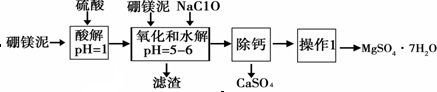
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
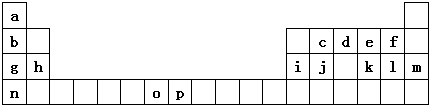
| 元素 | O | p | |
| 电离能 /kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | K+、CO32-、HS-、S2-、Al3+、AlO2- | B. | MnO4-、Na+、SO42-、K+、Cl- | ||
| C. | SO42-、Ag+、SO32-、S2-、AlO2-、K+ | D. | Fe3+、Cl-、H+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
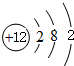 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .D在周期表中位置第三周期第ⅥA族.
.D在周期表中位置第三周期第ⅥA族. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 的不饱和度Ω为( )
的不饱和度Ω为( )| A. | 8 | B. | 7 | C. | 6 | D. | 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com