
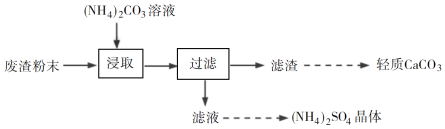
����Ŀ��ʵ�����Թ�ҵ��������Ҫ��CaSO4��2H2O����������SiO2��Al2O3��Fe2O3��Ϊԭ����ȡ����CaCO3��(NH4)2SO4���壬��ʵ���������£�
��1�������£���ӦCaSO4(s)+![]() (aq)
(aq)![]() CaCO3(s)+
CaCO3(s)+![]() (aq)�ﵽƽ�⣬����Һ��
(aq)�ﵽƽ�⣬����Һ�� =________[Ksp(CaSO4)=4.8��105��Ksp(CaCO3)=3��109]��
=________[Ksp(CaSO4)=4.8��105��Ksp(CaCO3)=3��109]��
��2������ˮ��NH4HCO3��Һ��ϣ����Ƶ�(NH4)2CO3��Һ�������ӷ���ʽΪ________����ȡ����ʱ����(NH4)2CO3��Һ�м�������Ũ��ˮ��Ŀ����________��
��3��������ȡ����ͼ��ʾ��װ���н��С����Ʒ�Ӧ�¶���60~70 �棬���裬��Ӧ3Сʱ���¶ȹ��߽��ᵼ��CaSO4��ת�����½�����ԭ����________�������¶ȡ���Ӧʱ�䡢��Ӧ����ܼ��������䣬ʵ�������CaSO4ת���ʵIJ�����________��

��4������ˮϴ���ಽ�����õ��Ʊ�����CaCO3�����CaCl2��Һ�������ˮϴ�������Ϊԭ�ϣ���ȡCaCl2��Һ��ʵ�鷽����______[��֪pH=5ʱFe(OH)3��Al(OH)3������ȫ��pH=8.5ʱAl(OH)3��ʼ�ܽ⡣ʵ���б���ʹ�õ��Լ��������Ca(OH)2]��
���𰸡�1.6��104 ![]() +NH3��H2O
+NH3��H2O![]()
![]() +
+![]() +H2O(��
+H2O(��![]() +NH3��H2O
+NH3��H2O![]()
![]() +
+![]() +H2O) ������Һ��
+H2O) ������Һ��![]() ��Ũ�ȣ��ٽ�CaSO4��ת�� �¶ȹ��ߣ�(NH4)2CO3�ֽ� �ӿ�������� �ڽ�����������ϡ�����з����������������۲첻�����ݲ������ˣ�����Һ�з�����������Ca(OH)2����pH��ֽ������ҺpH����pH����5~8.5ʱ������
��Ũ�ȣ��ٽ�CaSO4��ת�� �¶ȹ��ߣ�(NH4)2CO3�ֽ� �ӿ�������� �ڽ�����������ϡ�����з����������������۲첻�����ݲ������ˣ�����Һ�з�����������Ca(OH)2����pH��ֽ������ҺpH����pH����5~8.5ʱ������
��������
��1����ӦCaSO4��s��+CO32-��aq��![]() CaCO3��s��+SO42-��aq����ƽ�ⳣ������ʽΪ
CaCO3��s��+SO42-��aq����ƽ�ⳣ������ʽΪ![]() �����CaSO4��CaCO3��Ksp���㣻
�����CaSO4��CaCO3��Ksp���㣻
��2����ˮ��NH4HCO3��Ӧ���ɣ�NH4��2CO3�����백ˮ���ƣ�NH4��2CO3��ˮ�⣻
��3���¶ȹ��ߣ���NH4��2CO3�ֽ⣬ʹCaSO4ת�����½��������¶ȡ���Ӧʱ�䡢��Ӧ����ܼ��������䣬���CaSO4ת���ʼ���߷�Ӧ���ʣ���Ϸ�Ӧ���ص��Ӱ�췴Ӧ���ʵ����ط�����
��4�����ݹ�ҵ�����еijɷ�֪����ȡ�����˺����������к�CaCO3��SiO2��Al2O3��Fe2O3������ˮϴ�������Ϊԭ����ȡCaCl2��Һ����������Լ�������Ҫ�����������ὫCaCO3��ȫת��ΪCaCl2��ͬʱAl2O3��Fe2O3ת����AlCl3��FeCl3�����˳�ȥSiO2����������֪��������Ca��OH��2����pH��ȥAl3+��Fe3+��
��1����ӦCaSO4��s��+CO32-��aq��![]() CaCO3��s��+SO42-��aq���ﵽƽ��ʱ����Һ��
CaCO3��s��+SO42-��aq���ﵽƽ��ʱ����Һ��![]() =
=![]() =
=![]() =
=![]() =1.6��104���𰸣�1.6��104
=1.6��104���𰸣�1.6��104
��2��NH4HCO3������ʽ�Σ��백ˮ��Ӧ���ɣ�NH4��2CO3����Ӧ�Ļ�ѧ����ʽΪNH4HCO3+NH3��H2O=��NH4��2CO3+H2O[��NH4HCO3+NH3��H2O![]() ��NH4��2CO3+H2O]�����ӷ���ʽΪHCO3-+NH3��H2O=NH4++CO32-+H2O����HCO3-+NH3��H2O
��NH4��2CO3+H2O]�����ӷ���ʽΪHCO3-+NH3��H2O=NH4++CO32-+H2O����HCO3-+NH3��H2O![]() NH4++CO32-+H2O������ȡ����ʱ������ģ�NH4��2CO3�������������Σ���Һ�д���ˮ��ƽ�⣺CO32-+NH4++H2O
NH4++CO32-+H2O������ȡ����ʱ������ģ�NH4��2CO3�������������Σ���Һ�д���ˮ��ƽ�⣺CO32-+NH4++H2O![]() HCO3-+NH3��H2O����������Ũ��ˮ��ˮ��ƽ�������ƶ�����Һ��CO32-��Ũ������ӦCaSO4��s��+CO32-��aq��
HCO3-+NH3��H2O����������Ũ��ˮ��ˮ��ƽ�������ƶ�����Һ��CO32-��Ũ������ӦCaSO4��s��+CO32-��aq��![]() CaCO3��s��+SO42-��aq�������ƶ����ٽ�CaSO4��ת�����𰸣�HCO3-+NH3��H2O=NH4++CO32-+H2O����HCO3-+NH3��H2O
CaCO3��s��+SO42-��aq�������ƶ����ٽ�CaSO4��ת�����𰸣�HCO3-+NH3��H2O=NH4++CO32-+H2O����HCO3-+NH3��H2O![]() NH4++CO32-+H2O�� ������Һ��CO32-��Ũ�ȣ��ٽ�CaSO4��ת��
NH4++CO32-+H2O�� ������Һ��CO32-��Ũ�ȣ��ٽ�CaSO4��ת��
��3��������ξ��в��ȶ��ԣ������ֽ⣬�����¶ȹ��ߣ���NH4��2CO3�ֽ⣬�Ӷ�ʹCaSO4ת�����½������ڽ�ȡ�����еķ�Ӧ���ڹ�������Һ�ķ�Ӧ������������ת�����������¶ȡ���Ӧʱ�䡢��Ӧ����ܼ��������䣬���CaSO4ת���ʼ���߷�Ӧ���ʣ������������Ի�ѧ��Ӧ���ʵ�Ӱ�죬ʵ����������CaSO4ת���ʵIJ���Ϊ�ӿ�������ʣ�������Ӵ�������ӿ췴Ӧ���ʣ���߽�ȡ�ʣ����𰸣��¶ȹ��ߣ���NH4��2CO3�ֽ� �ӿ��������
��4����ҵ������Ҫ��CaSO4��2H2O������������SiO2��Al2O3��Fe2O3�����루NH4��2CO3��Һ��ȡ������CaSO4�루NH4��2CO3��Ӧ����CaCO3�ͣ�NH4��2SO4��SiO2��Al2O3��Fe2O3������Ӧ�����˺����������к�CaCO3��SiO2��Al2O3��Fe2O3������ˮϴ�������Ϊԭ����ȡCaCl2��Һ����������Լ�������Ҫ�����������ὫCaCO3��ȫת��ΪCaCl2�������ķ�ӦΪCaCO3+2HCl=CaCl2+H2O+CO2�������ͬʱ������ӦAl2O3+6HCl=2AlCl3+3H2O��Fe2O3+6HCl=2FeCl3+3H2O��SiO2����Ӧ�������˳�ȥSiO2���õ�����Һ�к�CaCl2��AlCl3��FeCl3��������pH=5ʱFe��OH��3��Al��OH��3������ȫ��pH=8.5ʱAl��OH��3��ʼ�ܽ�����Ϊ�˽���Һ��Al3+��Fe3+��ȫ��ȥ��Ӧ����Ca��OH��2������Һ��pH����5~8.5[����Ca��OH��2�Ĺ�����Ҫ�ӱ߲ⶨ��Һ��pH]��Ȼ����˼����Ƶ�CaCl2��Һ���𰸣��ڽ�����������ϡ�����з����������������۲첻�����ݲ������ˣ�����Һ�з�����������Ca��OH��2����pH��ֽ�����ҺpH����pH����5~8.5ʱ������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ϩ�� ������Ҫ���л�����ԭ�ϣ��㷺����ũҩ�������ϵ��������ش��������⣺
������Ҫ���л�����ԭ�ϣ��㷺����ũҩ�������ϵ��������ش��������⣺
��1����֪��![]() (g)=
(g)= ![]() (g)+H2(g) ��H1=100.3 kJ��mol 1 ��
(g)+H2(g) ��H1=100.3 kJ��mol 1 ��
H2(g)+ I2(g)=2HI(g) ��H2=��11.0 kJ��mol 1 ��
���ڷ�Ӧ��![]() (g)+ I2(g)=
(g)+ I2(g)=![]() (g)+2HI(g) �� ��H3=___________kJ��mol 1��
(g)+2HI(g) �� ��H3=___________kJ��mol 1��
��2��ij�¶��£������ʵ����ĵ�ͻ���ϩ��![]() ���ڸ��������ڷ�����Ӧ�ۣ���ʼ��ѹΪ105Pa��ƽ��ʱ��ѹ������20%������ϩ��ת����Ϊ_________���÷�Ӧ��ƽ�ⳣ��Kp=_________Pa���ﵽƽ��������ӻ���ϩ��ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��__________�����ţ���
���ڸ��������ڷ�����Ӧ�ۣ���ʼ��ѹΪ105Pa��ƽ��ʱ��ѹ������20%������ϩ��ת����Ϊ_________���÷�Ӧ��ƽ�ⳣ��Kp=_________Pa���ﵽƽ��������ӻ���ϩ��ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��__________�����ţ���
A��ͨ��������� B������¶�
C�����ӻ���ϩŨ�� D�����ӵ�Ũ��
��3�������ϩ�������ۺ����ɶ����壬�÷�ӦΪ���淴Ӧ����ͬ�¶��£���Һ�л����ϩŨ���뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ������˵����ȷ����__________�����ţ���

A��T1��T2
B��a��ķ�Ӧ����С��c��ķ�Ӧ����
C��a�������Ӧ���ʴ���b����淴Ӧ����
D��b��ʱ�������Ũ��Ϊ0.45 mol��L1
��4�������ϩ�������Ʊ���ï����Fe(C5H5)2�ṹ��ʽΪ �������߹㷺Ӧ���ں��졢�����������С���ï���ĵ绯ѧ�Ʊ�ԭ������ͼ��ʾ�����е��ҺΪ�ܽ����廯�ƣ�����ʣ��ͻ����ϩ��DMF��Һ��DMFΪ�����л��ܼ�����
�������߹㷺Ӧ���ں��졢�����������С���ï���ĵ绯ѧ�Ʊ�ԭ������ͼ��ʾ�����е��ҺΪ�ܽ����廯�ƣ�����ʣ��ͻ����ϩ��DMF��Һ��DMFΪ�����л��ܼ�����

�õ��ص�����Ϊ____________���ܷ�ӦΪ__________________������Ʊ���Ҫ����ˮ�����½��У�ԭ��Ϊ_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л�������C��H��O����Ԫ�أ���������ͼ��ʾ����4.3 g���л�����O2�г��ȼ�գ�ʹ����������ͨ������Ũ����ͼ�ʯ�ң�Ũ��������2.7 g����ʯ������8.8 g������

��1�����л�����Ħ������Ϊ____________g/mol��
��2�����л����ķ���ʽΪ ��
��3��1mol���л����������Ľ����Ʒ�Ӧ����1mol�������˴Ź��������������壬�������Ϊ2��1����д����ṹ��ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Y���п������������ã�����X�Ƶá�

�����йػ�����X��Y��˵����ȷ����
A. 1 mol X�������2 mol NaOH��Ӧ
B. Y���Ҵ�����������Ӧ�ɵõ�X
C. X��Y����������KMnO4��Һ��Ӧ
D. ������X��Y�ֱ�������Br2�ӳɵIJ������������̼ԭ����Ŀ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�����ᴿ��ʵ���У���ѡ�õķ�������������ȷ���ǣ�������
��� | A | B | C | D |
ʵ��Ŀ�� | ����ʳ��ˮ����ɳ | ����ˮ��CCl4 | ��ȡ����ˮ | ��Ũʳ��ˮ�еõ��Ȼ��ƾ��� |
���뷽�� | ���� | ��ȡ | ���� | ���� |
ѡ������ |
|
|
|
|
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��Ŵ��Ͷ����������������л����˷ḻ�ľ��飬�ܶ��������̵IJ��������뻯ѧʵ���е����ʷ�����ӷ������ơ����м������غŵ��������Ӧ���뷽����ȷ���ǣ�������
�����ݼ���ע�� | ��ͨ����¼�� | ����ҽ��¼�� | �������帮־�� |
����ҩ�ƣ�����ϸ������������� | ��½ȡ±����ɹ�����������±ˮ���� | ��������������С����������ȡҺ | ���»�����֮�������˵þƿ��� |
|
|
|
|
A.���ˡ�������ȡ������B.���ˡ���������ȡ������
C.��������ȡ��������D.��ȡ�����������ˡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���۲�����ʵ��װ��ͼ����Ҫ������

��1��д��ͼ��ʵ����������ƣ���_____ ��_____
��2��װ���������в������������ƣ�_____��_____
��3������ʵ����Ҫ������װ���н��У�������ţ�ÿ��װ�ý�ʹ��һ�Σ�
�� KCl��Һ�л�ȡKCl����_____���Ӻ�ˮ����ȡˮ_____������CaCO3��ˮ_____������ֲ���ͺ�ˮ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������Ṥҵ�Ļ�����������Pt���������·�������Ӧ�����Ӧ��
��.4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ��H1=-905 kJ/mol
4NO(g)+6H2O(g) ��H1=-905 kJ/mol
��.4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) ��H2
2N2(g)+6H2O(g) ��H2
��1����֪��
�����ж���1mol��ѧ����Ҫ������/kJ | NO | O2 | N2 |
629 | 496 | 942 |
���H2=___________��
��2����PtΪ��������1L�ܱ������г���1mol NH3��2mol O2������й����ʵ������¶ȵĹ�ϵ����ͼ��

�ٸô����ڸ���ʱ�Է�Ӧ__________�������������
��520��ʱ��NH3��ת����Ϊ____________��
��520��ʱ����Ӧ���ƽ�ⳣ��K=________�����ּ���ʽ����
������˵����ȷ����____________�����ţ���
A ��ҵ�ϰ�����������NOʱ������¶�Ӧ������840������
B ����NH3��O2�ij�ʼͶ�ϱȿ������NH3����NO��ƽ��ת����
C Ͷ�ϱȲ��䣬���ӷ�Ӧ���Ũ�ȿ������NH3����NO��ƽ��ת����
D ʹ�ô���ʱ���ɽ��ͷ�Ӧ�Ļ�ܣ��ӿ��䷴Ӧ����
���¶ȸ���840��ʱ��NO�����ʵ������ٵ�ԭ�������____________��
��3�������������£����ʹ���M�ܴ�NH3��NOx��Ӧ����N2��
��NH3��NO2����N2�ķ�Ӧ�У�������1mol N2ʱ��ת�Ƶĵ�����Ϊ___________mol��
�ڽ�һ��������O2��NH3��NOx�Ļ�����壬����ͨ��װ�д����ķ�Ӧ���з�Ӧ��
��Ӧ��ͬʱ��NOx��ȥ�����淴Ӧ�¶ȵı仯��������ͼ��ʾ����50-250�淶Χ�������¶ȵ����ߣ�NOx��ȥ������Ѹ��������������������Ҫԭ����_______________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���Y(��������������������)���п����������������ã����ɻ�����X��һ�������ºϳɣ�

����˵����ȷ����(����)
A. X����������ԭ��һ����ͬһƽ����
B. X��Y�����о�����1������̼ԭ��
C. 1molX����ˮ��ַ�Ӧ���������Br2�����ʵ���Ϊ2mol
D. 1molY��NaOH��Һ��ַ�Ӧ���������NaOH�����ʵ���Ϊ4mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com