
| A、80g硝酸铵(NH4NO3)含有氮原子数为2NA |
| B、1L1mol?L-1的盐酸溶液中,所含氯化氢分子数为NA |
| C、标准状况下,11.2L酒精(C2H5OH)所含分子数为0.5NA |
| D、在钠与氯气的反应中,1mol钠失去的电子数为2 NA |
| m |
| M |
| 80g |
| 80g/mol |


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
| 5 |
| 4 |
| 1 |
| 4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol/L甲酸溶液中c(H+)约为1×10-2mol/L |
| B、甲酸能与水以任意比互溶 |
| C、10mL 1mol/L甲酸恰好跟10 mL 1mol/L NaOH溶液完全反应 |
| D、甲酸的导电性比强酸溶液的导电性弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 强电解质 | HCl | FeCl3 | H3PO4 | HClO |
| 弱电解质 | HF | CH3COOH | BaSO4 | Ba(OH)2 |
| 非电解质 | NH3 | Cu | H2O | C2H5OH |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳的燃烧热大于110.5 kJ/mol |
| B、①的反应热为221 kJ/mol |
| C、稀硫酸与稀NaOH溶液反应的中和热为114.6 kJ/mol |
| D、稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
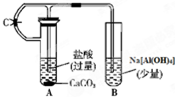 根据如图所示装置,请回答:
根据如图所示装置,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com