
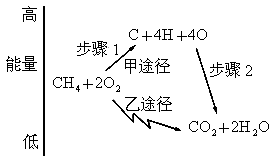
图是甲烷与氧气反应生成二氧化碳和水的两种可能途径.甲途径中,先
经由步骤1,甲烷和氧气分子间的共价键断裂,成为C、H及O三种原子,这三种原子再经由步骤2,形成二氧化碳和水.试问:(1)步骤1和步骤2分别是吸热反应还是放热反应?______________.
(2)若经由乙途径也可使甲烷与氧气反应最终生成二氧化碳与水,则其总反应为吸热反应还是放热反应?______________.
科目:高中化学 来源: 题型:
 氮的氧化物和SO2是常见的化工原料,但也是大气的主要污染物.综合治理其污染是化学家研究的主要内容.根据题意完成下列各题:
氮的氧化物和SO2是常见的化工原料,但也是大气的主要污染物.综合治理其污染是化学家研究的主要内容.根据题意完成下列各题:
| ||
查看答案和解析>>
科目:高中化学 来源:上海市十三校2012届高三第二次联考化学试题 题型:022
氮的氧化物和SO2是常见的化工原料,但也是大气的主要污染物.综合治理其污染是化学家研究的主要内容.根据题意完成下列各题:
1.用甲烷催化还原一氧化氮,可以消除一氧化氮对大气的污染.反应方程式如下:CH4(g)+4NO(g)![]() 2N2(g)+2H2O(g)+CO2(g)该反应平衡常数表达式为________.
2N2(g)+2H2O(g)+CO2(g)该反应平衡常数表达式为________.
2.硫酸生产中,接触室内的反应:2SO2(g)+O2(g)![]() 2SO3(g);SO2的平衡转化率与体系总压强的关系如图所示.某温度下,将2.0 mol SO2和1.0 mol O2置于30 L刚性密闭容器中,30秒反应达平衡后,体系总压强为2.70MPa.用氧气表示该反应的平均速率是________mol·L-1·min-1.
2SO3(g);SO2的平衡转化率与体系总压强的关系如图所示.某温度下,将2.0 mol SO2和1.0 mol O2置于30 L刚性密闭容器中,30秒反应达平衡后,体系总压强为2.70MPa.用氧气表示该反应的平均速率是________mol·L-1·min-1.
3.下图平衡状态由A变到B时,改变的外界条件是________.

a.又加入一些催化剂
b.又加入一些氧气
c.降低了体系的温度
d.升高了外界的大气压
4.新型纳米材料氧缺位铁酸盐MFe2Ox在常温下,能将氮的氧化物和SO2等废气分解除去.转化流程如图所示,若x=3.5,M为Zn,请写出ZnFe2O3.5分解SO2的化学方程式________

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮的氧化物和SO2是常见的化工原料,但也是大气的主要污染物.综合治理其污染是化学家研究的主要内容.根据题意完成下列各题:
氮的氧化物和SO2是常见的化工原料,但也是大气的主要污染物.综合治理其污染是化学家研究的主要内容.根据题意完成下列各题: 2SO3(g);SO2的平衡转化率与体系总压强的关系如图1所示.某温度下,将2.0mol SO2和1.0mol O2置于30L刚性密闭容器中,30秒反应达平衡后,体系总压强为2.70MPa.用氧气表示该反应的平均速率是______mol?L-1?min-1.
2SO3(g);SO2的平衡转化率与体系总压强的关系如图1所示.某温度下,将2.0mol SO2和1.0mol O2置于30L刚性密闭容器中,30秒反应达平衡后,体系总压强为2.70MPa.用氧气表示该反应的平均速率是______mol?L-1?min-1.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com