
【题目】化学与资源利用、材料研制、环境保护等密切相关。
(1)海水中蕴含的元素有80多种。
①海水中镁的总储量约为1.8×1015t,海水里镁的存在形式是__(填“游离态”或“化合态”)。
②氯碱工业是重要的化学工业之一,写出该反应原理的离子方程式:__。
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善人类生活。
①铁和铝是两种常见的金属材料,在空气中铝比铁耐腐蚀的原因是__。
②新型陶瓷氮化铝可用氧化铝高温还原法制备,化学方程式如下,请配平该化学反应方程式并标出电子转移方向和数目。_________
Al2O3+C+N2![]() AlN+CO
AlN+CO
(3)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。
①写出二氧化硫与足量NaOH溶液反应的离子方程式:__。
②酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强。写出这一过程的化学方程式:__。
【答案】化合态 2Cl-+2H2O![]() 2OH-+H2 ↑+Cl2↑ 铝在空气中表面易形成氧化膜,,可以保护铝不会进一步被腐蚀
2OH-+H2 ↑+Cl2↑ 铝在空气中表面易形成氧化膜,,可以保护铝不会进一步被腐蚀  SO2+2OH-= SO32-+H2O 2H2SO3+O2=2H2SO4
SO2+2OH-= SO32-+H2O 2H2SO3+O2=2H2SO4
【解析】
⑴①海水里镁的存在形式是化合态;
②氯碱工业是电解饱和食盐水。
⑵①在空气中铝比铁耐腐蚀的原因是铝在空气中表面易形成氧化膜,可以保护铝不会进一步被腐蚀;
②新型陶瓷氮化铝可用氧化铝高温还原法制备,碳化合价升高2个,氮气化合价降低6个,根据得失电子守恒,配平并标出电子转移方向和数目;
⑶①二氧化硫与足量NaOH溶液反应生成亚硫酸根和水;
②酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸。
⑴①海水里镁的存在形式是化合态;
②氯碱工业是重要的化学工业之一,该反应原理的离子方程式:2Cl-+2H2O![]() 2OH-+H2 ↑+Cl2↑;
2OH-+H2 ↑+Cl2↑;
⑵①铁和铝是两种常见的金属材料,在空气中铝比铁耐腐蚀的原因是铝在空气中表面易形成氧化膜,可以保护铝不会进一步被腐蚀;
②该反应的电子转移方程式为: ;
;
⑶①二氧化硫与足量NaOH溶液反应生成亚硫酸根和水,其离子方程式:SO2 +2OH-=SO32-+H2O;
②酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,这一过程的化学方程式:2H2SO3+O2=2H2SO4。


科目:高中化学 来源: 题型:
【题目】氢原子是最轻的原子,人们曾预言它可能是所有元素之母。碳是地球上组成生命的最基本的 元素之一。按要求回答:
(1)宇宙中含量最多的元素是氢和______。基态碳原子的核外电子占有______个原子轨道。
(2)光化学烟雾中除了含有 NOx 外,还含有 HCOOH、![]() (PAN)等二次污染物。
(PAN)等二次污染物。
①PAN 中 C 的杂化方式有______。1mol PAN 中含有的σ键数目为______。组成PAN 的元素的电负性大小顺序为______。
②相同压强下,HCOOH 的沸点比 CH3OCH3______(填“高”或“低”),
(3)水溶液中有 H3O+、H5O2+ 、H9O4 + 等微粒的形式。请画出 H5O2 的结构式:______。
(4)硅和碳在同一主族。下图为 SiO2 晶胞中 Si 原子沿 z 轴方向在 xy 平面的投影图(即俯视图),其 中 O原子略去,Si 原子旁标注的数字表示每个 Si 原子位于 z 轴的高度,则 SiA 与 SiB 之间的距离是______nm。
 (d 的单位为 nm)
(d 的单位为 nm)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种短周期主族元素,前三种元素在周期表中的位置如图所示:
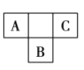
A、B、C三种元素中有两种元素的最高价氧化物对应的水化物是强酸,D元素的原子半径在短周期元素中最大,E是最高正价为![]() 的非金属元素。
的非金属元素。
(1)C在周期表中的位置是______
(2)A、B、C三种元素中两种元素所形成的两种强酸的分子式分别为______;上述五种元素形成的简单离子中,电子层结构相同的离子的半径由大到小的顺序为____________
(3)举例说明C的非金属性比B的非金属性强:____________
(4)D的单质与E所形成的最常见化合物能发生剧烈反应,写出相应的离子方程式:____________;A、E之间形成的最简单化合物(过量)与C的单质混合后可得到一种单质和一种盐,对应的化学方程式为____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有a~g7种短周期主族元素,它们在元素周期表中的相对位置如图所示,请回答下列问题:
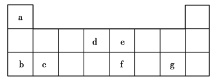
(1)下列选项中,元素的原子间最容易形成离子键的是______(填序号,下同),元素的原子间最容易形成共价键的是______。
A.![]() 和
和![]() B.
B.![]() 和
和![]() C.
C.![]() 和
和![]() D.
D.![]() 和
和![]()
(2)下列由a~g7种元素原子形成的各种分子中,所有原子最外层都满足8电子稳定结构的是______(填序号)。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(3)由题述元素中的3种非金属元素形成的AB型离子化合物的电子式为______。
(4)![]() 与
与![]() 可形成一种化合物
可形成一种化合物![]() ,其含有的化学键类型为______,其与过量稀盐酸反应的化学方程式为______。
,其含有的化学键类型为______,其与过量稀盐酸反应的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A与NaOH的醇溶液混合加热得产物C和溶液D。C与乙烯混合在催化剂作用下可反应生成 的高聚物。而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
的高聚物。而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
A. B.
B.
C.CH3CH2CH2ClD.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)填写表中空格:
符号 | 质子数 | 电子数 |
___ | 1 | 0 |
| ___ | ___ |
| ___ | b |
(2)元素周期表中第五周期共有___种元素,若第五周期ⅤA族元素的原子序数为![]() ,则第五周期ⅡA族元素的原子序数为___(用含
,则第五周期ⅡA族元素的原子序数为___(用含![]() 的代数式表示,下同),第六周期ⅤA族元素的原子序数为____。
的代数式表示,下同),第六周期ⅤA族元素的原子序数为____。
(3)紧邻第Ⅷ族之后的一个纵行为第____族,元素周期表中所含元素种数最多的族是第___族。
(4)某元素的一种同位素![]() 的原子的质量数为
的原子的质量数为![]() ,含
,含![]() 个中子,它与
个中子,它与![]() 原子组成
原子组成![]() 分子,则
分子,则![]()
![]()
![]() 中所含质子的物质的量是___
中所含质子的物质的量是___![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用微生物燃料电池原理,可以处理宇航员排出的粪便,同时得到电能。美国宇航局设计的方案是:用微生物中的芽孢杆菌来处理粪便产生氨气,氨气与氧气分别通入燃料电池两极,最终生成常见的无毒物质。示意图如下所示。下列说法错误的是( )
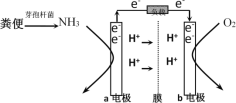
A.a电极是负极,b电极是正极
B.负极区发生的反应是2NH3 - 6e-=N2+6H+
C.正极区,每消耗标准状况下2.24 L O2,a向b电极转移0.4 mol电子
D.电池工作时电子通过由a经负载流向b电极,再穿过离子交换膜回到a电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的短周期主族元素。X分别与Y、Z、W结合形成质子数相同的甲、乙、丙三种分子。丁为无色气体,遇空气变红棕色;丙的水溶液可刻蚀玻璃。
上述物质有如图转化关系:
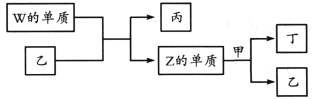
下列说法错误的是
A. 四种元素形成的单质中W的氧化性最强
B. 甲、乙、丙中沸点最高的是丙
C. 甲常用作致冷剂
D. 甲、乙分子均只含极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答:
(1)室温下,使用pH计测定0.1mol/LNH4Cl溶液的pH=5.12(如图1)由此可以得到的结论是___(填字母)。

a.NH3·H2O是弱碱
b.溶液中c(H+)>c(OH-)
c.NH4+水解是吸热反应
d.由H2O电离出的c(H+)<10-7mol/L
e.物质的量浓度相等的氨水和盐酸等体积混合,溶液pH=7
(2)室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的盐酸和醋酸,滴定曲线如图2所示。

①表示滴定盐酸的曲线是____(填序号)。若此实验选用酚酞为指示剂,则滴定到达终点的现象是____。若用标准NaOH溶液测定未知盐酸溶液的浓度,下列实验操作会使实验结果偏低的是____。
a.锥形瓶用待测液润洗后再注入待测液
b.碱式滴定管滴定前有气泡,滴定后无气泡
c.碱式滴定管滴定前仰视读数,滴定后平视读数
②在滴定醋酸溶液的过程中:
V(NaOH)=10.00mL时,溶液中离子浓度由大到小的顺序为____。当c(Na+)=c(CH3COO-)+c(CH3COOH)时,溶液pH____7(填“>”、“=”或“<”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com