
制烧碱所用盐水需两次精制。第一次精制主要是用沉淀法除去粗盐水中Ca2+、Mg2+、Fe3+、SO42-等离子,过程如下:
Ⅰ.向粗盐水中加入过量BaCl2溶液,过滤;
Ⅱ.向所得滤液中加入过量Na2CO3溶液,过滤;
Ⅲ.滤液用盐酸调节pH,获得一次精制盐水。
(1)过程Ⅰ、Ⅱ生成的部分沉淀及其溶解度(20℃/g)如下表:
| CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
①检测Fe3+是否除尽的方法是________________________________________。
②过程Ⅰ选用BaCl2而不选用CaCl2,运用表中数据解释原因____________________。
③检测Ca2+、Mg2+、Ba2+是否除尽时,只需检测_______(填离子符号)。
(2)第二次精制要除去微量的I-、IO3-、NH4+、Ca2+、Mg2+,流程示意如下:
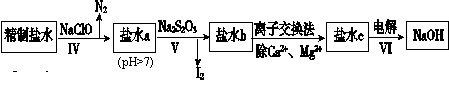

①过程Ⅳ除去的离子是________________。
②过程VI中,在电解槽的阴极区生成NaOH,结合化学平衡原理解释:___________。
科目:高中化学 来源: 题型:
下列对阿伏加德罗常数的叙述中,正确的是( )
①阿伏加德罗常数就是6.02×1023 mol-1
②阿伏加德罗常数为1 mol指定粒子的粒子数
③阿伏加德罗常数为12 g碳所含的碳原子数
④阿伏加德罗常数用符号NA表示,其值约为6.02×1023 mol-1
A.①② B.①③ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示装置是化学实验中常见的仪器,它除用于洗气外,还有其他用途:

(1)医院里给病人输氧时,往往在氧气钢瓶与病人呼吸面具之间安装盛有水的该装置,用 于观察气泡产生的情况,以便调节供氧速率, 此时氧气应从 (填标号,下同)管口导入。
(2)实验室用MnO2与浓HCl反应制Cl2的实验中,在将生成的Cl2通入NaOH溶液之前,先将Cl2从该装置 管口导入,此时,该装置所起的作用是防止NaOH溶液倒流入反应器。
(3) 当用此装置收集NO时,应采取的主要操作步骤是:
① ;
② 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:KClO3+C+S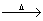 KCl+CO2 ↑+SO2↑,下列判断不正确的是
KCl+CO2 ↑+SO2↑,下列判断不正确的是
A.若反应中C和S的质量比为3:4,则n(KClO3):n(CO2)为1:1
B.若反应中C和S的质量比为3:16,则n(KClO3):n(CO2)为2:1
C.SO2通人NaHCO3溶液产生CO2,可证明非金属性S强于C
D.KClO3与SO2在强酸性溶液中反应制得ClO2,可证明SO2的还原性强于ClO2
查看答案和解析>>
科目:高中化学 来源: 题型:
水钴矿(含Cu0、C0203 ,Fe2O3、MgO等)用硫酸法浸出铜和钴,下图是不同还原剂对元素浸 出率的影响(硫酸浓度3 mol•L-1,温度60 0C),下列说法正确的是
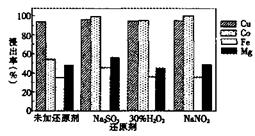 A. 是否使用还原剂对铜的浸出率影响很大
A. 是否使用还原剂对铜的浸出率影响很大
B. 用Na2SO3和NaNO2作还原剂,钴的浸出率均达98%。但工业上宜选用Na2SO3
C.加入还原剂的主要目的是为了还原Fe3+
D.用Na2SO3作还原剂可使镁元素以单质形式析出而有较大浸出率
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
A.制造水泥和普通玻璃的原料中都含有石灰石
B.普通玻璃是电的绝缘体,这种透明的固体物质熔点很低
C.石英玻璃能经受温度剧变且能抵抗酸碱的腐蚀
D.硅酸盐可用氧化物形式表示其组成,这表明硅酸盐是由氧化物组成的
查看答案和解析>>
科目:高中化学 来源: 题型:
钛(Ti)因为具有神奇的性能越来越引起人们的关注。常温下钛不和非金属、强酸反应。红热时,却可与常见的非金属单质反应。钛是航空、军工、电力等方面的必需原料。地壳中含钛矿石之一是金红石(TiO2),目前大规模生产钛的方法是:第一步:金红石、碳粉混合,在高温条件下通入Cl2制得TiCl4和一种可燃性气体,该反应的化学方程式为______________________________,该反应的还原剂是________。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)写出此反应的化学方程式:_____________________________________________。
(2)简述从上述所得产物中获取金属钛的步骤___________________________ _______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
⑴.将质量比为14 :15的N2和NO混合,则混合气体中N2和NO的物质的量之比为______,氮原子和氧原子的个数比为________。
⑵.同温同压下,质量相同的五种气体: ① CO2 ② H2 ③ O2 ④ CH4 ⑤ SO2
所占的体积由大到小的顺序是(填序号,下同)_________________;
密度由大到小的顺序是_________________________________。
⑶.VmL Al2(SO4)3溶液中含Al3+ ag,取V/4mL溶液稀释到VmL,则稀释后溶液中的SO42-的物质的量浓度是(单位为mol/L)______________。
⑷.有一质量为mg,相对分子质量为M的某种强碱M (OH)2,在一定温度下,完全溶解在水中得到VmL饱和溶液,若此溶液的密度为ρg/cm3,则该溶液中OH-的物质的量浓度为________,溶质的质量分数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com