
| n |
| V |
| 0.04mol |
| 0.1L |


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 减排是各个国家都在努力而为之的事,CO2和SO2的处理是许多科学家都在着力研究的重点.有学者想以下图所示装置用原电池原理将CO2、SO2转化为重要的化工原料.
减排是各个国家都在努力而为之的事,CO2和SO2的处理是许多科学家都在着力研究的重点.有学者想以下图所示装置用原电池原理将CO2、SO2转化为重要的化工原料.查看答案和解析>>
科目:高中化学 来源: 题型:
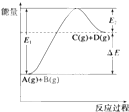 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,| A、⑤⑥⑦⑧ | B、①②③④ |
| C、①③⑤⑦ | D、②⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在氧气中比在空气中燃烧得更旺 |
| B、在氧气中火焰为明亮的蓝紫色 |
| C、在氧气中反应比在空气中反应速率快 |
| D、在氧气中燃烧比在空气中燃烧放出的热量多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com