
| A£® | µ±ČÜŅŗµÄpH=9Ź±£¬ČÜŅŗÖŠ“ęŌŚĻĀĮŠ¹ŲĻµ£ŗc£ØNH4+£©£¾c£ØHCO3-£©£¾c£ØNH3•H2O£©£¾c£ØCO32-£© | |
| B£® | NH4HCO3ČÜŅŗÖŠ“ęŌŚĻĀĮŠŹŲŗć¹ŲĻµ£ŗc£ØNH4+£©+c£ØNH3•H2O£©+c£ØH+£©=c£ØOH-£©+2c£ØCO32-£©+c£ØH2CO3£© | |
| C£® | ÓÉĶ¼æÉÖŖ£¬ĶłøĆČÜŅŗÖŠÖšµĪµĪ¼ÓĒāŃõ»ÆÄĘŹ±NH4+ÅضČÖš½„¼õŠ”£¬HCO3-ÅضČĻČŌö“óŗó¼õŠ” | |
| D£® | Ķعż·ÖĪöæÉÖŖ³£ĪĀĻĀ£ŗKa1£ØH2CO3£©£¾Kb£ØNH3•H2O£©£¾Ka2£ØH2CO3£© |
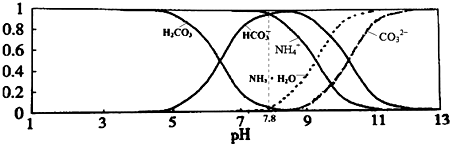
·ÖĪö A£®µ±pH=9Ź±£¬½įŗĻĶ¼ĻóÅŠ¶ĻČÜŅŗÖŠø÷Ąė×ÓÅØ¶Č“óŠ”£»
B£®øł¾ŻĢ¼ĖįĒāļ§ČÜŅŗÖŠµÄĪļĮĻŹŲŗć·ÖĪö£»
C£®øĆĢ¼ĖįĒāļ§ČÜŅŗµÄpH=7.8£¬½įŗĻĶ¼ĻóÅŠ¶ĻµĪČėĒāŃõ»ÆÄĘČÜŅŗŗóNH4+ŗĶHCO3-ÅØ¶Č±ä»Æ£»
D£®Ģ¼ĖįĒā°”ČÜŅŗĻŌŹ¾¼īŠŌ£¬øł¾ŻŃĪµÄĖ®½āŌĄķÅŠ¶Ļ¶žÕßµÄĖį¼īŠŌĒæČõ¼°µēĄėĘ½ŗā³£Źż“󊔣®
½ā“š ½ā£ŗA£®½įŗĻĶ¼ĻóæÉÖŖ£¬ČÜŅŗµÄpH=9Ź±£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”ĪŖ£ŗc£ØHCO3-£©£¾c£ØNH4+£©£¾c£ØNH3•H2O£©£¾c£ØCO32-£©£¬¹ŹA“ķĪó£»
B£®NH4HCO3ČÜŅŗÖŠ“ęŌŚĪļĮĻŹŲŗć£ŗc£ØNH4+£©+c£ØNH3•H2O£©=c£ØHCO3-£©+c£ØCO32-£©+c£ØH2CO3£©£¬ČÜŅŗĻŌ¼īŠŌŌņc£ØH+£©£¼c£ØOH-£©£¬ĖłŅŌc£ØNH4+£©+c£ØNH3•H2O£©+c£ØH+£©£¼c£ØOH-£©+2c£ØCO32-£©+c£ØH2CO3£©£¬¹ŹB“ķĪó£»
C£®0.1mol/LµÄNH4HCO3ČÜŅŗµÄpH=7.8£¬øł¾ŻĶ¼ĻóæÉÖŖ£¬µ±ČÜŅŗpHŌö“óŹ±£¬ļ§øłĄė×ÓÅضČÖš½„¼õŠ”£¬¶ųĢ¼ĖįĒāøłĄė×ÓÄܹ»ĻČŌö“óŗó¼õŠ”£¬¹ŹCÕżČ·£»
D£®ÓÉÓŚ0.1mol/LµÄNH4HCO3ČÜŅŗµÄpH=7.8£¬ĖµĆ÷Ģ¼ĖįĒāøłĄė×ÓµÄĖ®½ā³Ģ¶Č“óÓŚļ§øłĄė×ÓµÄĖ®½ā³Ģ¶Č£¬ŌņŅ»Ė®ŗĻ°±µÄµēĄėĘ½ŗā³£Źż“óÓŚKa1£ØH2CO3£©£¬Ka1£ØH2CO3£©£¼Kb£ØNH3•H2O£©£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģā½įŗĻĶ¼Ļóæ¼²éĮĖĄė×ÓÅØ¶Č“óŠ”±Č½Ļ”¢ŃĪµÄĖ®½āŌĄķµČÖŖŹ¶£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·Ķ¼ĻóĒśĻß±ä»ÆµÄŗ¬ŅåĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕµēŗÉŹŲŗć”¢ĪļĮĻŹŲŗć”¢ŃĪµÄĖ®½āŌĄķŌŚÅŠ¶ĻĄė×ÓÅØ¶Č“óŠ”ÖŠµÄÓ¦ÓĆ·½·Ø£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CCl4 | B£® | C2H4 | C£® | CH4 | D£® | C6H6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
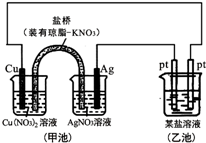
| A£® | Ķ¼ÖŠ¼×³ŲĪŖŌµē³Ų×°ÖĆ£¬µē×Ó“ÓĶµē¼«ĶعżČÜŅŗŗĶŃĪĒÅĮ÷ĻņAgµē¼« | |
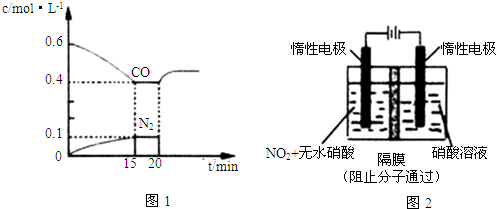
| B£® | ŹµŃé¹ż³ĢÖŠ£¬¼×³Ų×ó²ąÉÕ±ÖŠNO3-µÄÅØ¶Č²»±ä | |
| C£® | ČōÓĆĶÖĘUŠĪĪļ“śĢę”°ŃĪĒÅ”±£¬¹¤×÷Ņ»¶ĪŹ±¼äŗóČ”³öUŠĪĪļ³ĘĮæ£¬ÖŹĮæ²»±ä | |
| D£® | Čō¼×³ŲÖŠAgµē¼«ÖŹĮæŌö¼Ó5.4gŹ±£¬ŅŅ³Ųijµē¼«Īö³ö1.6g½šŹō£¬ŌņŅŅÖŠµÄijŃĪČÜŅŗ²»æÉÄÜŹĒAgNO3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K2CO3 | B£® | Na2SO4 | C£® | Ca£ØOH£©2 | D£® | Na2CO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĶعżŗģĶā¹āĘ×·ÖĪöæÉŅŌĒų·ÖŅŅ“¼ŗĶŅŅĖį | |
| B£® | æÉÓĆÕŗÅØŃĪĖįµÄĆŽ°ō¼ģŃéŹäĖĶ°±ĘųµÄ¹ÜµĄŹĒ·ńĀ©Ęų | |
| C£® | ¹ā“߻ƻ¹ŌĖ®ÖĘĒā±Čµē½āĖ®ÖĘĒāøü½ŚÄÜ»·±£”¢øü¾¼Ć | |
| D£® | ŹÆÓĶµÄĮŃ½ā”¢ĆŗµÄøÉĮ󔢵°°×ÖŹµÄŃĪĪöŗĶµķ·ŪµÄĖ®½ā¶¼ŹĒ»Æѧ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | T”ꏱ£¬²āµĆijNaNO2ČÜŅŗµÄpH=8£¬ŌņČÜŅŗÖŠc£ØNa+£©_c£ØNO2-£©=9.9”Į10-7mol•L-1 | |||||||||
| B£® | ŅŃÖŖH3PO2£Ø“ĪĮ×Ėį£©ŹĒŅ»ÖÖŅ»ŌŖÖŠĒæĖį£¬ŌņĘäÓėNaOHĖłŠĪ³ÉµÄĖįŹ½ŃĪNaH2PO2ČÜŅŗÖŠ“ęŌŚĻĀĮŠĄė×ÓÅØ¶Č“óŠ”¹ŲĻµc£ØNa+£©£¾c£ØH2PO2-£©c£ØOH-£©£¾c£ØH+£© | |||||||||
| C£® | Ņ»¶ØĪĀ¶ČĻĀ£¬ĄūÓĆpH¼Ę²ā¶Ø²»Ķ¬ÅØ¶Č“×ĖįČÜŅŗµÄpHÖµ£¬µĆµ½Čē±ķŹż¾Ż£ŗ
| |||||||||
| D£® |  ŅŃÖŖ£¬Ä³ĪĀ¶ČŹ±Ag2SO4ŌŚĖ®ÖŠµÄ³ĮµķČܽāĘ½ŗāĒśĻßČēĶ¼£¬æÉÖŖAg2SO4ŌŚ“ĖĪĀ¶ČĻĀµÄČܶȻż³£Źż£ØKsp£©ĪŖ8”Į10-4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ÅµēŹ±£ŗµ±ĶāµēĀ·Ķعż1molµÄµē×ÓŹ±£¬ĄķĀŪÉĻøŗ¼«°åµÄÖŹĮæŌö¼ÓĮĖ151.5g | |
| B£® | ³äµēŹ±£ŗŃō¼«·“Ó¦ŹĒPbSO4-2e-+2H2O=PbO2+SO42-+4H+ | |
| C£® | ·ÅµēŹ±£ŗÕż¼«·“Ó¦ŹĒPb-2e-+SO42-=PbSO4 | |
| D£® | ³äµēŹ±£ŗĒ¦Šīµē³ŲµÄŅõ¼«Ó¦ÓėµēŌ“µÄÕż¼«ĻąĮ¬ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com