
| A.天然气燃烧 | B.自然界中丁达尔效应 | C.蛋白质受热凝固 | D.食醋除水垢 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
分析 有新物质生成的变化叫化学变化,没有新物质生成的变化叫物理变化.化学变化的特征是:有新物质生成.判断物理变化和化学变化的依据是:是否有新物质生成.
解答 解:A.天然气主要成分为甲烷,甲烷燃烧生成了二氧化碳和水,反应的方程式是:CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O,有新物质生成,属于化学变化,故A不选;
B.丁达尔效应为胶体独有的性质,指光照射胶体,在垂直光的传播方向有一条光亮的通路,没有新物质生成,属于物理变化,故B选;
C.蛋白质受热凝固属于蛋白质变性,性质不同于原物质,有新物质生成,属于化学变化,故C不选;
D.食醋中的醋酸能和水垢中的碳酸钙反应生成醋酸钙、水和二氧化碳,属于化学变化,故D不选;
故选B.
点评 本考点考查了物理变化和化学变化的区别,基础性比较强,只要抓住关键点:是否有新物质生成,问题就很容易解决.本考点主要出现在选择题和填空题中,题目较简单.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:解答题
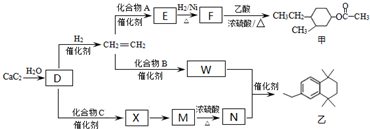
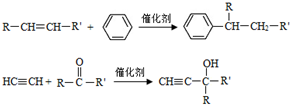 (-R、-R′代表烃基或-H)
(-R、-R′代表烃基或-H)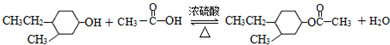 .
.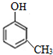 .
.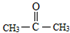 .
.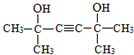 .
.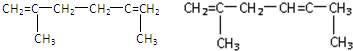 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,相同浓度的盐酸与氨水的混合溶液的pH=7,消耗盐酸的体积大 | |
| B. | 将pH=5的醋酸溶液稀释1000倍,溶液的pH=8 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铝熔点很高,可用于制造耐火坩埚 | |
| B. | 浓硫酸具有脱水性,可用于干燥氢气 | |
| C. | 氢氧化铝能与氢氧化钠反应,可用于治疗胃酸过多 | |
| D. | 二氧化硅能与氢氟酸反应,可用于制光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
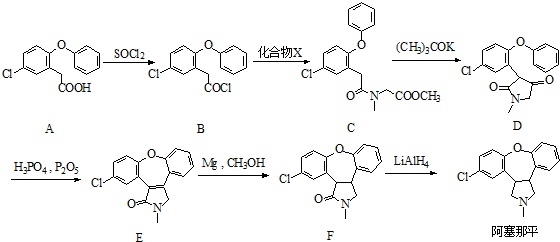
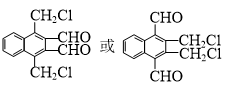 .
.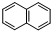 )的衍生物,且取代基都在同一个苯环上;
)的衍生物,且取代基都在同一个苯环上;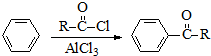 (R为烃基).根据已有知识并结合相关信息,写出以ClCH2CH2CH2Cl和
(R为烃基).根据已有知识并结合相关信息,写出以ClCH2CH2CH2Cl和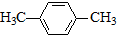 为原料制备
为原料制备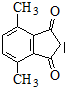 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验装置 | 电解质溶液 | 实验现象 | |
 | 5mol/L NaCl溶液 | a极附近 | b极附近 |
| 开始时,产生白色浑浊并逐渐增加,当沉入U形管底部时部分沉淀变为橙黄色;随后a极附近沉淀自下而上也变为橙黄色 | 产生无色气泡 | ||
| ①氯化亚铜(CuCl)为白色粉末,微溶于水; ②氢氧化亚铜(CuOH)为黄色不溶于水的固体,易脱水分解为红色的Cu2O; ③Cu+水溶液中不稳定,酸性条件下易歧化为Cu2+和Cu; ④氢氧化铜可以溶于浓NaOH得到蓝色溶液. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
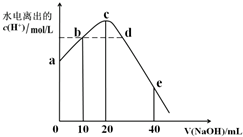
| A. | 从a到c,醋酸的电离始终受到促进 | |
| B. | a、d对应的纵坐标数值分别是:>10-12、>10-7 | |
| C. | b点:2c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| D. | 从b→c的过程中,既存在着pH=7的点,也存在着溶液中水所电离出的c(H+)=10-7的点 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 香叶醇是合成玫瑰精油的主要原料,其结构简式如下:
香叶醇是合成玫瑰精油的主要原料,其结构简式如下:查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上第一次质检化学卷(解析版) 题型:选择题
在一定温度和体积下,使9.6gC和一定量的O2在一密闭容器中完全反应, (C与O2均没有剩余),测知容器内压强比反应前增大了0.60倍,则O2的物质的量为
A.0.40mol B.0.50mol C.0.60mol D.0.70mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com