
| A�� | �٢ڢ� | B�� | �ڢۢ� | C�� | �ܢݢ� | D�� | �ڢۢ� |
���� �پ�����ԭ�ӳ��������������ж��Ǿ�����ԭ���������������Է��ԣ��Ǿ������Է��ԣ�
�ں��н��������ӵľ��岻һ�������Ӿ��壬�����ǽ������壻
�۹��ۼ��ɾ������ӵ��ȶ��ԣ�
�����Ӿ��������Ӱ뾶ԽС�������������Խ�࣬������Խ��
�ݾ����Ǿ���ṹ�Ļ�����Ԫ�������ڲ�������һ���������������ظ����У����Է��ԣ�
�������ý��ܶѻ���ʽ��
�߸ɱ������У�һ��CO2������Χ��12��CO2���ӽ��ڣ����Ӿ��岻һ�������ܶѻ���
��� �⣺�پ�����ԭ�ӳ��������������ж��Ǿ�����ԭ���������������Է��ԣ��Ǿ������Է��ԣ���������X��������ͷǾ��壬����ȷ��
�ڽ����������ɽ��������Ӻ����ɵ��ӹ��ɵģ����Ժ��н��������ӵľ��岻һ�������Ӿ��壬�����ǽ������壬�ʴ���
�۹��ۼ��ɾ������ӵ��ȶ��ԣ����Ӽ��������������Ӿ����۷е㣬�ʴ���
�����Ӿ��������Ӱ뾶ԽС�������������Խ�࣬������Խ��MgO��NaCl���־����У��뾶��Mg2+��Na+����MgO�ľ����ܽϴ��������۵�Ƚϸߣ�����ȷ��
�ݾ����Ǿ���ṹ�Ļ�����Ԫ�������ڲ�������һ���������������ظ����У����Է��ԣ���������X��������ͷǾ��壬����ȷ��
�������ý��ܶѻ���ʽ����ȡ���ܶѻ���ʽ������ʹ�����ñȽ��ȶ�������ȷ��
�߸ɱ������У�һ��CO2������Χ��12��CO2���ӽ��ڣ��ʴ���
���Բ���ȷ���Тڢۢߣ�
��ѡD��
���� ���⿼�龧��ͷǾ��������幹�����жϵ�֪ʶ�㣬��ȷ����ͷǾ����ص㡢���幹�����������ȶ���Ӱ�����ؼ��ɽ��ע����Ӽ������������Ӱ����Ӿ����۷е㡢��ѧ��Ӱ�����ȶ��ԣ�Ϊ�״��㣮


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
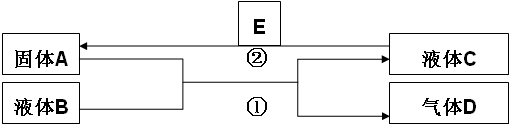
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | N2O��CO2 | B�� | O3��NO2 | C�� | CH4��NH3 | D�� | OH-��NH2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
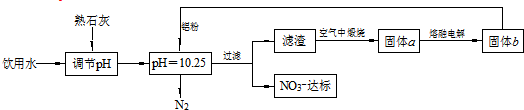
| A�� | �÷����ڵ���pHʱ����pH������С�������Al�������ʽ��� | |
| B�� | �ڼ������۵ķ�Ӧ�У���������ͻ�ԭ��������ʵ���֮��Ϊ10��3 | |
| C�� | ����ʯ�ҵ���PH��Ҫԭ���Ǽ۸�����������Ca2+�������� | |
| D�� | Ϊ�˽����ܺģ���ҵ��������AlCl3�������a���Ʊ�����b |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1-�ȱ�ϩ | B�� | ��ϩ | C�� | 2-��-2-��ϩ | D�� | 1-��ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ba��NO3��2--KOH--K2CO3--HNO3 | B�� | Ba��NO3��2--KOH--HNO3--K2CO3 | ||
| C�� | KOH--K2CO3--Ba��NO3��2--HNO3 | D�� | K2CO3--Ba��NO3��2--KOH--HNO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
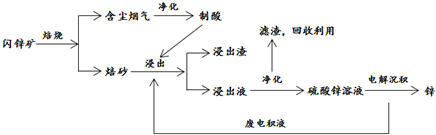
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
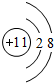 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com