
����Ŀ�����������(Na2S2O3)���н�ǿ�Ļ�ԭ�ԣ���������ǿ�ᷴӦ���ھ�ϸ��������Ӧ�ù㷺����SO2ͨ�밴һ���������Ƴɵ�Na2S��Na2CO3�Ļ����Һ�У����Ƶ�Na2S2O35H2O(���մ�)��
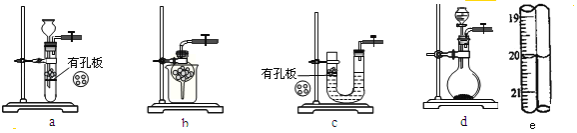
(1)ʵ������Na2SO3�������Ʊ�SO2����ѡ�õ����巢��װ����_____(ѡ����)������װ�������ԵIJ����ǣ��ر�ֹˮ�У���_______________��
(2)��Na2S��Na2CO3�Ļ����Һ�в���ͨ��SO2����Ĺ����У����֣�
��dz��ɫ�����������࣬��Ӧ�Ļ�ѧ����ʽΪ________________(���ɵ���Ϊ����)��
��dz��ɫ��������һ��ʱ�䲻�䣬����ɫ����������������Ӧ�Ļ�ѧ����ʽΪ__________________(���ɵ���Ϊ����)��
��dz��ɫ��������(��ʱ��Na2S2O3����)��
�ܼ���ͨ��SO2��dz��ɫ�����ֻ������࣬��Ӧ�Ļ�ѧ����ʽΪ_______________(���ɵ���Ϊ��ʽ��)��
(3)�Ʊ�Na2S2O3ʱ��Ϊ��ʹ��Ӧ�����������Na2S��Na2CO3�����ʵ���֮��ӦΪ_________��ͨ����Ӧ˳�ɱȽϳ����¶���ͬʱ��ͬ���ʵ���Ũ�ȵ�Na2S��Һ��Na2CO3��ҺpH�������_________��
(4)��������ƵĴ��ȿ��õζ������вⶨ��ԭ���ǣ�2S2O32��+I3��=S4O62��+3I����
��Ϊ��֤�����ʣ����������������Һ��������в���ȴ������ˮ����������___________��
��ȡ2.500g�����ʵ�Na2S2O35H2O�������50mL��Һ��ÿ��ȡ10.00mL��0.0500mol/L KI3��Һ�ζ�(�Ե���Ϊָʾ��)��ʵ����������(��3�γ�����Ϊ0.00���յ������ͼe�����ʲ��μӷ�Ӧ)��
��� | 1 | 2 | 3 |
����KI3��Һ�����/mL | 19.98 | 20.02 |
����ζ��յ��������_______________��Na2S2O35H2O(ʽ��248)������������(����4λС��)__________��
���𰸡�d ��Һ©��������ˮ����ˮ������˵������������ 3SO2+2Na2S=3S��+2Na2SO3 SO2+Na2CO3=Na2SO3+CO2 Na2S2O3+SO2+H2O=S��+2NaHSO3 2��1 ǰ�� ��ֹNa2S2O3��������O2���� ��Һ����ɫ��Ϊ��ɫ���Ұ�����ڲ���ȥ 99.20%
��������
(1)��ΪNa2SO3������ˮ��a��b��cװ�þ�����ѡ�ã�ʵ������Na2SO3�������Ʊ�SO2����ѡ�õ����巢��װ����d���ر�ֹˮ�У��������Ժܺã����Һ©����ˮ���ܵ�����ƿ�У�
(2)���䷴Ӧԭ��ΪSO2+Na2S+H2O=H2S+Na2SO3��2H2S+SO2=3S��+2H2O������3SO2+2Na2S=3S��+2Na2SO3��
����ɫ��ζ������ΪCO2���壬�仯ѧ����ʽΪSO2+Na2CO3=Na2SO3+CO2��
�ۻ�ɫ�������ٵ�ԭ��ΪNa2SO3+S=Na2S2O3��
�ܸ�������Na2S2O3������ǿ�ᷴӦ������dz��ɫ�����������ԭ��ΪNa2S2O3+SO2+H2O=S��+2NaHSO3��
(3)3SO2+2Na2S=3S��+2Na2SO3�٣�SO2+Na2CO3=Na2SO3+CO2�ڣ�Na2SO3+S=Na2S2O3�ۣ����+��+����3��4SO2+2Na2S+Na2CO3=3Na2S2O3+CO2������Na2S��Na2CO3�����ʵ���֮��Ϊ2��1����ΪSO2�Ⱥ�Na2S��Ӧ�������¶���ͬʱ��ͬ���ʵ���Ũ�ȵ�Na2S��Һ��Na2CO3��Һ��Na2S��Һ��pH����
(4)��������в���ȴ������ˮ��Ϊ�˸ϳ�ˮ�е�����������������Ʊ�������
�ڴﵽ�ζ��յ�ʱ��ɫͻ����30s����ɫ���ȸ��ݵζ����ĵı�Һ����������ƽ�����������2S2O32-+I3-=S4O62-+3I-�Ķ�����ϵ���㡣
(1)��ΪNa2SO3������ˮ��a��b��cװ�þ�����ѡ�ã�ʵ������Na2SO3�������Ʊ�SO2����ѡ�õ����巢��װ����d������װ�������ԵIJ����ǣ��ر�ֹˮ�У��������Ժܺã����Һ©����ˮ���ܵ�����ƿ�У�
(2)��dz��ɫ�����������࣬�䷴Ӧԭ��ΪSO2+Na2S+H2O=H2S+Na2SO3��2H2S+SO2=3S��+2H2O������Ӧ�Ļ�ѧ����ʽΪ��3SO2+2Na2S=3S��+2Na2SO3��
��dz��ɫ��������һ��ʱ�䲻�䣬����ɫ����������������Ӧ�Ļ�ѧ����ʽΪ����ɫ��ζ������ΪCO2���壬�仯ѧ����ʽΪSO2+Na2CO3=Na2SO3+CO2��
��dz��ɫ�������٣���ʱ��Na2S2O3���ɻ�ɫ���������ٵ�ԭ��Ϊ��Na2SO3+S=Na2S2O3��
�ܸ�������Na2S2O3������ǿ�ᷴӦ������ͨ��SO2��dz��ɫ�����ֻ������࣬����dz��ɫ�����������ԭ��Ϊ��Na2S2O3+SO2+H2O=S��+2NaHSO3��
(3)3SO2+2Na2S=3S��+2Na2SO3��
SO2+Na2CO3=Na2SO3+CO2��
Na2SO3+S=Na2S2O3��
��+��+����3��4SO2+2Na2S+Na2CO3=3Na2S2O3+CO2������Na2S��Na2CO3�����ʵ���֮��Ϊ2��1����ΪSO2�Ⱥ�Na2S��Ӧ�������¶���ͬʱ��ͬ���ʵ���Ũ�ȵ�Na2S��Һ��Na2CO3��Һ��Na2S��Һ��pH����
(4)��Ϊ��֤�����ʣ����������������Һ��������в���ȴ������ˮ���������ǣ���ֹNa2S2O3��������O2������
�ڴﵽ�ζ��յ�ʱ�����μ����һ�������������Һ����Һ��ɫ��ȥ�Ұ�����ڲ��仯��2�����ĵ�I2��Һ�����ƽ��ֵΪ20.00mL��
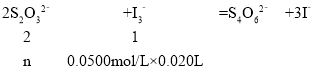
![]() �����n=0.002mol��250ml��Һ�к���Cr2O72�����ʵ���Ϊ0.002mol��
�����n=0.002mol��250ml��Һ�к���Cr2O72�����ʵ���Ϊ0.002mol��![]() =0.01mol��Na2S2O35H2O(ʽ��248)������������=
=0.01mol��Na2S2O35H2O(ʽ��248)������������=![]() ��100%=99.20%��
��100%=99.20%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ϳɾ������½ṹ�������ӡ�
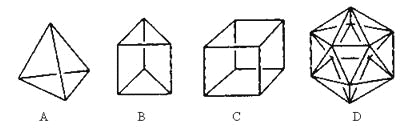
��1���ṹD��Ȼ�Dz����ܺϳɵģ�ԭ����________________________________��
��2���ڽṹA��ÿ����̼ԭ��֮�����һ��CH2ԭ���ţ������γɽ����Ľṹ��д�������ķ���ʽ___________��
��3��B��һ��ͬ���칹������ķ���������֤���÷������еĻ�ѧ�����ǵ�˫���������е���ʵ��______
a�����Ķ�λ��Ԫȡ����ֻ��һ�� b��������λ��Ԫȡ����ֻ��һ��
c������������̼̼���ļ�������� d���ܷ���ȡ����Ӧ�ͼӳɷ�Ӧ
��4�������й�����˵����ȷ����_______
a��������ͨʽCnH2n+2������һ���������ͼ���
b����������Hԭ�Ӹ�����һ������Cԭ�Ӹ����ࣻ
c����֪����ij����C��Hԭ�Ӹ����ȣ�ֻ�ܵó����������ʽ�������ܵó�����ʽ��
d����������H%��ߵ��Ǽ��顣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ӱ�컯ѧ��Ӧ���ʵ����غܶ࣬ij������ȤС����ʵ�鷽������̽����
(1)ȡ�����ʵ���Ũ�ȡ��������H2O2��Һ�ֱ����H2O2�ķֽ�ʵ�飬ʵ�鱨�����±���ʾ������ͽ����ԣ���

��ʵ��1��2�о�����__________��H2O2�ֽ����ʵ�Ӱ�졣
��ʵ��2��3��Ŀ����_______________��H2O2�ֽ����ʵ�Ӱ�졣
(2)������֪��Cu2����H2O2�ֽ�Ҳ�д����ã�Ϊ�Ƚ�Fe3����Cu2����H2O2�ֽ�Ĵ�Ч������С���ͬѧ�ֱ��������ͼ�ס�����ʾ��ʵ�顣�ش�������⣺

�ٶ�����ͼ��ͨ���۲�_______�����ԱȽϵó����ۡ���ͬѧ�����CuSO4��Һ��ΪCuCl2��Һ����������������_________��
�ڶ�����ͼ����ʾ��ʵ��ʱ���ռ���40 mL����Ϊ��������������Ӱ��ʵ������أ�ʵ������Ҫ������������__________��
(3)���Ը��������Һ�Ͳ�����Һ�ɷ�����Ӧ��2KMnO4��5H2C2O4��3H2SO4=K2SO4��2MnSO4��8H2O��10CO2����ʵ��ʱ���ֿ�ʼ��Ӧ���ʽ�������Һ��ɫ�����ԣ���һ��ʱ���ͻȻ��ɫ����Ӧ�������Լӿ졣�Դ�չ�����ۣ�
��ijͬѧ��ΪKMnO4��H2C2O4�ķ�Ӧ��______�ȷ�Ӧ������_______________��
�ڴ�Ӱ�컯ѧ��Ӧ���ʵ����ؿ�������Ϊ��������________��Ӱ�졣Ҫ֤����IJ��룬ʵ�鷽����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ��ɱ���ܱ������д������·�Ӧ��CO(g)+H2O(g)![]() CO2(g)+H2(g) ��H<0
CO2(g)+H2(g) ��H<0

���з�������ȷ����
A��ͼ���о���ֻ��t0ʱʹ�ô����Է�Ӧ���ʵ�Ӱ��
B��ͼ���о�����t0ʱ��С��������Է�Ӧ���ʵ�Ӱ��
C��ͼ���о������¶ȶԻ�ѧƽ���Ӱ�죬���ҵ��¶Ƚϸ�
D��ͼ���о����Ǵ����Ի�ѧƽ���Ӱ�죬�Ҽ�ʹ���˴���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��M����������ϩ�Ʒӣ�����һ�ּ�����ҩ��ṹ��ʽ���¡�������������ȷ����
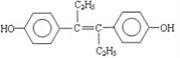
A.M���ڷ����廯����
B.M����NaOH��Һ��NaHCO3��Һ������Ӧ
C.1molM�������7molH2�����ӳɷ�Ӧ
D.1molM�뱥����ˮ��ϣ��������5molBr2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ȼ�շ��ⶨij�ְ�����(CxHyOzNm)�ķ�����ɡ�ȡWg���ְ�������ڴ����г��ȼ�գ����ɶ�����̼��ˮ�͵���������ͼ��ʾװ�ý���ʵ�顣

�ش��������⣺
��1��ʵ�鿪ʼʱ������ͨ��һ��ʱ�����������������__________________��
��2������װ������Ҫ���ȵ�������_______ (��д��ĸ)������ʱӦ�ȵ�ȼ_____���ľƾ��ơ�
��3��Aװ���з�����Ӧ�Ļ�ѧ����ʽ��____________________________��
��4��Dװ�õ�������____________________________��
��5����ȡ���������ʱ��Ӧע����_________________����_________________��
��6��ʵ���в�õ��������ΪVmL(��״��)��Ϊȷ���˰�����ķ���ʽ������Ҫ���й�������____________________��
A�����ɶ�����̼���������
B������ˮ������
C��ͨ�����������
D�����������Է�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2���ǻ��춡������������ˮ����һ��Ӧ�����л��ϳɺ�ҩ������Ļ���ԭ�ϡ�

��1��2���ǻ��춡�������ķ���ʽΪ_________����ͬ��ѧ���������ں˴Ź�������ͼ���в�ͬ�����շ壬��2���ǻ��춡��������_________�����շ壻
��2���٢ڵķ�Ӧ���ͷֱ�Ϊ_________��_________��
��3����֪IΪ�������I��B�Ļ�ѧ����ʽΪ_________��
��4�����۲���F�Ľṹ��ʽΪ_________��
��5�������![]() ��
�� ��˵����ȷ����_________��˫ѡ������ĸ����
��˵����ȷ����_________��˫ѡ������ĸ����
A����������FeCl3��Һ����ɫ����ǰ�߲���
B�����߶�������NaHCO3��Һ��Ӧ�ų�CO2
C�����߶�����������������Һ������Ӧ�����������ʵ������ʱ�������������Ƶ��������
D�����߶����������������ӳɷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£������йص������Һ��˵���в���ȷ���ǣ� ��
A.��0.1molL-1CH3COOH��Һ�м�������ˮ����Һ��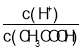 ��С
��С
B.��CH3COONa��Һ��20��������30�棬��Һ��![]() ��С
��С
C.�������м��백ˮ�����ԣ���Һ��![]() =1
=1
D.��AgCl��AgBr�ı�����Һ�м�������AgNO3����Һ��![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾʵ��װ�ý�����Ӧʵ�飬�ܴﵽʵ��Ŀ�ĵ���
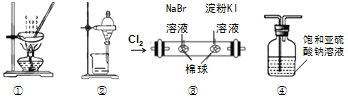
A.ͼ����ʾװ�ã�����NH4Cl������Һ�Ʊ�NH4Cl����
B.ͼ����ʾװ�ã�����CCl4��ȡI2ˮ����л���
C.ͼ����ʾװ�ã�֤�������ԣ�Cl2��Br2��I2
D.ͼ����ʾװ�ã���ȥSO2�л��е�����HCl����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com