
| A、能使湿润的蓝色石蕊试纸先变红后褪色 |
| B、使沾有酸性高锰酸钾溶液的滤纸褪色,证明了二氧化硫的漂白性 |
| C、使品红试纸褪色,证明了二氧化硫的漂白性 |
| D、沾有酚酞和NaOH 溶液的滤纸褪色,证明了二氧化硫具有漂白性 |


科目:高中化学 来源: 题型:
| 化学键 | H-H | Cl-Cl | Cl-H |
| 键能/(kJ?mol-1) | 436 | 243 | 431 |
| A、+862 kJ?mol-1 |
| B、+679 kJ?mol-1 |
| C、-183 kJ?mol-1 |
| D、+183 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、C+O2
| ||||
B、CH4+2O2
| ||||
| C、CaO+H2O=Ca(OH)2 | ||||
D、CuO+H2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、③④①② |
| C、①③④② | D、①③②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图装置,已知两电极上发生的电极反应分别为:
如图装置,已知两电极上发生的电极反应分别为:查看答案和解析>>
科目:高中化学 来源: 题型:
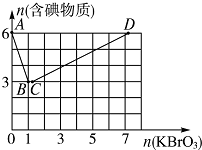 现向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.请回答下列问题:
现向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com