
| A. | 属于羧基类的有2种 | |
| B. | 属于酯类的有3种 | |
| C. | 存在分子中含有六元环的同分异构体 | |
| D. | 分子中可含有两种不同的官能团 |
分析 A、C4H8O2属于羧酸时,可以根据羧基位置异构可以得到丁酸的同分异构体;
B、C4H8O2属于酯类的同分异构体,为饱和一元酯,根据酸和醇的种类来确定;
C、根据六元环结合有机物的分子式来确定;
D、C4H8O2属于羟基醛时,具有两种官能团,据此解答即可.
解答 解:A、C4H8O2属于羧酸时,可以是丁酸或2-甲基丙酸,共有2种同分异构体,故A正确;
B、C4H8O2属于酯类的同分异构体,为饱和一元酯,若为甲酸与丙醇形成的酯,甲酸只有1种结构,丙醇有2种,形成的酯有2种,若为乙酸与乙醇形成的酯,乙酸只有1种结构,乙醇只有1种结构,形成的乙酸乙酯有1种,若为丙酸与甲醇形成的酯,丙酸只有1种结构,甲醇只有1种结构,形成的丙酸甲酯只有1种,所以C4H8O2属于酯类的同分异构体共有4种,故B错误;
C、存在分子中含有六元环的同分异构体: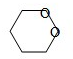 ,故C正确;
,故C正确;
D、C4H8O2属于羟基醛时,即含有羟基和醛基两种官能团,故D正确;故选B.
点评 本题考查同分异构体的种类,根据官能团异构和位置异构和碳链异构来综合分析同分异构体的种数,难度不大,有利于培养学生的逻辑推理能力


科目:高中化学 来源: 题型:解答题
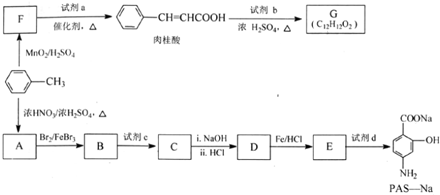
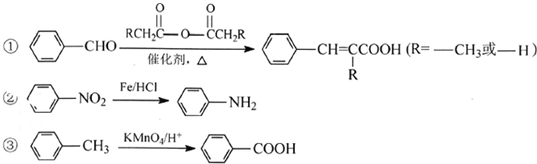
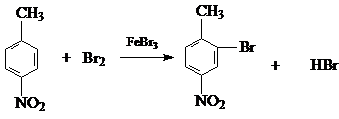 .
.  .
. 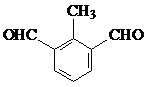 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li为电池的负极 | |
| B. | 电池的电解液可用LiCl水溶液代替 | |
| C. | 放电时电子从负极经外电路流向正极 | |
| D. | 充电时阳极反应式为:4Cl-+S+SO2-4e-=2SOCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以通过过滤的方法将淀粉胶体中混有的氯化钠溶液除去 | |
| B. | 在2mL10%的CuSO4(aq)中滴入3滴 2%的NaOH(aq),配制检验醛基的试剂 | |
| C. | 用托盘天平准确称取14.80g Ca(OH)2,配制100mL 2.0 mol/L的Ca(OH)2溶液 | |
| D. | 乙酸乙酯中少量乙醇杂质可加水除去,其原理与溴水中加四氯化碳萃取溴类似 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用浓盐酸与二氧化锰共热制氯气 | |
| B. | 标准状况下,将1 g铝片投入20 mL 18 mol•L-1硫酸中 | |
| C. | 向100 mL 4 mol•L-1硝酸中加入5.6 g 铁 | |
| D. | 在5×107 Pa、500℃和铁触媒催化的条件下,用氮气和氢气合成氨 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北石家庄辛集中学高二上阶段考一化学卷(解析版) 题型:选择题
分子式为C4H8Cl2的同分异构体有( )
A.3种 B.5种 C.8种 D.9种
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氟是电负性最大的非金属元素,又因其半径较小,极易和金属元素反应,并将它们氧化到最高价态,生成MnF7、VF5、CaF2等.氟还可以和氧形成一系列的氟化物,如OF2、O2F2、O4F2等.请回答下列问题:
氟是电负性最大的非金属元素,又因其半径较小,极易和金属元素反应,并将它们氧化到最高价态,生成MnF7、VF5、CaF2等.氟还可以和氧形成一系列的氟化物,如OF2、O2F2、O4F2等.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com