
| Čõµē½āÖŹ | H2CO3 | NH3•H2O |
| µēĄėĘ½ŗā³£Źż | Ka1=4.30”Į10-7 Ka2=5.61”Į10-11 | Kb=1.77”Į10-5 |
·ÖĪö ¢ŁČõµē½āÖŹµÄµēĄėĘ½ŗā³£ŹżŌ½Š”£¬ĘäĻąÓ¦µÄČõĄė×ÓĖ®½ā³Ģ¶ČŌ½“ó£¬Ģ¼ĖįµŚ¶ž²½µēĄėĘ½ŗā³£ŹżŠ”ÓŚŅ»Ė®ŗĻ°±µēĄėĘ½ŗā³£Źż£¬ŌņĢ¼ĖįøłĄė×ÓĖ®½ā³Ģ¶Č“óÓŚŅ»Ė®ŗĻ°±£¬¾Ż“ĖÅŠ¶ĻĢ¼ĖįÄĘČÜŅŗĖį¼īŠŌ£»
¢ŚĢ¼ĖįøłĄė×ÓĖ®½ā³Ģ¶Č“óÓŚļ§øłĄė×ÓĖ®½ā³Ģ¶Č£¬Ģ¼ĖįĒāøłĄė×ÓÅØ¶Č“óÓŚŅ»Ė®ŗĻ°±ÅØ¶Č£¬ČÜŅŗÖŠ“ęŌŚµēŗÉŹŲŗćŗĶĪļĮĻŹŲŗć£¬½įŗĻµēŗÉŹŲŗć”¢ĪļĮĻŹŲŗćŗĶÖŹ×ÓŹŲŗćÅŠ¶Ļ£®
½ā“š ½ā£ŗ¢Ł·ÖĪöµēĄėĘ½ŗā³£ŹżæÉÖŖµēĄė³Ģ¶Č£¬NH3•H2O£¾H2CO3£¾HCO3-£¬¶ŌÓ¦ŃĪĖ®½ā³Ģ¶ČNH4+£¼HCO3-£¼CO32-£¬³£ĪĀĻĀ0.1mol•L-1µÄ£ØNH4£©2CO3ČÜŅŗ³Ź¼īŠŌ£¬ÓÉÓŚNH3•H2OµÄµēĄėĘ½ŗā³£Źż“óÓŚHCO3-µÄµēĄėĘ½ŗā³£Źż£¬Ņņ“ĖCO32-Ė®½ā³Ģ¶Č“óÓŚNH4+Ė®½ā³Ģ¶Č£¬ČÜŅŗÖŠc £ØOH-£©£¾c£ØH+£©£¬ČÜŅŗ³Ź¼īŠŌ£»
¹Ź“š°øĪŖ£ŗ¼ī£»ÓÉÓŚNH3•H2OµÄµēĄėĘ½ŗā³£Źż“óÓŚHCO3-µÄµēĄėĘ½ŗā³£Źż£¬Ņņ“ĖCO32-Ė®½ā³Ģ¶Č“óÓŚNH4+Ė®½ā³Ģ¶Č£¬ČÜŅŗ³Ź¼īŠŌ£»
¢ŚA£®ČÜŅŗÖŠļ§øłĄė×ÓÅØ¶Č“óÓŚĢ¼ĖįøłĄė×ÓÅØ¶Č£¬Ģ¼ĖįøłĄė×ÓĖ®½ā³Ģ¶Č“óÓŚļ§øłĄė×ÓĖ®½ā³Ģ¶Č£¬ĖłŅŌČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”ĪŖ£ŗc£ØNH4+£©£¾c£ØCO32-£©£¾c£ØHCO3-£©£¾c£ØNH3•H2O£©£¬¹ŹAÕżČ·£»
B£®ČÜŅŗÖŠ“ęŌŚµēŗÉŹŲŗćĪŖ£ŗc£ØNH4+£©+c£ØH+£©=c£ØHCO3-£©+c£ØOH-£©+2c£ØCO32-£©£¬¹ŹB“ķĪó£»
C£®ŅĄ¾ŻČÜŅŗÖŠĪļĮĻŹŲŗćµĆµ½£ŗc£ØCO32-£©+c£ØHCO3-£©+c£ØH2CO3£©=0.1mol•L-1 £¬¹ŹCÕżČ·£»
D£®ŅĄ¾ŻČÜŅŗÖŠĪļĮĻŹŲŗć£¬n£ØN£©£ŗn£ØC£©=2£ŗ1£¬½įŗĻČÜŅŗÖŠĄė×ÓÖÖĄąŗĶŹŲŗć¹ŲĻµµĆµ½£ŗc£ØNH4+£©+c£ØNH3•H2O£©=2c£ØCO32-£©+2c£ØHCO3-£©+2c£ØH2CO3£©£¬¹ŹDÕżČ·£»
E£®ŅĄ¾ŻČÜŅŗÖŠÖŹ×ÓŹŲŗć£¬c£ØNH3•H2O£©+c£ØOH-£©=c£ØHCO3-£©+c£ØOH-£©+2c£ØH2CO3£©£¬¹ŹE“ķĪó£»
¹Ź“š°øĪŖ£ŗBE£®
µćĘĄ ±¾ĢāŅŌŃĪĄąĖ®½āĪŖŌŲĢåæ¼²éĄė×ÓÅØ¶Č“óŠ”±Č½Ļ£¬ĪŖøßĘµæ¼µć£¬Ć÷Č·µēĄėĘ½ŗā³£ŹżÓėČõĄė×ÓĖ®½ā³Ģ¶Č¹ŲĻµŹĒ½ā±¾Ģā¹Ų¼ü£¬×¢ŅāŹŲŗćĖ¼ĻėµÄĮé»īŌĖÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®


 æģĄÖŹī¼ŁŹī¼ŁÄÜĮ¦×Ō²āÖŠĪ÷Źé¾ÖĻµĮŠ“š°ø
æģĄÖŹī¼ŁŹī¼ŁÄÜĮ¦×Ō²āÖŠĪ÷Źé¾ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C2H4 µÄ½į¹¹¼ņŹ½æɱķŹ¾ĪŖ CH2CH2 | |
| B£® | 6 øöĢ¼Ō×ÓŠĪ³ÉµÄĢž·Ö×ÓÖŠ£¬×ī¶ąÓŠ5øöC-Cµ„¼ü | |
| C£® | C6H6 ·Ö×ÓÖŠ£¬ĖłÓŠŌ×Ó¾łæÉÄÜŌŚĶ¬Ņ»Ę½ĆęÄŚ | |
| D£® | C3H6 ·Ö×ÓÖŠŅ»¶Øŗ¬ÓŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
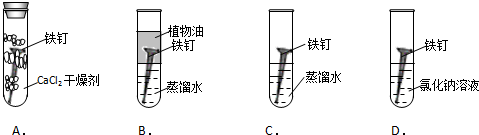
| A£® | ĀČŅŅĶéŹĒÓÉĢ¼”¢Ēā”¢ĀČČżÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļ | |
| B£® | ĀČŅŅĶéŹĒÓÉ2øöĢ¼Ō×Ó”¢5øöĒāŌ×ÓŗĶ1øöĀČŌ×Ó¹¹³ÉµÄ | |
| C£® | ĀČŅŅĶéÓĆÓŚĄä¶³Āé×ķÓėĘä·Šµć½ĻµĶ£¬Ņ×»Ó·¢ĪüČČÓŠ¹Ų | |
| D£® | ĀČŅŅĶéÖŠĢ¼”¢Ēā”¢ĀČČżÖÖŌŖĖŲµÄÖŹĮæ±ČĪŖ48£ŗ10£ŗ7l |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
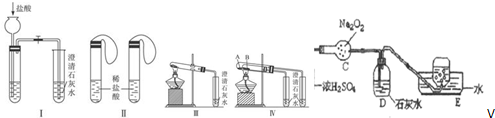
 Ä³Ń§ÉśÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠ»Æѧ·“Ó¦X+2YØT2ZÄÜĮæ±ä»ÆĒéæöµÄŃŠ¾æ£®µ±ĶłŹŌ¹ÜÖŠµĪ¼ÓŹŌ¼ĮYŹ±£¬æ“µ½µ¼¹ÜÖŠ¼×“¦ŅŗĆęĻĀ½µ£¬ŅŅ“¦ŅŗĆęÉĻÉż£®¹ŲÓŚøĆ·“Ó¦µÄŠšŹöÕżČ·µÄŹĒ£Ø””””£©
Ä³Ń§ÉśÓĆČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠ»Æѧ·“Ó¦X+2YØT2ZÄÜĮæ±ä»ÆĒéæöµÄŃŠ¾æ£®µ±ĶłŹŌ¹ÜÖŠµĪ¼ÓŹŌ¼ĮYŹ±£¬æ“µ½µ¼¹ÜÖŠ¼×“¦ŅŗĆęĻĀ½µ£¬ŅŅ“¦ŅŗĆęÉĻÉż£®¹ŲÓŚøĆ·“Ó¦µÄŠšŹöÕżČ·µÄŹĒ£Ø””””£© | A£® | ¢Ł¢Ś¢Ū | B£® | ¢Ł¢Ū | C£® | ¢Ł¢Ś | D£® | ¢Ś |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com