
分析 (1)反应后溶液温度升高,说明该反应为放热反应;
(2)氢氧化钾与硫酸反应生成氯酸钾和水,据此写出反应的化学方程式、离子方程式;
(3)氢氧化钾与硫酸的反应实质为氢离子与氢氧根离子发生中和反应,从而可知中和反应为放热反应.
解答 解:(1)测得反应后溶液温度升高,说明氢氧化钾和硫酸的反应为放热反应,
故答案为:硫酸与烧碱的反应是放热反应;
(2)氢氧化钾和硫酸反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O,改写成离子方程式为:H++OH-=H2O,
故答案为:2NaOH+H2SO4=Na2SO4+2H2O,H++OH-=H2O;
(3)氢氧化钾与硫酸反应实质为:H++OH-=H2O,从而证明酸碱中和反应都是放热反应,
故答案为:酸碱中和反应是放热反应.
点评 本题考查了离子方程式、化学方程式的书写及探究吸热反应与放热反应,题目难度中等,明确离子方程式、化学方程式书写原则为解答关键,注意明确化学反应与能量变化的关系.


 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表有七个主族,八个副族 | |
| B. | 每个短周期都有8种元素,每个长周期中都有18种元素 | |
| C. | 第三主族位于元素周期表的第三列(从左往右) | |
| D. | 零族位于元素周期表的第18列(从左往右) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能描述出反应发生的状态 | B. | 说明反应条件 | ||
| C. | 为了区别一般的化学方程式 | D. | 物质呈现的状态与反应热有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取样,若加入淀粉溶液,溶液显蓝色,则一定有I- | |
| B. | 取样,若加入AgNO3溶液由白色沉淀,则一定有Cl- | |
| C. | 取样,若加入BaCl2溶液,有白色沉淀产生,则一定有SO42- | |
| D. | 取样,若加入NaOH溶液,微热,产生使湿润红色石蕊试纸变蓝的气体,则一定有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和苯都能发生加成反应 | |
| B. | 乙醇和乙酸都能与氢氧化钠溶液反应 | |
| C. | 乙烯和苯都能使酸性KMnO4溶液褪色 | |
| D. | 葡萄糖和蔗糖都可发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
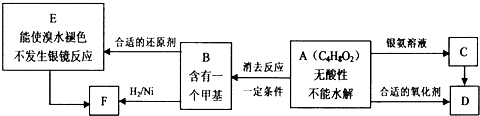
 .
.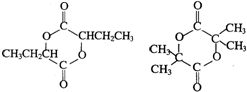 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com