
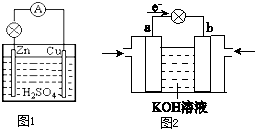
 原电池是直接把化学能转化为电能的装置.
原电池是直接把化学能转化为电能的装置.

 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2(g)+Cl2(g)=2HCl(g);△H=-92.3 kJ/mol |
| B、H2(g)+Cl2(g)=HCl(g);△H=+92.3kJ/mol |
| C、2HCl=H2+Cl2;△H=+184.6kJ/mol |
| D、H2 (g)+Cl2(g)=2HCl(g);△H=-184.6kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2(g)+O2(g)=2H2O(1)2H2(g)+O2(g)=2H2O(g) | ||||
B、
| ||||
C、C(s)+
| ||||
| D、S(s)+O2(g)=SO2(g) S(g)+O2(g)=SO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、开发利用太阳能、生物质能等清洁能源 |
| B、研制开发燃料电池汽车 |
| C、积极发展公共交通,倡导绿色出行 |
| D、充分开发利用纯天然纤维,停止使用各种化学合成材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com