
【题目】已知某可逆反应:mA(g)+nB(g) ![]() r C(g)在密闭容器中进行。下图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线。由曲线分析下列判断正确的是( )
r C(g)在密闭容器中进行。下图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线。由曲线分析下列判断正确的是( )
A.T1>T2 , p1>p2 , m+n>r,正反应吸热
B.T1<T2 , p1<p2 , m+n<r,正反应吸热
C.T1>T2 , p1>p2 , m+n<r,正反应放热
D.T1<T2 , p1<p2 , m+n>r,正反应放热
【答案】B
【解析】根据“先拐先平,温高压大”,当压强相同时,温度为T2的先达到平衡,说明温度是T2大于T1。但温度越高,反应物的含量越低,所以正反应是吸热反应。当温度相同时,压强为P2的先达到平衡,说明P2大于P1 , 压强越大,反应物的含量越高,所以正反应是体积增大的反应,即m+n<r;选B。
第一步:温度、压强大小判断
温度越高,反应越快,越先平衡:由P2相同时,T2先于T1平衡,说明温度是T2大于T1
压强越大,气体体积减小,则浓度越大,反应越快,越先平衡,由T2相同时,压强为P2的先达到平衡,说明P2大于P1 ,
第二步:平衡移动方向判断
由P2相同时,T2大于T1 , 【平衡向减小温度(吸热)的方向移动】,现随温度越高,反应物B%减小,所以正反应是吸热反应。
由T2相同时,压强P2大于P1 , 【平衡向减小压强(气体物质系数总和小)的方向移动】,现随压强越高,反应物B%增大,所以m+n<r


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量。某兴趣小组用下图所示装置制备NaNO2并对其性质作如下探究(A中加热装置已略去)。
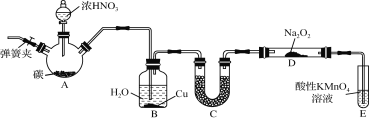
【背景素材】
①2NO+Na2O2=2NaNO2;
②NO能被酸性KMnO4氧化成NO![]() ,MnO
,MnO![]() 被还原为Mn2+。
被还原为Mn2+。
③在酸性条件下NaNO2能把I-氧化为I2;S2O32-能把I2还原为I-。
【制备NaNO2】
(1) 装置A三颈烧瓶中发生反应的化学方程式为 。
(2) B装置的目的是① ,② 。
(3) 为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是 (填序号)。
A. P2O5 B. 碱石灰 C. 无水CaCl2 D. 生石灰
(4) E装置发生反应的离子方程式是 。
【测定NaNO2纯度】
(5) 本小题可供选择的试剂有:
A.稀硫酸
B.c1mol·L-1KI溶液
C.淀粉溶液
D.c2mol·L-1Na2S2O3溶液
E.c3mol·L-1酸性KMnO4溶液
①利用NaNO2的还原性来测定其纯度,可选择的试剂是 (填序号)。
②利用NaNO2的氧化性来测定其纯度的步骤是:准确称取质量为m g的NaNO2样品放入锥形瓶中,加适量水溶解 (请补充完整实验步骤)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,下列叙述中不正确的是( )
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,下列叙述中不正确的是( )
A.x的值为2
B.A的转化率为60%
C.B的平衡浓度为0.8 mol/L
D.D的体积分数为25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为实验室从海带中提取碘单质的流程示意图,判断下列说法错误的是( )
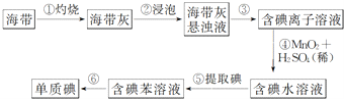
A. 步骤①需要用到蒸发皿 B. 步骤③需要过滤装置
C. 步骤⑤需要用到分液漏斗 D. 步骤⑥需要蒸馏装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH 的关系如下图所示。下列有关叙述正确的是
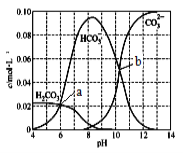
A. 随pH增大,![]() 数值先减小后增大
数值先减小后增大
B. b点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(Cl-)+c(HCO3- )
C. 25℃时,碳酸的第一步电离常数Ka1=10-7
D. 溶液呈中性时:c(HCO3- )>c(CO32-)>c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属的工业制法中,正确的是![]()
![]()
A. 制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液
B. 制铁:以铁矿石为原料,用焦炭和空气反应生成CO在高温下还原铁矿石中的铁
C. 制镁:用海水为原料,经一系列过程制得氧化镁固体,电解熔融的氧化镁得镁
D. 制钛:用金属钠置换![]() 溶液中的钛
溶液中的钛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下几种有机物:
![]()

![]() 癸烷
癸烷 ![]()
![]()
![]()
![]()
![]()
![]()

![]() 丙烷
丙烷
请利用上述给出的物质按要求回答下列问题:
(1)相对分子质量为44的烷烃的结构简式为__________________;
(2)与③互为同分异构体的是_________(填序号),③在光照的条件下与氯气发生反应生成的一氯代物结构有__________种;
(3)有机物②在加热条件下和CuO反应的化学方程式__________________________;
(4)用“![]() ”表示
”表示![]() 熔沸点高低顺序:____________(填序号);
熔沸点高低顺序:____________(填序号);
(5)有机物②和与它相对分子质量相同的饱和一元羧酸发生酯化反应的化学方程式___________________________________________________;
(6)在![]() ,
,![]() 条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是___________(填序号);它与
条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是___________(填序号);它与![]() 互为___________关系。
互为___________关系。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中列出五种短周期元素A、B、C、D、E的信息,请推断后回答:
元素 | 有关信息 |
A | 元素主要化合价为-2,原子半径为0.074nm |
B | 所在主族序数与所在周期序数之差为4 ,形成的单质是黄绿色有毒气体 |
C | 原子半径为 |
D | 最高价氧化物的水化物能按 |
E | 原子半径为 |
(1)写出C元素在周期表中的位置_________________,写出D元素最高价氧化物的水化物电子式________________。
(2)写出A与C元素气态氢化物的稳定性由大到小的顺序是______________![]() 填化学式
填化学式![]() 。
。
(3)写出B与C元素最高价氧化物的水化物酸性由弱到强的顺序是_________![]() 填化学式
填化学式![]() 。
。
(4)写出D的单质在氧气中燃烧生成产物为淡黄色固体,该氧化物含有的化学键类型是________________。
(5)砷![]() 与E同一主族,As原子比E原子多两个电子层,则As的原子序数为_______,其氢化物的化学式为___________。
与E同一主族,As原子比E原子多两个电子层,则As的原子序数为_______,其氢化物的化学式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com