
【题目】下列关于常见有机物的说法正确的是
A. 乙醚和乙醇互为同分异构体
B. 糖类、油脂、蛋白质均能发生水解反应
C. 聚氯乙烯可用作生产食品包装材料的原料
D. 分子式为C3H8O的有机物,只有2种能发生酯化反应
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是( )
A. 乙烷与氯气在光照下反应生成氯乙烷;乙烯与氯化氢反应生成氯乙烷
B. 甲苯硝化生成对硝基甲苯;乙醇催化氧化生成乙醛
C. 苯使溴水褪色;丙烯使溴水褪色
D. 乙酸和乙醇生成乙酸乙酯;苯与液溴反应生成溴苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼和铝位于同一主族,它们可以形成许多组成和性质类似的化合物。一种用硼镁矿 (Mg2B2O5 H2O)制取单质硼的工艺流程图如下:

结合流程图回答下列问题:
(1)溶液a、溶液b中溶质的化学式分别为 、 。
(2)写出步骤①的化学方程式 。
(3)写出步骤②的离子方程式 。
(4)步骤③中化学反应可以发生的原因是 。

(5)过硼酸钠晶体(NaBO3 4H2O)是一种优良的漂白剂,在 70℃以上加热会逐步失去结晶水。实验测得过硼酸钠晶体 的质量随温度变化的情况如右图所示,则T2℃时所得晶体的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;
X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则在X极附近观察到的实验现象是 ;Y电极上的电极反应式为 .若电解过程转移的电子为0.2mol,则X电极上产生的气体体积是 L(标准状况下).
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是 ;Y电极的电极反应式为 .(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)如图为某粒子的结构示意图,当A-B=10时,该粒子是 (填原子、阳离子或阴离子);例如 (填化学用语) 当B=8时,若该粒子带1个单位的正电荷,则该粒子的符号是 ;若该粒子带1个单位的负电荷,则该粒子的符号是 。
(2)下表是元素周期表的一部分,这四种元素均位于第 周期,它们的本质区别是 。硅与碳位于同族,化学性质相似,则二氧化硅与烧碱溶液反应的化学方程式为 。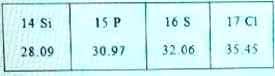
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小明用蜡烛进行了下列活动.
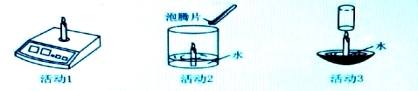
(1)活动1:点燃蜡烛后,电子秤示数逐渐减小.蜡烛减小的质量 (填“大于”、
“等于”或“小于”)燃烧后生成物的总质量.
(2)活动2:加入泡腾片(主要成分含柠檬酸、碳酸氢钠等),观察到水中产生大量气泡、
蜡烛逐渐熄灭.产生上述现象的原因是 。
(3)活动3:用玻璃杯迅速扣住燃烧的蜡烛,并使杯口始终浸没在水中.下列说法正确的
是 (填序号).
A.可观察到蜡烛熄灭 B.最终杯中液面高于碗中液面
C.该方法能准确测定空气中氧气的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是( )
A.NH4+,SO42﹣,K+,OH﹣ B.Na+,Ba2+,NO3﹣,SO42﹣
C.K+,Cl﹣,CO32﹣,Na+ D.H+,NO3﹣,Na+,CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2O4(g)![]() 2NO2(g)△H=+57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示。下列说法正确的是( )
2NO2(g)△H=+57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示。下列说法正确的是( )

A.a、c两点的反应速率:a>c
B.a、c两点气体的颜色:a深,c浅
C.由状态b到状态a,可以用加热的方法
D.a、c两点气体的平均相对分子质量:a>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】800 ℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O维持恒温,发生反应CO(g)+H2O(g)![]() H2(g)+CO2(g),反应过程中测定的部分数据见下表:
H2(g)+CO2(g),反应过程中测定的部分数据见下表:
反应时间/min | 0 | 2 | 4 | 6 |
n(CO)/mol | 1.20 | 0.90 | 0.80 | |
n(H2O)/mol | 0.60 | 0.20 |
(1)反应在2 min内的平均速率为v(H2O)=________。
(2)800 ℃时,化学平衡常数K的值为________。
(3)保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率________(填“增大”、“减小”或“不变”)。
(4)在恒温恒压密闭容器中通入CO和H2O各1 mol发生该反应,当反应达到平衡后,维持温度与压强不变,t1时再通入各1 mol的CO和H2O的混合气体,请在下图中画出正(v正)、逆(v逆)反应速率在t1后随时间t变化的曲线图。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com