
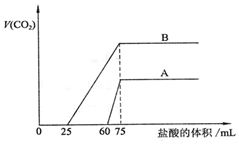
 取等物质的量浓度的NaOH溶液两份A和B,每份50mL,向其中各通入一定量的CO2,然后各取溶液10mL,分别将其稀释为100mL,再分别向稀释后的溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2气体体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
取等物质的量浓度的NaOH溶液两份A和B,每份50mL,向其中各通入一定量的CO2,然后各取溶液10mL,分别将其稀释为100mL,再分别向稀释后的溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2气体体积与所加盐酸体积之间的关系如图所示,试回答下列问题:分析 (1)由图可知,对应A溶液来说,滴加盐酸60mL时没有气体生成,可能发生OH-+H+=H2O和CO32-+H+=HCO3-,假设原溶液中只有碳酸钠,生成碳酸氢钠需要盐酸的体积和碳酸氢钠生成氯化钠需要盐酸的体积相等,实际上需要盐酸的体积为60mL,远远大于碳酸氢钠生成氯化钠需要盐酸的体积(75-60)mL=15mL,说明原溶液中的溶质是NaOH和Na2CO3;
生成二氧化碳消耗盐酸的体积为75mL-60mL=15mL,生成CO2气体时,发生反应HCO3-+H+=H2O+CO2↑,根据n=cV计算n(HCl),再根据方程式计算二氧化碳的体积;
(2)对于B溶液来说,假设原溶液中只有碳酸钠,生成碳酸氢钠需要盐酸的体积和碳酸氢钠生成氯化钠需要盐酸的体积相等,实际上需要盐酸的体积25mL小于碳酸氢钠生成氯化钠需要盐酸的体积(75-25)mL=50mL,说明原溶液中的溶质是Na2CO3和NaHCO3;生成CO2气体时,发生反应HCO3-+H+=H2O+CO2↑,根据n=cV计算n(HCl),再根据方程式计算二氧化碳的体积;
(3)先向氢氧化钠溶液中通入二氧化碳,后向通入二氧化碳的氢氧化钠溶液中滴加盐酸,当二氧化碳气体完全放出时,溶液的溶质是氯化钠,该反应的实质是盐酸和氢氧化钠反应生成氯化钠,根据盐酸的物质的量计算氢氧化钠的物质的量浓度.
解答 解:(1)由图可知,对应A溶液来说,滴加盐酸60mL时没有气体生成,可能发生OH-+H+=H2O和CO32-+H+=HCO3-,假设原溶液中只有碳酸钠,生成碳酸氢钠需要盐酸的体积和碳酸氢钠生成氯化钠需要盐酸的体积相等,实际上需要盐酸的体积为60mL,远远大于碳酸氢钠生成氯化钠需要盐酸的体积(75-60)mL=15mL,说明原溶液中的溶质是NaOH和Na2CO3;
生成二氧化碳消耗盐酸的体积为:75mL-60mL=15mL,生成CO2气体时,发生反应HCO3-+H+=H2O+CO2↑,由方程式可知:n(CO2)=n(HCl)=0.015L×0.1mol/L=0.0015mol,标况下体积为0.0015mol×22.4L/mol=0.0336L=33.6mL,
故答案为:NaOH、Na2CO3;33.6;
(2)对于B溶液来说,假设原溶液中只有碳酸钠,生成碳酸氢钠需要盐酸的体积和碳酸氢钠生成氯化钠需要盐酸的体积相等,实际上需要盐酸的体积25mL小于碳酸氢钠生成氯化钠需要盐酸的体积(75-25)mL=50mL,说明原溶液中的溶质是Na2CO3和NaHCO3,生成二氧化碳消耗盐酸的体积为75mL-25mL=50mL,生成CO2气体时,发生反应HCO3-+H+=H2O+CO2↑,由方程式可知,n(CO2)=n(HCl)=0.05L×0.1mol/L=0.005mol,标况下体积为0.005mol×22.4L/mol=0.112L=112mL,
故答案为:Na2CO3和NaHCO3;112;
(3)先向氢氧化钠溶液中通入二氧化碳,后向通入二氧化碳的氢氧化钠溶液中滴加盐酸,当二氧化碳气体完全放出时,溶液的溶质是氯化钠,该反应的实质是盐酸和氢氧化钠反应生成氯化钠,盐酸和氢氧化钠反应的物质的量之比为1:1,
设氢氧化钠的物质的量浓度为cmol/L,加入75mL盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液;根据氯离子、钠离子守恒,所以n(NaOH)=n(NaCl)=n(HCl)=0.075L×0.1mol/L=7.5×10-3mol,c(NaOH)=$\frac{n}{V}$=$\frac{7.5×1{0}^{-3}mol}{0.01L}$=0.75mol/L,根据溶液具有均一性可知,原NaOH溶液的浓度为0.75mol/L,
故答案为:0.75mol/L.
点评 本题考查混合物的有关计算,侧重分析与计算能力、图象与反应对应关系判断能力的考查,根据消耗盐酸体积判断溶质成分为解答关键,题目难度较大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤⑥ | B. | ④⑥ | C. | ②④⑦ | D. | ③④⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
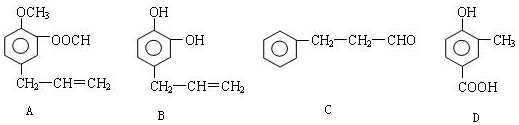
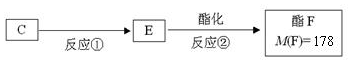
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.3 g | B. | 3.45 g | C. | 1.15 g | D. | 0.575 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分散系的分类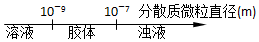 | |
| B. | Fe与Cl2反应的产物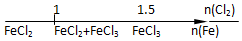 | |
| C. | 向AlCl3溶液滴加NaOH溶液后铝的存在形式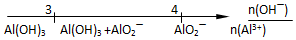 | |
| D. | Na与O2反应的产物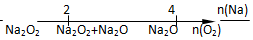 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 砝码质量/g | 50 | 20 | 20 | 10 | 5 |
| 称量(取用砝码过程) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(NO3 )2(溶液) | B. | K2CO3(溶液) | C. | CH3COOK(固体) | D. | CuSO4 (固体) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com