
【题目】(1)现有CuO和Fe2O3组成的混合物ag,向其中加入2 molL﹣1的硫酸溶液50 mL,恰好完全反应。若将ag该混合物在足量H2中加热,使其充分反应,计算冷却后剩余固体质量_________。
(2)取一定量的CuO粉末与0.5 L稀硫酸充分反应后,将一根50 g铁棒插入上述溶液中,至铁棒质量不再变化时,铁棒增重0.24 g。并收集到224 mL气体(标准状况)。求此CuO粉末的质量_________。
【答案】ag﹣1.6 g 8 g
【解析】
(1)CuO和Fe2O3的混合物与硫酸溶液反应生成盐和水,根据元素守恒,硫酸的物质的量与金属氧化物中O元素的物质的量相等;n(H2SO4)=0.05 L×2 mol·L-1=0.1 mol,金属氧化物中O的质量为0.1 mol×16 g·mol-1=1.6 g。将混合物与氢气完全反应后,剩余固体为金属单质,其质量为ag﹣1.6 g。
(2)氧化铜与硫酸反应生成硫酸铜和水,生成的硫酸铜与铁反应生成硫酸亚铁和铜,生成的铜附着在铁的表面,铁与硫酸反应生成氢气的体积为224 mL气体(标准状况),则n(H2)=0.01mol,根据铁和稀硫酸反应的化学方程式:Fe+H2SO4=FeSO4+H2↑,可知消耗的铁的物质的量和生成的氢气的物质的量相等,即0.01mol,所以和稀硫酸反应消耗的铁的质量为0.56g。反应后铁棒质量增重0.24g,说明铁与硫酸铜反应时增重的质量为0.24 g+0.56 g=0.8 g。设硫酸铜的质量为y,
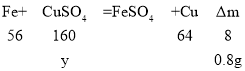
y=16 g
硫酸铜的物质的量是![]() ,根据铜元素守恒,氧化铜的物质的量为0.1mol,氧化铜的质量为0.1mol×80g/mol=8g;
,根据铜元素守恒,氧化铜的物质的量为0.1mol,氧化铜的质量为0.1mol×80g/mol=8g;
所以此CuO粉末的质量为8 g。


科目:高中化学 来源: 题型:
【题目】人类冶炼最多的金属元素是_______;请写出它与水在一定条件反应的化学方程式________熔点最低的金属是_________;导电性最好的金属是_________;人体内最多的金属元素是_________;海水中含量最多的金属元素是_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
A.如图表示反应2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0在有无催化剂时的能量变化
2SO3(g) ΔH<0在有无催化剂时的能量变化
B.如图表示电解精炼铜时纯铜和粗铜的质量随时间的变化
C.如图表示铅蓄电池放电时负极质量随转移电子物质的量的变化
D.如图表示反应2NO2(g)![]() N2O4(g)和2NO2(g)
N2O4(g)和2NO2(g)![]() N2O4(l)的能量变化
N2O4(l)的能量变化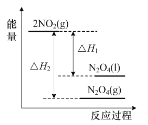
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氧化三铁俗称为磁性氧化铁,通常用作颜料、抛光剂和电讯器材等。某化学兴趣小组取磁性氧化铁进行铝热反应实验并对产物进行探究。
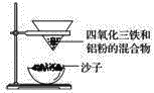
(1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是__________。
(2)取少许反应生成的“铁块”溶于盐酸,滴加硫氰化钾溶液后溶液不变红,则______(填“能”或“不能”)说明“铁块”一定不含四氧化三铁,理由是_________。
(3)设计一个简单的实验方案,证明上述所得的“铁块”中含有金属铝,该实验所用的试剂是__________,反应的离子方程式为___________。
(4)请写出此铝热反应的化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列事实书写的离子方程式正确的是( )
A.用酸性高锰酸钾标准溶液滴定草酸:![]()
B.向![]() 溶液中加入
溶液中加入![]() 溶液得到
溶液得到![]() 沉淀:
沉淀:![]()
C.向![]() 溶液中加入足量稀氨水:
溶液中加入足量稀氨水:![]()
D.用铁电极电解饱和食盐水:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知部分被氧化的镁条1.6 g,和足量的盐酸反应,在标准状况下生成H21.12 L,在跟盐酸反应前被氧化的镁是 ( )
A.1.2 gB.0.64 gC.0.4 gD.0.24 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应,X2++Z=X+Z2+,Y+Z2+=Y2++Z。这四种离子被还原成0价时,表现的氧化性强弱顺序为( )
A.R2+>X2+>Z2+>Y2+B.X2+>R2+>Y2+>Z2+
C.Y2+>Z2+>R2+>X2+D.Z2+>X2+>R2+>Y2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①H2(g)+![]() O2(g)=H2O(g) ΔH1=akJ·mol1
O2(g)=H2O(g) ΔH1=akJ·mol1
②2H2(g)+O2(g)=2H2O(g) ΔH2=bkJ·mol1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=ckJ·mol1
O2(g)=H2O(l) ΔH3=ckJ·mol1
④2H2(g)+O2(g)=2H2O(l) ΔH4=d kJ·mol1
下列关系式中正确的是
A.a<c<0B.b>d>0C.2a=b<0D.2c=d>0
查看答案和解析>>
科目:高中化学 来源: 题型:
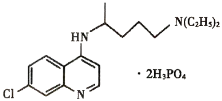
【题目】磷酸氯喹(结构如图所示)在细胞水平上能有效抑制新型冠状病毒的感染,我国印发的《新型冠状病毒肺炎诊疗方案(试行第七版)》中明确规定了其用量。
(1)碳、硅、锗为同一主族元素,则基态硅原子核外电子的空间运动状态有________种,基态锗原子的最外层的电子排布图为__________________。
(2)C、N、O三种元素第一电离能由大到小的顺序是_____________________。
(3)磷酸氯喹分子中氮原子的杂化方式为________,苯环中含有的共价键类型是________。
(4)![]() 的空间构型是____________,与
的空间构型是____________,与![]() 互为等电子体的分子是____________(写一种即可)。
互为等电子体的分子是____________(写一种即可)。
(5)由C、H、O元素组成的H2O和C2H5OH可以任意比例互溶,其原因是________________。
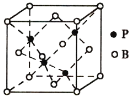
(6)由P与B元素形成的化合物BP的晶胞(如图所示)中B采用面心立方堆积,P原子填入四面体空隙中。已知晶胞边长为a pm,晶体中B原子与P原子的最近距离是___________,设阿伏加德罗常数的值为NA,则BP晶体的密度是___________g/cm3(列出计算表达式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com