
【题目】关于元素周期表的叙述中正确的是( )
A. 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料元素
B. 在过渡元素中可以寻找制备催化剂
C. 在元素周期表的右上角可以寻找制备耐高温和耐腐蚀的元素
D. 在地球上元素的分布和它们在元素周期表中的位置有密切关系
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】(1)某同学设计了如下实验流程:在一个小烧杯里,加入20g Ba(OH)2·8H2O晶体和10gNH4Cl晶体,然后将小烧杯放在事先已滴有3滴~4滴水的玻璃片上,并立即用玻璃棒迅速搅拌。实验流程示意图如下,回答下列问题:
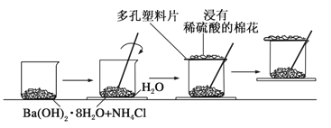
①实验中玻璃棒的作用是_______。
②浸有稀硫酸的棉花的作用是______。
(2)沼气是一种廉价能源,农村存在大量的秸秆、杂草等废弃物,它们经微生物发酵之后,便可产生沼气,可用来点火做饭。在农村推广建造沼气池,不仅能有效地利用____能,还能为农业生产提供优良的肥料。已知:标准状况下的112.0LCH4气体完全燃烧,生成CO2和液态水,放出4448kJ的热量。
①写出CH4完全燃烧的热化学方程式为________。
②如果上述反应生成的是水蒸气,则反应放出的热量___4448kJ。(填“>”或“<”或“=”)
(3)钢铁在潮湿的空气中生锈主要是由电化学腐蚀造成的,发生腐蚀时铁和内部的杂质碳及钢铁表面的电解质溶液形成原电池。钢铁发生吸氧腐蚀时正极的电极反应式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中,发生可逆反应mA(g) + nB(g) ![]() pC(g) + qD(g),当m、n、p、q为任意整数时,反应达到平衡的标志是( )
pC(g) + qD(g),当m、n、p、q为任意整数时,反应达到平衡的标志是( )
②体系温度不再改变
③各组分的浓度不再改变
④各组分的质量分数不再改变
⑤反应速率v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q
⑥单位时间内m mol A断键反应,同时p mol C也断键反应
⑦体系的密度不再变化
A.③④⑤⑥ B.②③④⑥
C.①③④⑤ D.③④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知KMnO4和H2C2O4(草酸)在酸性溶液中会发生氧化还原反应。甲、乙两个实验小组欲探究影响化学反应速率的因素,设计实验方案如下(实验中所用KMnO4溶液均已酸化)
(1)甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率,实验装置如图所示:

实验时仪器中的A溶液一次性加入,A、B的成分见下表:
序号 | A溶液 | B溶液 |
① | 2 mL 0.1 mol·L-1H2C2O4溶液 | 4 mL 0.01 mol·L-1KMnO4溶液 |
② | 2 mL 0.2 mol·L-1H2C2O4溶液 | 4 mL 0.01 mol·L-1KMnO4溶液 |
③ | 2 mL 0.2 mol·L-1H2C2O4溶液 | 4 mL 0.01 mol·L-1KMnO4溶液,少量MnSO4固体(催化剂) |
①盛放A溶液的仪器名称_______,锥形瓶中反应的化学方程式:______
②该实验探究的是_____因素对化学反应速率的影响。在反应停止之前,相同时间内针筒中所得CO2的体积由大到小的顺序是____(填实验序号)。
(2)乙组:通过测定KMnO4溶液褪色所需时间的长短来比较化学反应速率。
取两支试管各加入2 mL 0.1 mol·L-1H2C2O4溶液,另取两支试管各加入4 mL 0.1 mol·L-1KMnO4溶液,将四支试管分成两组(每组各有一支试管盛有H2C2O4溶液和KMnO4溶液),一组放入冷水中,另一组放入热水中,一段时间后,分别混合并振荡,记录溶液褪色所需时间。该实验试图探究________因素对化学反应速率的影响,但该组同学始终没有看到溶液完全褪色,其原因是______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2 ![]() 2SO3(正反应放热),反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
2SO3(正反应放热),反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
请回答下列问题:
(1)判断该反应达到平衡状态的标志是______。(填字母)
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.容器中气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)求该反应达到平衡时SO2的转化率______(用百分数表示)。(写出计算过程)
(3)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀多少克?(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容下,将2 mol A气体和2 mol B气体通入体积为2 L的密闭容器中发生如下反应:2A(g)+B(g)![]() xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol·L-1。
xC(g)+2D(s),2 min时反应达到平衡状态,此时剩余1.2 mol B,并测得C的浓度为1.2 mol·L-1。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为_______________________
(2)x=________。
(3)A的转化率为_____________。
(4)下列各项可作为该反应达到平衡状态的标志的是________。
A.压强不再变化
B.气体密度不再变化
C.气体的平均相对分子质量不再变化
D.A的消耗速率与B的消耗速率之比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据事实,写出下列反应的热化学方程式。
(1)1 mol C2H4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出1411 kJ能量: 。
(2)1 mol C2H5OH(l)与适量O2(g)反应生成CO2(g)和H2O(l),放出1366.8 kJ热量: 。
(3)2 mol Al(s)与适量O2(g)发生反应生成Al2O3(s),放出1669.8 kJ热量: 。
(4)在200°C、101 kPa时,1 mol H2与碘蒸气作用生成HI气体,放出14.9 kJ热量: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用如图装置进行中和热的测定,请回答下列问题:

(1)做1次完整的中和热测定实验,温度计至少需使用________次,某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和碱的温度,你是否同意该同学的观点,为什么?_______________。
(2)实验室用50 mL 0.50 mol·L-1盐酸,50 mL 0.55 mol·L-1 NaOH溶液进行测定中和热的实验,为了把测量数据记录下来,请你设计表格__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z、M、G五种短周期元素,原子序数依次增大。W、Z同主族,可形成离子化合物ZW;Y、M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性。请回答下列问题:
(1)Y在元素周期表中的位置为___________;
(2) W、Y、Z、G形成的简单离子的半径大小顺序是___________(用化学符号表示)
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有________ (任写两个)
(4)ZW的电子式为___________,W2Y2的电子式为______
(5)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,请用相关离子方程式解释原因________。
(6)已知
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是是___________ ;制铝时,电解Al2O3而不电解AlCl3的原因是___________ 。
(7)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N≡N放出942kJ热量。根据以上信息和数据,下列说法正确的是___________ 。

A.N4属于一种新型化合物 B.N4晶体熔点高,硬度大
C.相同质量的N4的能量高于N2 D.1molN4转变为N2将吸收882kJ的能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com