
| A. | 硫化羰在氧气中完全燃烧后的生成物是CO2和SO2 | |
| B. | C3O2与CO一样可以在氧气中燃烧生成CO2 | |
| C. | COS分子中所有原子都满足8电子稳定结构 | |
| D. | CO、C3O2、CO2都是碳的氧化物,它们互为同素异形体 |
分析 A.燃烧遵循元素守恒,生成稳定氧化物;
B.C3O2与CO中C元素的化合价分别为+3、+2价;
C.硫化羰与二氧化碳的结构相似,结构式为S=C=O;
D.同种元素的不同单质互为同素异形体.
解答 解:A.由元素守恒可知,硫化羰在氧气中完全燃烧后的生成物是CO2和SO2,故A正确;
B.C3O2中碳元素的化合价为+3价和CO中碳元素的化合价为+2价,碳元素充分燃烧的产物是二氧化碳,其中碳元素的化合价为+4价,所以C3O2和CO一样可以燃烧生成CO2,故B正确;
C.硫化羰与二氧化碳的结构相似,结构式为S=C=O,O、S最外层有6个电子,C最外层有4个电子,则分子中所有原子都满足8电子稳定结构,故C正确;
D.同种元素的不同单质互为同素异形体,而CO、C3O2、CO2都是碳的氧化物,为不同化合物,故D错误;
故选D.
点评 本题考查共价键及物质的性质,为高频考点,把握习题中的信息及共价键的形成为解答的关键,侧重分析与应用能力的考查,注意迁移能力的应用,题目难度不大.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的摩尔质量等于其相对分子(原子)质量 | |
| B. | “物质的量”是国际单位制中的一个基本单位 | |
| C. | 0.012kg 12C中所含的碳原子数为NA | |
| D. | 1 mol任何物质都含有约6.02×1023个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是两种或两种以上的物质发生的反应都属于化合反应 | |
| B. | 在反应中,不一定所有元素的化合价都发生变化 | |
| C. | 一种元素被氧化,一定有另一种元素被还原 | |
| D. | 物质只有和氧气发生反应才是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1 | B. | 0.3mol•L-1 | C. | 0.2mol•L-1 | D. | 0.4mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 羰基硫与烧碱溶液反应生成水和两种正盐的离子方程式为COS+4NaOH=Na2S+Na2CO3+2H2O羰基硫的脱硫常用两种方法,其反应式分别为:
羰基硫与烧碱溶液反应生成水和两种正盐的离子方程式为COS+4NaOH=Na2S+Na2CO3+2H2O羰基硫的脱硫常用两种方法,其反应式分别为:| 化学键 | C=O(CO2) | C=O(COS) | C=S | H-S | H-O |
| 键能(kJ/mol) | 803 | 742 | 577 | 339 | 465 |
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | mmolCO2、3mmolH2、 nmolCH3OH(g)、nmolH2O(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
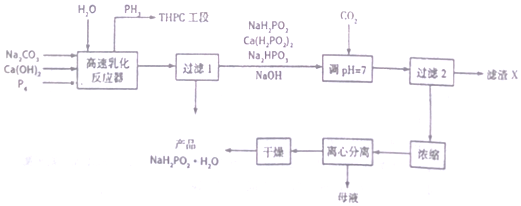
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠、盐酸都为强电解质 | |
| B. | 铁生锈、食物腐败都有氧化反应发生 | |
| C. | 糖类、蛋白质都为高分子化合物 | |
| D. | 一氧化碳和二氧化碳都是酸性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com